-
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是
A.Z2Y B.X2Y2 C.Z2Y2 D.ZYX
难度: 中等查看答案及解析
-
现有三种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.第一电离能:③>②>① B.原子半径:③>②>①
C.电负性:③>②>① D.最高正化合价:③>②>①
难度: 简单查看答案及解析
-
下列有关表述正确的是( )
A.次氯酸的电子式:
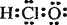
B.N原子的电子排布图为:

C.硫原子的价电子排布式:3s23p4
D.二氧化硅的分子式:SiO2
难度: 简单查看答案及解析
-
下列过程没有破坏化学键的是
A.2O3=3O2 B.干冰升华 C.金刚石受热融化 D.HCl气体溶于水
难度: 简单查看答案及解析
-
下列叙述中正确的是
A.CO、CO2都是极性分子 B.H2O2、C2H2都是直线型分子
C.CH4、CCl4都是含有极性键的非极性分子 D.BF3、NCl3都是平面三角形分子
难度: 中等查看答案及解析
-
下列各分子中所有原子都满足最外层8电子稳定结构且共用电子对发生偏移的是
A.BeCl2 B.PCl3 C.PCl5 D.N2
难度: 中等查看答案及解析
-
下列四种分子中中心原子杂化类型与三个不同的是( )
A.CH4 B.NH3 C.H2O D.BF3
难度: 简单查看答案及解析
-
在基态多电子原子中,关于核外电子的叙述正确的是
A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转
B.电子从低能级跃迁到高能级的过程中一定要释放能量
C.在同一能级上运动的电子,其运动状态一定相同
D.能量低的电子在离核近的区域运动,能量高的电子在离核远的区域运动
难度: 简单查看答案及解析
-
已知Be在周期表中位于Al的左上方,则下列有关Be的说法中错误的是
A.单质Be与酸或碱反应都能放出氢气 B.Be(OH)2为两性氢氧化物
C.Be的氧化物的化学式为Be2O3 D.BeCl2晶体属于分子晶体
难度: 中等查看答案及解析
-
下列变化或数据与氢键无关的是
A.水凝结成冰时,密度变小 B.氨分子与水分子生成一水合氨
C.水在2000℃时,只有4%的H2O发生分解 D.水的沸点比同主族元素氢化物的高
难度: 中等查看答案及解析
-
下列各组微粒属于等电子体的是
A.C2H2和N2 B.NO和NO2
C.CH4和NH3 D.CO2和N2O
难度: 中等查看答案及解析
-
已知氯化铝易溶于苯和四氯化碳,其熔点为190℃,则下列结论错误的是
A.氯化铝是电解质 B.固体氯化铝是分子晶体
C.可用电解熔融氯化铝的办法制取金属铝 D.氯化铝为非极性分子
难度: 中等查看答案及解析
-
下列各组无机酸的酸性强弱比较正确的是
A.HClO>HClO2>HClO3>HClO4 B.HF<HCl<HBr<HI
C.H2CO3<H2SiO3<H2GeO3 D.HNO3<H3PO4
难度: 简单查看答案及解析
-
下列说法正确的是 ( )
A.元素周期表每一周期元素原子的最外层电子排布均是从ns1 过渡到ns2np6
B.所有的非金属元素都分布在p区
C.原子核外电子排布式为1s1的原子与原子核外电子排布式为1s22s1的原子的化学性质相似
D.元素周期表中ⅢB到ⅡB的10个纵行的元素都是金属,所以统称过渡金属元素
难度: 极难查看答案及解析
-
Na3N是离子化合物,它能与水反应生成氨气。下列关于Na3N的说法中错误的是
A.在Na3N与水反应中Na3N是还原剂
B.Na3N与盐酸反应时生成两种盐
C.Na3N分子中Na+的半径比N3-的半径小
D.Na+与N3-的核外电子排布都与氖原子的相同
难度: 中等查看答案及解析
-
已知X、Y是主族元素,I为电离能,单位是kJ/mol。根据下表所列数据判断错误的是
元素
I1
I2
I3
I4
X
496
4562
6912
9543
Y
578
1817
2745
11600
A.元素X的常见化合价是+1价
B.元素X与氯形成化合物时,化学式为XCl
C.元素Y是ⅢA族的元素
D.若元素Y处于第3周期,它可与冷水剧烈反应
难度: 中等查看答案及解析
-
下列叙述不正确的是
A.在干冰晶体中,每一个二氧化碳分子周围有12个二氧化碳分子紧密相邻
B.金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子
C.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D.在12g金刚石晶体中,含共价键为2NA
难度: 中等查看答案及解析
-
“类推”是一种重要的学习方法,但有时会产生错误的结论,下列类推结论中正确的
A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序是:HCl>H2S>PH3
B.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序是:AsH3>PH3>NH3
C.二甲苯的沸点顺序是:邻二甲苯>对二甲苯;则羟基苯甲醛的沸点顺序是:邻羟基苯甲醛>对羟基苯甲醛
D.根据“相似相溶”,乙醇能与水以任意比互溶,则戊醇也能与水以任意比互溶
难度: 中等查看答案及解析
-
在核电荷数为26的元素Fe的基态原子核外的3d、4s轨道内,下列电子排布图正确的是
A.
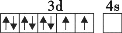 B.
B.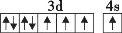
C.
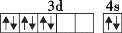 D.
D.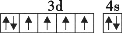
难度: 简单查看答案及解析
-
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是
A.X3YZ3 B.X2YZ2 C.XYZ2 D.XYZ3
难度: 中等查看答案及解析