-
科学家在月球表面的土壤里发现了一种非常珍贵的资源—
He,它是可控核聚变的原料,关于:
He的叙述正确的是( )
A.
He核内中子数比质子数多l
B.
He和
He互为同位素
C.He元素的相对原子质量就是3
D.
He和
He属于同种元素,所以物理性质和化学性质都相同
难度: 简单查看答案及解析
-
元素符号、结构示意图、电子式、结构式等通常叫做化学用语,下列化学用语错误的是( )
A.CO2分子的电子式为:
B.NaOH的电子式为:

C.Cl-的结构示意图为:
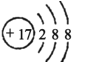
D.HClO的结构式为:H-Cl-O
难度: 简单查看答案及解析
-
在下列物质中,所含化学键类型相同的一组是( )
A.Na2O2、H2O2 B.Na2S、SO2
C.CCl4、CH4 D.NH4Cl、HCl
难度: 简单查看答案及解析
-
下列有关物质结构的描述,正确的是( )
①溴苯分子中的所有原子不可能共平面
②乙烯分子中的所有原子共平面
③二氯甲烷分子为正四面体结构
④乙烷分子中的所有原子不可能都在同一平面内
A.①③ B.②④ C.①④ D.②③
难度: 简单查看答案及解析
-
下列有关元素周期表的说法,正确的是( )
A.元素周期表一共有18个纵行,18个族
B.元素周期表中IA族元素和IVA族元素,原子序数相差值可能为:3,13,27
C.元素周期表中同主族元素的原子序数之差可能为:2,8,18,25等
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
难度: 简单查看答案及解析
-
若甲烷与氯气以物质的量之比1:3混合于试管中进行如下实验(如图),下列对于试管内发生的反应及现象的说法正确的是( )
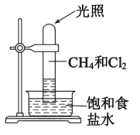
A.反应完全后,向饱和食盐水中加入紫色石蕊试液无变化
B.甲烷和Cl2反应后的产物只有CHCl3和HCl两种产物
C.反应过程中试管内黄绿色逐渐消失,试管壁上有油珠产生
D.CH4和Cl2完全反应后液面上升,液体充满试管
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.离子键就是阴、阳离子间的静电引力
B.所有金属元素与所有非金属元素之间都能形成离子键
C.HCl在水中能电离出H+和Cl-,所以HCl由H+和Cl-构成
D.某化合物熔融态能导电,则该化合物中一定含有离子键
难度: 简单查看答案及解析
-
下列说法错误的是( )
A.白磷和红磷互称为同素异形体
B.
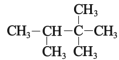 和
和 互称为同分异构体
互称为同分异构体C.C2H6和C4H10互为同系物
D.正戊烷和异戊烷是同分异构体
难度: 简单查看答案及解析
-
核电荷数小于18的某元素X,其原子核外的电子层数为n,最外层电子数为(2n+1),原子核内质子数是(2n2-1),则下列有关X的说法错误的是( )
A.X的最低价氢化物易溶于水,且水溶液一定显酸性
B.X的最高价氧化物对应的水化物都为强酸
C.X的最高正价可能为+7价
D.X形成的单质可能无色,且常温下为气体
难度: 中等查看答案及解析
-
下列物质中都能使酸性KMnO4溶液褪色的是( )
①甲烷②苯③乙醇④乙烯⑤乙酸
A.②⑤ B.③④ C.②④ D.①③
难度: 简单查看答案及解析
-
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍。下列说法正确的是( )
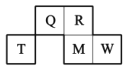
A.简单离子半径大小顺序为r(M)>r(W)>r(Q)>r(R)
B.Q、W的单核离子的核外电子数相等
C.铁常温下不能和M的最高价含氧酸的浓溶液发生化学反应
D.W最低价氢化物的还原性比M最低价氢化物的还原性强
难度: 中等查看答案及解析
-
下列有机反应方程式书写错误的是( )
A.
+HO-NO2
+H2O
B.nCH2=CH2
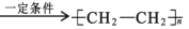
C.CH3COOH+CH3CH2OH
H2O+CH3COOCH2CH3
D.2CH3CH2OH+O2
2CH3CHO
难度: 简单查看答案及解析
-
根据同主族和同周期元素性质的递变性分析下面的推断,其中正确的是( )
A.已知Ca是第四周期IIA族元素,故Ca(OH)2的碱性比Mg(OH)2的碱性弱
B.已知As是第四周期VA族元素,故AsH3的稳定性比NH3的稳定性强
C.已知Cs是第六周期IA族元素,故Cs与水反应比Na与水反应剧烈
D.已知Se是第四周期VIA族元素,故Se的最高价氧化物对应水化物的酸性比硫酸的酸性强
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.乙烯的结构简式是CH2CH2
B.乙酸和乙醇都既能与钠反应产生气体,又能与碳酸钠反应产生气体
C.C4H10的一氯取代物共有4种
D.标准状况下,22.4L氯仿中含有3molCl原子
难度: 中等查看答案及解析
-
现有7种元素的性质如下表所示,它们位于第二或第三周期,下列判断错误的是( )
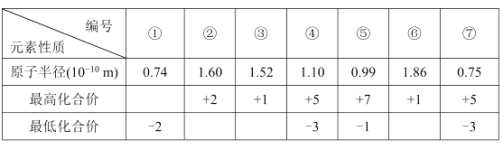
A.编号为⑥的元素比编号为②的元素金属性强,所以⑥的单质能从②形成的盐溶液中置换出②的单质
B.编号为④⑤的原子之间可形成共价化合物
C.编号为⑦的元素的最低价氢化物与最高价氧化物对应的水化物能反应生成盐
D.编号为⑥的单质一般保存在煤油中
难度: 中等查看答案及解析
-
短周期元素W、X、Y和Z的原子序数依次增大。元素W是第二周期原子半径最大的元素,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A.元素W与氯形成的化合物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1:2的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
难度: 中等查看答案及解析
-
下列每组物质分别混合后,能发生反应,且甲组为取代反应,乙组为加成反应的是( )
选项
甲
乙
A
苯与溴水
乙烯与水(条件:催化剂)
B
乙酸与乙醇(条件:加入浓硫酸、加热)
苯与氢气(条件:催化剂、加热)
C
乙烯与酸性高锰酸钾溶液
将苯、浓硫酸、浓硝酸混合(条件:在50~60°C水浴中加热)
D
乙烯与溴的四氯化碳溶液
甲烷与氯气(条件:光照)
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
A、B、C是同主族的三种元素,已知其最高价氧化物对应的水化物的酸性由强到弱的顺序是HAO4>HBO4>HCO4。下列说法正确的是( )
A.简单离子半径:A>B>C B.元素的非金属性:A<B<C
C.气态氢化物的稳定性:A<B<C D.原子序数:A<B<C
难度: 中等查看答案及解析
-
X、Y、Z、W、R属于短周期主族元素。X元素是短周期主族元素中金属性最强的元素,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,Y元素原子与R元素原子的核外电子数之比为1:2。下列叙述正确的是( )
A.Y的最低价氢化物的沸点比R的最低价氢化物的沸点低
B.Z、W、R按最高价氧化物对应水化物的酸性强弱排列顺序是R>Z>W
C.X2Y2化合物中的化学键与X2Y中的化学键类型完全相同
D.RY2能使品红溶液褪色,是因为RY2具有漂白性
难度: 中等查看答案及解析
-
为提纯下列物质(括号内为杂质),所用的除杂试剂和最佳分离方法都正确的是( )
选项
不纯物
除杂试剂
最佳分离方法
A
苯(Br2)
NaOH溶液
分液
B
CH4(C2H4)
酸性高锰酸钾溶液
洗气
C
C2H5OH(H2O)
新制生石灰
过滤
D
乙酸乙酯(乙酸)
饱和Na2CO3溶液
蒸发
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m<n,对下列叙述的判断正确的是( )
①元素的原子序数a>b>c>d②c-n=d-m③离子半径Z>R>X>Y④元素金属性Y>X⑤最低价氢化物的热稳定性R>Z
A.①②③正确 B.③④正确
C.①②③④⑤都正确 D.③⑤正确
难度: 简单查看答案及解析
-
短周期主族元素a、b、c、d的原子序数依次增大,X、Y、Z均是由这些元素组成的二元化合物,它们存在转化关系:M
X↑+Y↑+Z,组成化合物X的原子个数比为1:3,且液态X常用作制冷剂,Y的排放是形成酸雨的主要原因,且Y的组成元素位于同一主族且原子序数相差8,常温常压下Z为无色液体。下列说法错误的是( )
A.原子半径:d>b>c>a
B.b的最低价氢化物能使湿润的蓝色石蕊试纸变红
C.M既能与强酸溶液反应,又能与强碱溶液反应
D.b2c5、dc3均为酸性氧化物
难度: 中等查看答案及解析