-
有下列物质:①金属铜 ②NaOH ③I2 ④MgCl2 ⑤Na2O2 ⑥氩气 回答下列问题:
(1)不存在化学键的是_________________________
(2)只存在非极性键的是__________________________
(3)只存在离子键的是__________________________
(4)既存在离子键又存在极性键的是__________________________
(5)既存在离子键又存在非极性键的是____________________________
难度: 简单查看答案及解析
-
利用如图所示的装置收集以下7种气体:①H2 ②Cl2 ③O2 ④HCl ⑤NH3 ⑥NO ⑦NO2
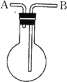
⑴若烧瓶是干燥的,则由B口进气,可收集的气体有___,若把装置颠倒,由A口进气,可收集的气体有____。
⑵若在烧瓶内充满水,可收集的气体有____,气体应由____口进入。
⑶若烧瓶中装入适量浓硫酸,可以用它来干燥的气体有____,气体应由____口进入。
难度: 简单查看答案及解析
-
已知:①SO2中S元素的化合价+4价,既可以升高为+6价,又可以降低为0价,因此SO2既体现了氧化性又体现了还原性。SO2能与氯水、溴水、碘水等发生如下类型的反应:SO2+X2+2H2O=2HX+H2SO4,(其中X2表示Cl2、Br2或I2)②SO2具有漂白性:SO2能与大部分有机色质化合生成不稳定的无色物质,该无色物质在受热条件下又会变为原来的有色物质,但SO2不能漂白酸碱指示剂。
试根据以上信息,回答下列问题:
⑴二氧化硫能使浸过溴水的滤纸褪色,这说明了_______;
A.SO2的漂白性 B.溴的挥发性 C.SO2的氧化性 D.SO2的还原性
⑵将二氧化硫通入品红溶液,可以看到溶液______,这体现了二氧化硫的_____性;
⑶相同状况,将1体积SO2和1体积Cl2同时通入品红溶液,可观察到品红溶液______;
A.立刻褪色 B.慢慢褪色 C.先褪色,后复原 D.颜色不褪
⑷上述现象的原因是___________(用离子方程式表示)。
难度: 简单查看答案及解析