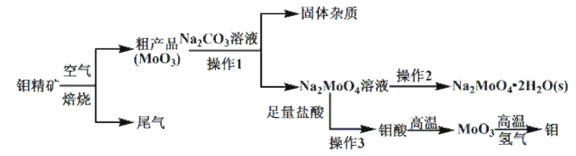
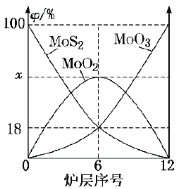
-
下列与我国科技成果有关的说法,不正确的是( )

中国天眼

蛟龙号潜水器

飞机

港珠澳大桥
A.传输信息用的光纤材料是硅
B.用到钛合金,22号钛元素属于过渡元素
C.用到的氮化硅陶瓷是新型无机非金属材料
D.用到的合金材料,具有强度大、密度小、耐腐蚀等性能
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
设
为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,
中所含中子数为
B.
溶液中含有
数目小于
C.熔融状态下,
中所含阳离子数目为2
D.25°C时,
的碳酸钠溶液中,由水电离出的
数目为
难度: 中等查看答案及解析
-
下列关于有机物的说法,正确的是( )
A.油脂和氨基酸在一定条件下均可以与氢氧化钠溶液反应
B.聚乙烯和聚氯乙烯的单体都是不饱和烃,均能使溴水褪色
C.糖类化合物都具有相同的官能团
D.通过石油分馏获得乙烯,已成为目前工业上生产乙烯的主要途径
难度: 简单查看答案及解析
-
下表中相关物质的信息都正确的一项是( )
选项
化学式
物质的性质
与性质相对应的用途
A
水溶液呈弱碱性
工业制硝酸
B
具有两性
耐高温材料
C
强氧化性
消毒液
D
受热易分解
泡沫灭火器
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.与金属铝反应放出氢气的溶液:
B.能使紫色石蕊试液变蓝色的溶液:
C.
溶液:
D.
的溶液:
难度: 中等查看答案及解析
-
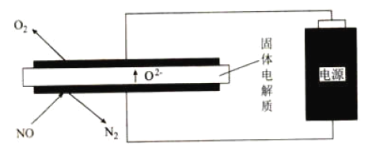
催化
还原
的机理示意图如下。下列说法不正确的是( )
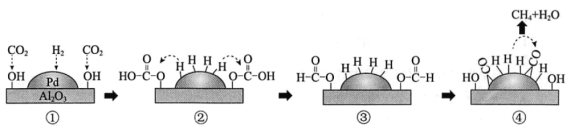
A.
的断裂需要吸收能量 B.①→②,
发生加成反应
C.④中,
被氧化为
D.生成
总反应的化学方程式是
难度: 中等查看答案及解析
-
下列离子的检验方法一定正确的是( )
A.向某溶液中滴加
溶液,有白色沉淀,再滴加足量稀
,若沉淀不溶解,则原溶液中一定含
B.向某溶液中滴加
溶液,若出现红色则原溶液中含
C.向某溶液中滴加足量稀盐酸,产生气体使澄清石灰水变浑浊,则原溶液中含
D.用铂丝蘸取某溶液在酒精灯火焰上灼烧,未观察到紫色火焰,则原溶液中不含
难度: 中等查看答案及解析
-
由下列实验及现象不能得出相应结论的是( )
实验
现象
结论
A
向浓度均为
的
和
溶液中分别滴加酚酞
溶液不变色,
溶液变成红色
非金属性:
B.
向含有酚酞的
溶液中加入少量
固体
观察到红色变浅
证明
溶液中存在水解平衡
C
室温下,用pH试纸测
溶液的pH
约为5
电离大于水解
D.
向盛有10滴
溶液的试管中滴加
溶液,至不再有白色沉淀生成,再向其中滴加
溶液
有黄色沉淀生成
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某无色溶液
中,可能含有
中的一种或几种。现取该溶液适量,向其中加入一定物质的量浓度的稀盐酸,产生沉淀的物质的量(n)与加入盐酸的体积(V)的关系如图所示。下列说法中不正确的是( )
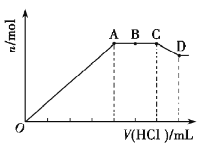
A.溶液
中一定不含
,可能含有
B.
段参加反应的阴离子的物质的量之比为
或
C.
段一定生成了气态物质
D.
段发生反应的离子方程式为:
难度: 困难查看答案及解析
-
根据下列图示所得出的结论正确的是( )
A.
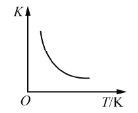 ,反应
,反应的平衡常数与温度的关系,说明该反应的
B.
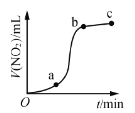 ,
,与过量浓硝酸反应生成的
气体体积随时间的变化关系,说明该反应在b→c时间段内反应速率最快
C.
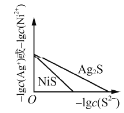 ,常温下
,常温下和
的沉淀溶解平衡曲线,若
时,两者的
相等
D.
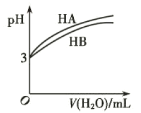 ,常温下
,常温下的
和
溶液分别加水稀释时
的变化曲线,说明两者的电离平衡常数
难度: 中等查看答案及解析
-
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如右,该电池工作时反应为:4VB2+11O2=4B2O3 +2V2O5。下列说法不正确的是
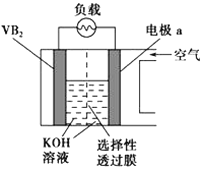
A.电极a 为电池正极
B.图中选择性透过膜为阴离子透过性膜
C.电池工作过程中,电极a附近区域pH减小
D.VB2极发生的电极反应为:2VB2 +22OH——22e- = V2O5 + 2B2O3 + 11H2O
难度: 中等查看答案及解析
-
甲、乙是两种常见的化合物,X、Y、Z是三种常见的单质。下表所列各组物质之间通过一步反应不能实现如图所示转化的是( )
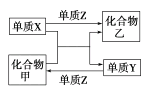
选项
X
Y
Z
甲
乙
A
C
H2
O2
H2O
CO
B
Zn
Fe
Cl2
FeCl2
ZnCl2
C
Mg
C
O2
CO2
MgO
D
H2
Si
Cl2
SiCl4
HCl
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
短周期主族元素
的原子序数依次增大,其中
位于同一主族。
的气态氢化物常用作制冷剂。
与水剧烈反应,可观察到液面上有白雾生成,并有刺激性气味的气体逸出,该气体可使品红溶液褪色。下列说法正确的是( )
A.最简单氢化物的沸点:
B.原子半径:
C.把
通入石蕊试液中,石蕊先变红后褪色
D.向
与水反应后的溶液中滴加
溶液有白色沉淀生成
难度: 中等查看答案及解析
-
25℃时,将浓度均为
的
溶液和
溶液按体积分别为Va和Vb混合,保持
,且生成的
可溶于水。已知
与混合液pH关系如图。下列说法错误的是( )

A.曲线Ⅰ表示
溶液体积 B.
点存在
C.电离平衡常数
D.向
点溶液加入
,水的电离程度减小
难度: 中等查看答案及解析