-
下列叙述中,不属于氮的固定的方法是( )
A.根瘤菌把氮气变为硝酸盐 B.氮气和氢气合成氨
C.从液态空气中分离氮气 D.氮气和氧气合成一氧化氮
难度: 简单查看答案及解析
-
在2A+B=3C+4D反应中,表示该反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
难度: 简单查看答案及解析
-
目前我国城市公布的空气质量报告中的污染物一般不涉及 ( )
A.SO2 B.NO2 C. CO2 C.可吸入颗粒物
难度: 简单查看答案及解析
-
下列化学用语正确的是
A.CO2 的电子式::O::C::O: B.氮气的电子式:
C.氨气的电子式:
D.氯离子的结构示意图:
难度: 简单查看答案及解析
-
不能由单质直接化合而得到的化合物是
A.FeCl3 B.SO2 C.CuS D.FeS
难度: 简单查看答案及解析
-
下列物质中、属于电解质的是
A.氯气 B.铜 C.硫酸钾 D.蔗糖
难度: 简单查看答案及解析
-
下列属于弱电解质的是
A.碳酸钙固体 B.氢氧化钾 C.水 D.二氧化硫
难度: 简单查看答案及解析
-
下列溶液中,呈酸性的是
A.硝酸铵溶液 B.硝酸钾溶液 C.硫化钠溶液 D.碳酸钾溶液
难度: 简单查看答案及解析
-
下列物质不能破坏水的电离平衡的是
A.NaCl B.FeSO4 C.K2CO3 D.NH4Cl
难度: 简单查看答案及解析
-
硫的非金属性弱于氯的非金属性,最主要的事实是
A.通常情况下硫为浅黄色固体,而氯为黄绿色气体。
B.硫不溶于水,而氯气可溶于水。
C.与氢气反应时,硫被还原为-2价,而氯被还原为-1价
D.与Fe反应时,铁被硫氧化成+2价,而被氯气氧化成+3价
难度: 简单查看答案及解析
-
下列气体不能用浓硫酸干燥的是
A.O2 B.H2S C.SO2 D.Cl2
难度: 简单查看答案及解析
-
下列能鉴别CO2和SO2的是
A.品红溶液 B.澄清石灰水 C.紫色石蕊试液 D.氯化钡溶液
难度: 简单查看答案及解析
-
下列叙述正确的是
A.pH=7的溶液一定是中性溶液
B.酸雨就是指呈酸性的雨水
C.医学上可用液氮保存待移植的活性器官
D.浓H2SO4 沾到皮肤上,应先用水冲洗
难度: 简单查看答案及解析
-
能证明SO2有漂白性的是
A.酸性KMnO4溶液中通入SO2气体后,紫色消失
B.品红溶液中通入SO2后,红色消失
C.SO2通入加有NaOH的酚酞溶液后,红色消失
D.溴水通入SO2气体后,橙色消失
难度: 简单查看答案及解析
-
下列反应中硫酸只表现出氧化性的是
A.实验室用浓硫酸干燥氯气、氯化氢等气体
B.将单质碳与浓硫酸混合加热、有刺激性气味气体产生
C.浓硫酸与铜反应,会生成硫酸铜
D.用浓硫酸在木制品上“烙”字画
难度: 简单查看答案及解析
-
医疗上用作X射线透视肠胃的内服药“钡餐”的物质是
A.BaCO3 B.BaO C.BaCl2 D.BaSO4
难度: 简单查看答案及解析
-
下列叙述正确的是
A.常温下,浓硫酸不与铜反应,是因为铜被钝化
B.可用铁罐来进行储存、运输冷的浓硫酸
C.SO3具有氧化性,SO2只有还原性
D.SO2、Cl2的漂白原理相同
难度: 简单查看答案及解析
-
下列叙述中不正确的是
A.氨遇硫酸冒白烟
B.氨在一定条件下能与氧气反应生成一氧化氮和水
C.氨是一种极易溶于水,且易液化的气体
D.氨能使酚酞试液变红色
难度: 简单查看答案及解析
-
能使干燥的红色石蕊试纸变蓝色的物质是
A.氨气 B.液氨 C.氨水 D.NH4Cl溶液
难度: 简单查看答案及解析
-
下列叙述正确的是
A.稀硫酸溶液中不存在H2SO4分子
B.凡是能电离的物质一定能达到电离平衡
C.氯化钠溶液在电流作用下电离成钠离子和氯离子
D.氨水中全部是NH4+、OH-,无分子存在
难度: 简单查看答案及解析
-
下列溶液中导电性最强的是
A.1L 0.1mol/L醋酸 B.0.1L 0.1mol/L H2SO4溶液
C.0.5L pH=1的盐酸 D.2L 0.1mol/L H2SO3溶液
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+
B.2L0.5mol/L Na2SO4溶液中的Na+数目为2NA
C.1.00 mol NaCl中含有NA个NaCl分子
D.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
难度: 中等查看答案及解析
-
关于电解食盐水溶液,下列说法正确的是
A.电解时在阳极得到氯气 B.电解时在阴极得到金属钠
C.电解时在正极得到氯气 D.电解时在负极得到氢气
难度: 简单查看答案及解析
-
反应2SO2 + O2
2SO3是工业生产硫酸的关键步骤,下列说法不正确的
A.实际生产中,此反应在接触室进行
B.过量空气能提高SO2的转化率
C.使用催化剂能提高该反应的反应速率
D.2molSO2与1molO2混合一定能生成2molSO3
难度: 简单查看答案及解析
-
一定条件下,向某密闭容器中充入一定量的H2和I2蒸气,发生如下反应:H2(g)+I2(g)
2HI(g),反应达到平衡,下列说法正确的是
A.平衡时,正逆反应速率相等且等于零
B.平衡时,c( H2)=c(I2)=c(HI)
C.平衡时只有H2和I2反应生成HI
D.平衡时,混合气体的所有成分的质量分数均保持不变
难度: 简单查看答案及解析
-
以下实验事实可以证明一水合氨是弱电解质的是
①0.1mol/L的氨水可以使酚酞溶液变红 ②0.1mol/L的氯化铵溶液的pH约为5③0.1mol/L的氨水的pH值为11.2 ④铵盐受热易分解。
A.①② B.②③ C.③④ D.②④
难度: 简单查看答案及解析
-
有(NH4)2SO4、NH4Cl、Na2SO4、NaCl四种溶液,只用一种试剂就能将其鉴别的是
A.BaCl2溶液 B.NaOH溶液 C.AgNO3溶液 D.Ba(OH)2溶液
难度: 简单查看答案及解析
-
下列过程与盐类水解无关的是
A.利用明矾净化浊水
B.铁在潮湿的环境下生锈
C.配制FeCl3溶液时,加少量稀盐酸
D.浓硫化钠溶液有臭味
难度: 简单查看答案及解析
-
下列各组离子中,能大量共存的一组是…………………………………………( )
A.K+、NO3-、Na+、CO32- B.Na+、Cl-、H+、HCO3-
C.Mg2+、Al3+、Cl-、OH- D.Ca+、CO32-、K+、OH-
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A.氢氧化钡溶液与稀硫酸混合:Ba2++SO42-→BaSO4↓
B.Fe与HCl反应:2Fe+6H+→2Fe3++3H2↑
C.碳酸钙跟盐酸反应:CO32-+2H+→CO2↑+H2O
D.醋酸与氢氧化钠溶液反应:CH3COOH+OH-→CH3COO-+H2O
难度: 简单查看答案及解析
-
在CH3COONa溶液中各离子的浓度由大到小排列顺序正确的是
A.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
难度: 简单查看答案及解析
-
下列说法中正确的是
A.NaNO3溶液中:c(Na+)=c(NO3-)
B.在Na2CO3溶液中,c(H+)=c(OH-)
C.在CH3COOH溶液中,c(CH3COOH)=c(H+)
D.K2S溶液中:2c(K+)=c(S2−)
难度: 中等查看答案及解析
-
下列装置所示的实验中,能达到实验目的的是
A.分离碘酒中的碘和酒精
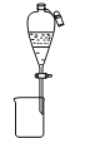
B.配制100mL 0.1mol/L的盐酸

C.排水法收集NO
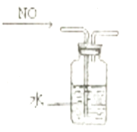
D.氨气吸收
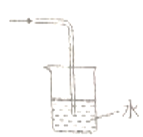
难度: 简单查看答案及解析
-
配制一定物质的量浓度的溶液,下列说法正确的是
A.容量瓶未干燥即用来配置溶液导致配置溶液浓度偏低
B.把4.0gCuSO4溶于250mL蒸馏水中配置250mL0.1mol/LCuSO4溶液
C.转移溶液没有用蒸馏水洗涤烧杯,直接用蒸馏水定容,导致配制溶液浓度偏低
D.称取硫酸铜晶体45g,配置90mL 2mol/L的硫酸铜溶液
难度: 中等查看答案及解析
-
下列有关物质检验的实验结论正确的是
序号
实验操作
现象
实验结论
A
向某溶液中加硝酸酸化的氯化钡溶液
生成白色沉淀
溶液中一定有SO42―
B
将某气体通入紫色石蕊中
溶液变红
该气体一定是CO2
C
将某气体通过无水硫酸铜
固体由白色变蓝色
该气体一定含有水
D
将某气体点燃
产生淡蓝色火焰
该气体一定是H2S
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在下列合成氨事实中N2(g)+3H2(g)=2NH3(g)+Q,不能用勒夏特列原理解释的是
①使用铁做催化剂有利于合成氨的反应
②在高温下反应,更有利于合成氨的反应
③增大体系的压强,可以提高氨的产量
④在合成氨中要不断补充高压N2、H2混合气
A.①③ B.②④ C.①② D.③④
难度: 中等查看答案及解析
-
要使在容积恒定的密闭容器中进行的可逆反应2A(g)+B(s)
2C(g)的反应速率显著加快,可采用的措施是
A.降温 B.加入B C.充入氦气,使压强增大 D.加入A
难度: 简单查看答案及解析
-
实现下列变化需要加入还原剂才能实现的是
A.Fe2O3→Fe
B.NH3→NH4Cl
C.SO3→H2SO4
D.H2SO4→SO3
难度: 简单查看答案及解析
-
在一密闭容器内,充入0.8mol氢气和0.6mol碘蒸气,发生反应H2(g)+I2(g)
2HI(g),反应中各物质浓度随时间变化正确的图像为
A.
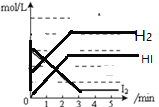 B.
B.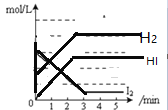
C.
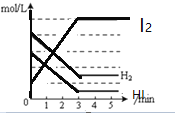 D.
D. 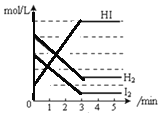
难度: 简单查看答案及解析
-
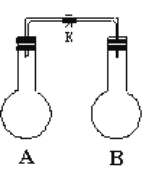
如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强最大的是
编号
①
②
③
④
A中气体
H2S
H2
NH3
NO
B中气体
SO2
Cl2
HCl
O2
A.① B.② C.③ D.④
难度: 中等查看答案及解析