在一密闭容器内,充入0.8mol氢气和0.6mol碘蒸气,发生反应H2(g)+I2(g)2HI(g),反应中各物质浓度随时间变化正确的图像为
A. 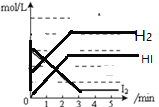 B.
B.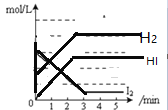
C.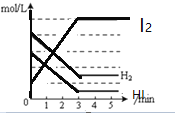 D.
D. 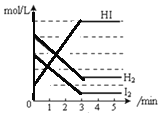
高一化学单选题简单题
在一密闭容器内,充入0.8mol氢气和0.6mol碘蒸气,发生反应H2(g)+I2(g)2HI(g),反应中各物质浓度随时间变化正确的图像为
A.  B.
B.
C. D.
D. 
高一化学单选题简单题
在一密闭容器内,充入0.8mol氢气和0.6mol碘蒸气,发生反应H2(g)+I2(g)2HI(g),反应中各物质浓度随时间变化正确的图像为
A.  B.
B.
C. D.
D. 
高一化学单选题简单题查看答案及解析
在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g) 2HI(g)+9.4 KJ
反应中各物质的浓度随时间变化情况如图1:
(1)在反应趋向平衡状态的过程中,下列说法正确的是_________。
A.HI的生产速率等于分解速率 B.HI的生产速率小于分解速率
C.HI的生产速率大于分解速率 D.无法判断HI的生产速率和分解速率的相对大小
(2)下列说法能说明该反应一定达到平衡的是__________。
A.混合气体的密度不再发生变化 B.混合气体的颜色不再发生变化
C.反应放出的热量恰好为9.4 kJ D.混合气体的压强不再发生变化
(3)根据图1数据,反应开始至达到平衡(第3 min)时,平衡速率v(HI)为____________(用小数表示)。
(4)反应达到平衡后,第8分钟时:
①若升高温度,HI浓度的变化正确的是_________;
②若加入I2,H2浓度的变化正确的是____________。(用图2中相应编号回答)
(5)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。________
高一化学计算题中等难度题查看答案及解析
在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定条件下发生如下反应:H2(g)+I2(g) 2HI(g)ΔH<0,反应中各物质的浓度随时间变化情况如下图甲所示:
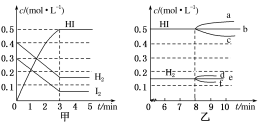
(1)该反应的化学平衡常数表达式为________。
(2)根据图甲数据,反应开始至达到平衡时,平均速率v(HI)为________。
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K________(填“增大”“减小”或“不变”),HI浓度的变化正确的是________(用图乙中a~c的编号回答)。
②若加入I2,H2浓度的变化正确的是________(用图乙中d~f的编号回答)。
高一化学填空题困难题查看答案及解析
(10分)在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+ I2(g) 2HI(g) ΔH<0。反应中各物质的浓度随时间变化情况如图1:
(1)该反应的化学平衡常数表达式为 。
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为 。
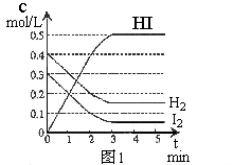
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写增大、减小或不变),HI浓度的变化正确的是 (用图2中a-c的编号回答)。
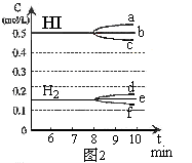
②若加入I2,则H2浓度的变化正确的是 (用图2中d-f的编号回答)。
高一化学填空题中等难度题查看答案及解析
I.一定温度下在2L的密闭容器内发生反应:H2(g)+I2(g)2HI(g),开始时通入0.8molH2和一定量的I2(g),各物质的浓度随时间的变化情况如图所示,其中I2(g)的浓度变化曲线前半部分已略去。

请回答下列问题:
(1)比较正反应速率(同一物质)的大小:A点_____(填“>”“≤”或“=”)B点。
(2)从反应开始至达到平衡,HI的平均反应速率为________。
(3)起始时I2的物质的量为______mol。
II.下图是煤综合利用的一种简单流程。已知烃A对氢气的相对密度是14,C为常见的酸味剂,E是一种有水果香味的透明液体。
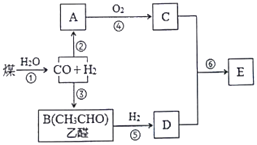
(1)有机物D中含有的官能团的名称是___________。
(2)①~⑥过程中属于加成反应的是_______(填序号)。
(3)写出③的反应方程式____________。
(4)下列说法正确的是____(填字母)。
a.第①步是煤的液化,为煤的综合利用的一种方法
b.有机物C和D都可以与金属钠发生反应
c.有机物C和D的水溶液都具有杀菌消毒作用
d.有机物E与有机物D混合物的分离,可以用氢氧化钠溶液振荡、分液方法
高一化学综合题中等难度题查看答案及解析
698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g)⇌2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间的变化关系如图所示。
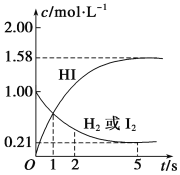
该反应达到平衡状态时,______(填“吸收”或“放出”)的热量为:____kJ。
高一化学计算题中等难度题查看答案及解析
(8分)698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g) = 2HI(g),测得各物质的物质的量浓度与时间变化的关系如图所示。
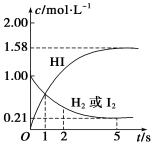
请回答下列问题:
(1)容器的体积V=_____L
(2)反应达到最大限度的时间是_ _s,该时间内平均反应速率v(HI)= mol·L-1·s-1
(3)判断该反应达到平衡的依据是 (填序号)
①(I2)=2
(HI)
②H2、I2、HI的浓度都不变
③容器内气体的压强保持不变
④容器内气体的密度保持不变
高一化学填空题困难题查看答案及解析
密闭容器中的可逆反应H2(g)+I2(g)2HI(g),能说明反映达到平衡状态的是( )
A.容器内压强不再随时间而发生变化
B.单位时间内消耗1molH2,同时生成2molHI
C.氢气、碘蒸气和碘化氢气体的物质的量之比为1:1:2
D.HI的分子数不再发生变化
高一化学选择题中等难度题查看答案及解析
(6分)
将1molH2和1molI2(g)加入2L密闭容器中进行反应:H2 + I2 2HI,反应进行到2min时测得反应速率v(HI)= 0.2mol /(L·min)。求
(1)用氢气的浓度变化来表示2min内的该反应的平均速率?
(2)2min末I2(g)的物质的量浓度?
高一化学计算题简单题查看答案及解析
在密闭容器中进行如下反应:I2(g)+H2(g) 2HI(g),已知I2、H2、HI的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
A.HI为0.4mol/L B.H2为0.15mol/L C.I2为0.2mol/L D.HI为0.35mol/L
高一化学选择题中等难度题查看答案及解析