-
甲、乙两烧杯中各有100mol,3mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
A.5.4g B.3.6 g C.2.7 g D.1.8 g
难度: 中等查看答案及解析
-
化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
选项
现象或事实
解释
A
溶液可用于铜质印刷电路板刻制
Cu从
溶液中置换出铁
B
节日燃放的五彩缤纷的烟花
碱金属以及锶、钡等金属化合物的焰色反应
C
铝箔在酒精灯火焰上加热熔化但不滴落
氧化铝的熔点低于铝的熔点
D
氢氟酸可用于蚀刻玻璃
是碱性氧化物
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列关于合金的说法中正确的是( )
A.改变原料的配比、变更制造合金的工艺,可以制得具有不同性能的合金
B.合金都是由不同金属单质组成的混合物
C.古代留下大量的青铜器文物是由于青铜比纯铜柔软,容易制成各种器皿
D.飞机机身使用的是镁铝合金而不是钢材,是因为钢材价格高
难度: 简单查看答案及解析
-
下列试剂的保存方法错误的是( )
A.实验室少量的钠保存在煤油中
B.新制的氯水保存在棕色玻璃瓶中
C.漂白粉应密封保存
D.Na2CO3溶液保存在带玻璃塞的试剂瓶中
难度: 简单查看答案及解析
-
下列实验操作中有错误的是( )
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.蒸馏装置中,温度计水银球应与蒸馏烧瓶的支管口在同一水平线上
C.用酒精萃取碘水溶液中的碘
D.称量时,称量物放在称量纸上或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘中
难度: 简单查看答案及解析
-
下列有关胶体的说法不正确的是( )
A.Fe(OH)3胶体制好后可以用渗析的方法进一步净化
B.电泳现象可以证明胶体都带电
C.利用丁达尔效应可以区分溶液和胶体
D.由于胶粒之间有排斥作用,胶粒不易聚集成大的颗粒,这是胶体具有介稳性的主要原因
难度: 简单查看答案及解析
-
用下列装置制备Cl2并检验其性质,下列说法正确的是( )
A.I图中:如果MnO2过量,浓盐酸就可全部消耗完

B.II图中:用排饱和食盐水收集一试管氯气,充分光照后,水槽中溶液酸性增强,量筒中液面上升

C.III图中:生成蓝色的烟,若向集气瓶中加入少量水,所得溶液呈黄色
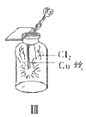
D.IV图中:干燥的有色布条不褪色,湿润的有色布条能褪色,说明Cl2有漂白性

难度: 简单查看答案及解析
-
将标准状况下的aL氯化氢气体溶于100g水中,得到密度为bg·mL-1的盐酸,则该盐酸的物质的量浓度(mol·L-1)是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
设NA表示阿伏伽德罗常数,下列说法正确的是( )
A.16gO2与O3的混合气体中含有的原子数为NA
B.100g46%的乙醇(C2H5OH)溶液共含氢原子数6NA
C.7.8gNa2O2含有的离子数为0.4NA
D.0.1molFe在足量氧气中燃烧,转移电子数为0.3NA
难度: 中等查看答案及解析
-
下列各组关于强电解质、弱电解质、非电解质、混合物的归类,完全正确的是( )
A
B
C
D
强电解质
Fe
NaCl
弱电解质
非电解质
蔗糖
苯
混合物
碱石灰
胆矾
碘酒
液氯
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
向Ba(OH)2溶液中逐滴加入等浓度的稀硫酸,溶液导电性变化合理的图像为( )
A.
 B.
B.
C.
 D.
D.
难度: 简单查看答案及解析
-
同温同压下,等体积的N2O和CO2两种气体相比较:①质量相等;②所含原子数相等;③所含电子数相等;④所含分子数相等;⑤所含氧原子数相等,上述结论中不正确的是( )
A.③⑤ B.②④ C.①③ D.⑤
难度: 简单查看答案及解析
-
下列除去杂质的方法错误的是( )
物质
杂质
试剂
主要操作
A
FeCl2溶液
CuCl2
Fe(足量)
过滤
B
Cl2
HCl
饱和食盐水+浓硫酸
洗气
C
Fe
Fe2O3
稀盐酸(足量)
过滤
D
Na2CO3固体
NaHCO3
无
加热
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列关于钠及其化合物的叙述中正确的是( )
A.钠是一种银白色金属,其硬度很大
B.向酚酞试液中加入适量的Na2O2粉末,振荡后,溶液先变红后褪色
C.可用氢氧化钡溶液鉴别碳酸钠和碳酸氢钠溶液
D.将5gHCHO在氧气中完全燃烧的产物全部通入到足量的过氧化钠固体中,则过氧化钠固体增重2.5g
难度: 简单查看答案及解析
-
下列各组离子,在强酸性溶液中能大量共存的是( )
A.Al3+、Ca2+、HCO3-、SiO32- B.Na+、K+、SO42-、Cl-
C.Mg2+、Fe3+、I-、NO3- D.Cu2+、AlO2-、MnO4-、S2-
难度: 简单查看答案及解析
-
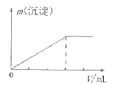
下列实验结果与图像相符的是( )
A.向含有盐酸、氯化镁和氯化铝的溶液中逐滴加入NaOH溶液直至过量

B.向澄清石灰水中通入CO2气体直至过量

C.向NaAlO2溶液中逐滴加入盐酸直至过量

D.向AlCl3溶液中逐滴加入氨水直至过量
难度: 中等查看答案及解析

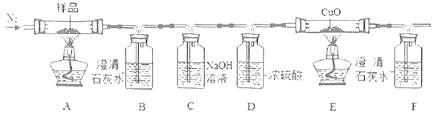
 收集多余的CO,气体应从___端进入(选填“a”或“b”)。
收集多余的CO,气体应从___端进入(选填“a”或“b”)。