-
下列各分子中,所有原子都满足最外层为8电子结构的是( )
A. H2O B. BF3 C. CCl4 D. PCl5
难度: 简单查看答案及解析
-
下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
难度: 中等查看答案及解析
-
测定稀盐酸和氢氧化钠稀溶液中和热的实验中没有使用的仪器有:①大、小烧杯;②容量瓶;③量筒;④环形玻璃搅拌棒;⑤试管;⑥温度计;⑦蒸发皿;⑧托盘天平中的( )
A. ①②⑥⑦ B. ②⑤⑦⑧ C. ②③⑦⑧ D. ③④⑤⑦
难度: 简单查看答案及解析
-
下列叙述中,正确的是( )
A.在多电子的原子里,能量高的电子通常在离核近的区域内活动
B.核外电子总是先排在能量低的电子层上,例如只有排满了L层后才排M层
C.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
D.微粒的最外层只能是8个电子才稳定
难度: 中等查看答案及解析
-
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
A.X、M两种元素只能形成X2M型化合物
B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低
C.元素Y、Z、W的单质晶体属于同种类型的晶体
D.元素W和M的某些单质可作为水处理中的消毒剂
难度: 中等查看答案及解析
-
已知溴跟氢气反应的热化学方程式如下(Q1、Q2、Q3均为正值):H2(g)+Br2(g)→2HBr(l)+Q1,H2(g)+Br2(g)→2HBr(g)+Q2,H2(g)+Br2(l)→2HBr(g)+Q3,下列判断正确的是
A.Q1>Q2>Q3
B.Q1与Q3的大小无法判断
C.溴蒸气转化为液态溴需要放出(Q2-Q3)kJ的热量
D.1LH2和1LBr2蒸气反应生成2LHBr气体时放出Q2kJ热量
难度: 中等查看答案及解析
-
有X、Y两种元素,原子序数小于等于20,X的原子半径小于Y,且X、Y原子最外层电子数相同(m、n均为正整数)。则下列说法正确的是( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为m,则X的最高正价一定为m
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 任何化学反应都伴随着能量的变化
B. H2O(g)═H2O(l)该过程放出大量的热,所以该过程是化学变化
C. 化学反应中能量的变化都表现为热量的变化
D. 对于如图所示的过程,是吸收能量的过程
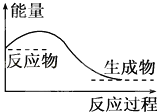
难度: 中等查看答案及解析
-
下列关于
与
两种粒子的叙述中正确的是( )
A.质子数一定相等,质量数和中子数一定不同
B.化学性质几乎相同
C.一定由质子、中子和电子构成
D.核电荷数、核外电子数一定相同
难度: 中等查看答案及解析
-
已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O=O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
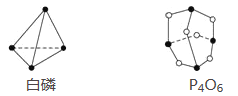
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
难度: 中等查看答案及解析
-
根据碘与氢气反应的热化学方程式
(i)I2(g)+H2(g)
2HI(g)ΔH=-9.48kJ·mol-1
(ii)I2(s)+H2(g)
2HI(g)ΔH=+26.48kJ·mol-1
下列判断正确的是( )
A.254gI2(g)中通入2gH2(g),反应放热9.48kJ
B.1mol固态碘与1mol气态碘所含的能量相差17.00kJ
C.反应(Ⅰ)的产物比反应(Ⅱ)的产物稳定
D.反应(Ⅱ)的反应物总能量比反应(Ⅰ)的反应物总能量低
难度: 中等查看答案及解析
-
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.188 kJ D.436 kJ
难度: 中等查看答案及解析
-
化学反应N2+3H2
2NH3的能量变化如图所示,该反应的热化学方程式是( )
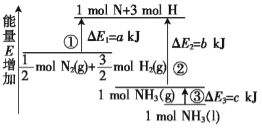
A.N2(g)+3H2(g)
2NH3(l) △H=2(a-b-c)kJ/mol
B.N2(g)+3H2(g)
2NH3(g) △H=2(b-a)kJ/mol
C.N2(g)+H2(g)
NH3(l) △H=(b+c-a)kJ/mol
D.N2(g)+H2(g)
NH3(g) △H=(a+b)kJ/mol
难度: 中等查看答案及解析
