-
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol I2与4 mol H2反应生成的HI分子数为2NA
B.标准状况下,2. 24 L H2O含有的电子数为NA
C.1 L 0.1 mol/L的NH4NO3溶液中含有的氮原子数为0.2NA
D.7.8 g苯中碳碳双键的数目为0.3NA
难度: 中等查看答案及解析
-
X、Y、Z、M、R、Q是短周期主族元素,已知常温下X单质为黄色固体,Y是无机非金属材料的主角,Z焰色反应呈黄色。部分信息如下表:
X
Y
Z
M
R
Q
原子半径/nm
0.104
0.117
0.186
0.074
0.099
0.143
主要化合价
-2
+4,-4
+1
-2
-1,+7
+3
下列说法正确的是:
A.R在元素周期表中的位置是第二周期ⅥA族
B.X、Y均可跟M形成化合物,但它们的成键类型不相同
C.Z、R、Q最高价氧化物的水化物能相互反应
D.Y元素氧化物是用于制造半导体器件、太阳能电池的材料
难度: 中等查看答案及解析
-
下列有关垃圾处理的方法不正确的是
A.废电池必须集中处理的原因是防止电池中汞、镉、铬、铅等重金属元素形成的有毒化合物对土壤和水源污染
B.将垃圾分类回收是垃圾处理的发展方向
C.家庭垃圾中的瓜果皮、菜叶、菜梗等在垃圾分类中属于湿垃圾
D.不可回收垃圾图标是
难度: 简单查看答案及解析
-
关于①②③三种化合物:
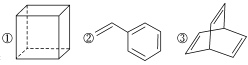 ,下列说法正确的是
,下列说法正确的是A.它们均能使酸性高锰酸钾溶液褪色
B.它们的分子式都是C8H8
C.它们分子中所有原子都一定不共面
D.③的二氯代物有4种
难度: 中等查看答案及解析
-
下列实验操作、现象和结论均正确,且存在对应关系的是
选项
实验操作
实验现象
结论
A
将NaOH溶液逐滴滴加到AlC13溶液中至过量
先产生白色胶状沉淀,后沉淀溶解
Al(OH)3是两性氢氧化物
B
NaHCO3溶液与NaAlO₂溶液混合
生成白色沉淀
结合H+的能力:CO32->AlO2-
C
向盛有Na2SiO3,溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至过量
试管中红色逐渐褪去,出现白色凝胶
非金属性:Cl>Si
D
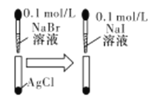
白色固体先变为淡黄色,后变为黄色
溶度积常数:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI)
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
碳钢广泛应用在石油化工设备管道等领域,随着深层石油天然气的开采,石油和天然气中含有的CO2及水引起的腐蚀问题(俗称二氧化碳腐蚀)引起了广泛关注。深井中二氧化碳腐蚀的主要过程如下所示:
负极:Fe(s)+ 2HCO3- (aq) -2e- = FeCO3 (s)+H2CO3(aq)(主要)
正极:2H2CO3(aq) +2e- = H2↑+2HCO3- ( aq)(主要)
下列说法不正确的是
A.钢铁在CO2 水溶液中的腐蚀总反应可表示为CO2+H2O +Fe= FeCO3 +H2
B.深井中二氧化碳对碳钢的腐蚀主要为化学腐蚀
C.碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含量高腐蚀速率会加快
D.腐蚀过程表明含有CO2 的溶液其腐蚀性比相同pH 值的 HCl溶液腐蚀性更强
难度: 中等查看答案及解析
-
25℃时,向20. 00 mL 0.1 mol/L H2X溶液中滴入0.1 mo1/L NaOH溶液,溶液中由水电离出的c水(OH-) 的负对数[一lgc水(OH-)]即pOH水-与所加NaOH溶液体积的关系如图所示。下列说法中正确的是

A.水的电离程度:M>P B.图中P点至Q点对应溶液中
逐渐增大
C.N点和Q点溶液的pH相同 D.P点溶液中
难度: 中等查看答案及解析

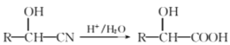 (R为烃基);
(R为烃基);