-
分子式为C5H7Cl的有机物,其结构不可能是( )
A.只含有1个双键的直链有机物 B.含2个双键的直链有机物
C.含1个双键的环状有机物 D.含一个三键的直链有机物
难度: 简单查看答案及解析
-
除去二氧化碳中混有的少量二氧化硫气体,不可选用的试剂是( )
A.饱和碳酸钠溶液 B.高锰酸钾溶液
C.溴水 D.饱和碳酸氢钠溶液
难度: 中等查看答案及解析
-
下列有机物分离提纯方法正确的是
A.除去乙醇中的水:加入少量金属钠 B.除去苯中的溴苯:采用分液法
C.除去乙烯中的甲烷:通入氢氧化钠溶液 D.提纯苯甲酸:利用重结晶法
难度: 中等查看答案及解析
-
化学与生活密切相关。下列说法错误的是( )
A.工业可用二氧化硫漂白纸浆、毛、丝、草帽辫等,也可用于杀菌消毒
B.医用消毒酒精中乙醇的浓度(体积分数)为 95%
C.燃煤中加入 CaO 可以减少酸雨的形成却不能减少温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
难度: 中等查看答案及解析
-
已知①丙烷②正丁烷③异丁烷④2-甲基丁烷⑤己烷,上述物质的沸点按由低到高的顺序排列的是
A.①③②④⑤ B.⑤④③②① C.①②③④⑤ D.⑤①②④③
难度: 简单查看答案及解析
-
以下名称、化学用语均正确的是( )
A.乙醇的分子式:CH3CH2OH
B.顺-1,2-二溴乙烯结构式为:
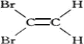
C.甲酸的结构式:
D.醛基的电子式:
难度: 中等查看答案及解析
-
下列现象或事实不能用同一原理解释的是
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硝酸
D.SO2和Na2SO3溶液都能使氯水褪色
难度: 中等查看答案及解析
-
下列关于有机物的说法中,错误的是( )
A.在一定条件下葡萄糖能与新制Cu(OH)2发生反应
B.肥皂的主要成分是油脂在碱性条件下水解生成的
C.淀粉、纤维素和油脂都是天然高分子化合物
D.蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水
难度: 简单查看答案及解析
-
设 NA 为阿伏加德罗常数,下列叙述正确的是( )
A.含1mol乙酸的溶液中H+数等于0.1NA
B.标准状况下,22.4L乙醇的分子数为NA
C.28g乙烯和丙烯所含碳氢键的数目为4NA
D.1 mol甲基所含的电子数为10NA
难度: 中等查看答案及解析
-
我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
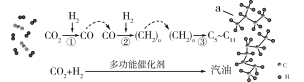
下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C11的烃类混合物
D.图中a的名称是2-甲基丁烷
难度: 中等查看答案及解析
-
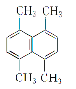
某有机物的结构简式如图所示。下列关于该有机物分子结构的说法中正确的是( )

A.最多有18个原子在同一平面内
B.最多有4个碳原子在一条直线上
C.最多有12个碳原子在同一平面内
D.所有原子都可能在同一平面内
难度: 中等查看答案及解析
-
以下指定化学反应的离子方程式正确的是
A.常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O
B.向氯化铵的稀溶液中加入少量NaOH :NH4++OH- =NH3↑+H2O
C.向(NH4)2SO4溶液中加入适量Ba(OH)2 :Ba2++SO42- =BaSO4↓
D.向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.用银氨溶液检验乙醛中的醛基:CH3CHO + 2Ag(NH3)2+ +2OH-
CH3COONH4 + 3NH3 + 2Ag↓+ H2O
B.苯酚钠溶液中通入少量CO2:CO2+ H2O + 2C6H5O-→ 2C6H5OH + CO32-
C.氯乙烷中滴入AgNO3溶液检验其中氯元素:Cl-+ Ag+ =AgCl↓
D.硫酸铝溶液中加入过量的氨水:Al3+ + 3NH3·H2O=Al(OH)3↓ + 3NH4+
难度: 中等查看答案及解析
-
用下列实验装置进行相应的实验,能够达到实验目的的是( )
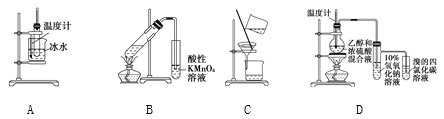
A.实验室制取少量硝基苯 B.证明溴乙烷、NaOH、乙醇溶液共热生成乙烯
C.分离乙酸乙酯、碳酸钠和水的混合物 D.证明乙醇浓硫酸共热生成乙烯
难度: 困难查看答案及解析
-
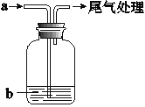
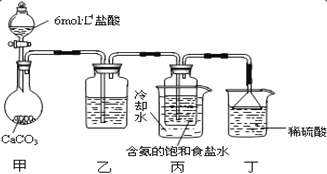
如图装置,将溶液A逐渐加入固体B中,下列叙述中不正确的是( )
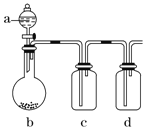
A.若a为浓硫酸,b为Na2SO3固体,c中盛石蕊溶液,则c中溶液先变红后褪色
B.若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液不褪色
C.若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊
D.若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀
难度: 中等查看答案及解析
-
将气体a通入溶液b中,始终无明显变化的是
气体a
溶液b
A
Cl2
NaBr
B
CO2
CaCl2
C
SO2
Ba(NO3)2
D
NO2
FeSO4
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
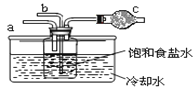
某兴趣小组探究 SO2 气体还原 Fe3+,他们使用的药品和装置如图所示,下列说法不合理的是( )
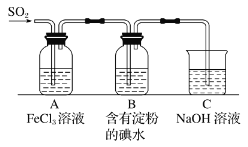
A.为了验证 A 中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
B.为了验证 A 中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
C.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
D.装置C的作用是吸收SO2尾气,防止污染空气
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.乙烯与环丙烷(C3H6)互为同系物
B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色
C.皮肤沾上浓HNO3变成黄色,立即用饱和NaOH溶液冲洗
D.丙酸、乙酸甲酯和2-羟基丙醛(CH3CHOHCHO)互为同分异构体
难度: 中等查看答案及解析
-
一种新的刺激性非致命武器叫臭鼬弹,可用来驱散抗议者。已知臭鼬剂主要成分是丁硫醇(C4H9SH),人的口臭是由于分泌出臭味的甲硫醇(CH3SH),液化气中添加的报警剂是极臭的乙硫醇(CH3CH2SH)。下列说法你认为不正确的是( )。
A.丁硫醇、甲硫醇与乙硫醇互为同系物
B.沸点不同的丁硫醇有四种
C.乙硫醇在空气中燃烧生成二氧化碳、三氧化硫和水
D.乙硫醇中加入K能产生H2
难度: 中等查看答案及解析
-
1.92g 铜投入一定量浓 HNO3 中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL 气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的 O2,恰好使气体完全溶于水中,则通入O2 的体积可能是
A.504mL B.168mL C.336mL D.224mL
难度: 中等查看答案及解析
-
某食用香料乙酸橙花酯的结构简式如图所示,则关于该有机物叙述中正确的个数是( )
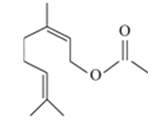
①分子式为C12H20O2
②它的同分异构体中有芳香族化合物
③能使酸性KMnO4溶液褪色
④1mol该有机物在一定条件下能和3mol H2反应
⑤密度比水小
⑥1mol该有机物水解时能消耗1mol NaOH
⑦能在一定条件下生成高分子化合物
A.3个 B.4个 C.5个 D.6个
难度: 中等查看答案及解析


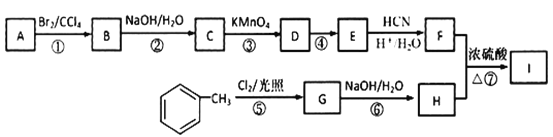
 其中R为烃基。
其中R为烃基。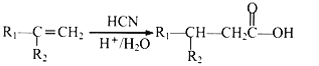 其中R1和R2均为烃基。
其中R1和R2均为烃基。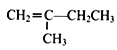 为原料(无机试剂任选),经4步反应制备可降解塑料
为原料(无机试剂任选),经4步反应制备可降解塑料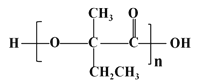 _____________。
_____________。