-
0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当—个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积是
A.5.6L B.6.72L
C.1.344L D.11.2L
难度: 中等查看答案及解析
-
下列溶液肯定呈酸性的是
A.含有H+离子的溶液 B.酚酞显无色的溶液
C.c(OH-)<c(H+)的溶液 D.pH小于7的溶液
难度: 简单查看答案及解析
-
下列过程或现象与盐类水解无关的是( )
A.纯碱溶液去油污 B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深 D.浓硫化钠溶液有臭味
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B.25 ℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7
C.25 ℃时,0.1 mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D.0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中c(Cl-)=c(I-)
难度: 中等查看答案及解析
-
醋酸在水中电离方程式可表示为:
,下列操作能使
浓度增大的是
A.加入少量水 B.加热升温
C.加入锌粉 D.加入固体
难度: 中等查看答案及解析
-
一种充电电池放电时的电极反应为:H2+2OH—
2e—=2H2O、NiO(OH) + H2O +e—=Ni(OH)2+ OH—。当为电池充电时,与外电源正极连接的电极上发生的反应是( )
A.H2O的还原 B.NiO(OH)的还原
C.H2的氧化 D.Ni(OH)2的氧化
难度: 简单查看答案及解析
-
用惰性电极电解下列物质的水溶液时,在阳极上不生成O2的是( )
A.NaOH B.H2SO4 C.ZnCl2 D.Na2SO4
难度: 简单查看答案及解析
-
将等物质的量的A、B混合于2L的恒容密闭容器中,发生如下的反应:3A(g )+B(g)
xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率为0.1mol/(L﹒min)。则x的值为( )
A.4 B.3 C.2 D.1
难度: 简单查看答案及解析
-
常温下,将足量的AgCl固体分别放入下列液体中,AgCl的溶解度由大到小排列的顺序正确的是
①20 mL蒸馏水
②30 mL 0.03 mol/L HCl溶液
③40 mL 0.05 mol/L AgNO3溶液
④50 mL 0.02 mol/L CaCl2溶液
A. ②>④>③>① B. ①>②>④>③ C. ①>②>③>④ D. ③>②>④>①
难度: 中等查看答案及解析
-
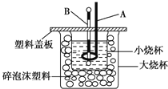
某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—
Cl2↑+H2↑
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D.断开K1,闭合K2时,石墨电极作正极
难度: 中等查看答案及解析
-
一种充电电池放电时的电极反应为:H2+2OH—
2e—=2H2O、NiO(OH) + H2O +e—=Ni(OH)2+ OH—。当为电池充电时,与外电源正极连接的电极上发生的反应是( )
A.H2O的还原 B.NiO(OH)的还原
C.H2的氧化 D.Ni(OH)2的氧化
难度: 简单查看答案及解析
-
反应C(s)+H2O(g)
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积增大
A. ①② B. ①③ C. ②③ D. ③④
难度: 中等查看答案及解析
-
下图中烧杯里盛的是海水,铁被腐蚀由快到慢的顺序是( )
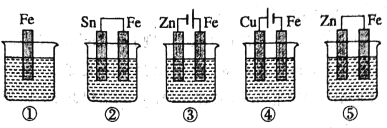
A.③>②>①>⑤>④ B.④>②>①>③>⑤ C.③>②>④>⑤>① D.④>⑤>②>③>①
难度: 简单查看答案及解析
-
下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成; 乙烯与水生成乙醇的反应
D.在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反应
难度: 简单查看答案及解析
-
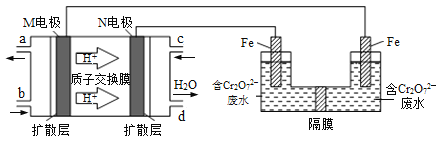
下图为某二次电池充电时的工作原理示意图,该过程可实现盐溶液的淡化。下列说法错误的是( )

A.充电时,a 为电源正极
B.充电时,
向Bi 电极移动,
向
电极移动
C.放电时,正极的电极反应为
D.充电时,新增入电极中的物质:
:
:3
难度: 中等查看答案及解析
-
室温下,下列说法正确的是
A.将
的盐酸和
的硫酸等体积混合,所得溶液
B.HF比HCN易电离,则NaF溶液的pH比同浓度NaCN溶液的pH大
C.向
氨水中加入少量硫酸铵固体,溶液中
增大
D.将1 mL
的HA溶液稀释到10 mL,若溶液的
,则HA为弱酸
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.25℃,Cu(OH) 2 在水中的溶度积常数比其在 Cu(NO3) 2 溶液中的大
B.一定温度下,将 0.10 mol/L的氨水加水稀释,溶液中各离子浓度均减小
C.用0.1mol/L的盐酸滴定0.1mol/L的氨水时,可用酚酞作指示剂
D.常温下,NaHS 溶液中:c(H+)+c(H2S)=c(S2-)+c(OH-)
难度: 中等查看答案及解析
-
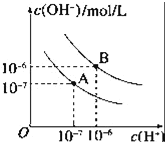
室温时,在由水电离出c(OH﹣)=1.0×10-12mol/L的溶液中,一定能大量共存的离子组是( )
A.K+、Na+、HCO3-、Cl- B.K+、MnO4-、Br-、Cl-
C.Na+、Cl-、NO3-、SO42- D.Al3+、NH4+、Cl-、SO42-
难度: 中等查看答案及解析
-
把A、B、C、D四块金属片浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;A、C相连时,C极上产生大量气泡,B、D相连时,D极发生氧化反应。这四种金属的活动性顺序是
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
难度: 中等查看答案及解析
-
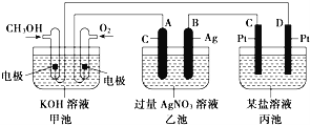
如图所示,甲池的总反应式为:
,下列关于该电池工作时的说法正确的是
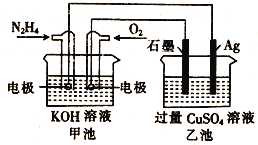
A.该装置工作时,Ag电极上有气体生成
B.甲池中负极反应为
C.甲池和乙池中的溶液的pH均减小
D.当甲池中消耗
时,乙池中理论上最多产生
固体
难度: 中等查看答案及解析