-
用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
A. 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液
B. 碱式滴定管尖端有气泡,滴定后气泡消失
C. 记录消耗的碱液,滴定前平视,滴定后俯视凹液面
D. 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸
难度: 中等查看答案及解析
-
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速度加大的是( )
A.加热
B.不能稀硫酸而用浓硫酸
C.往溶液中加入少量CuSO4固体
D.不能铁片而用铁粉
难度: 简单查看答案及解析
-
下列反应中,属于吸热反应的是
A. 乙醇燃烧 B. 碳酸钙受热分解
C. 氧化钙溶于水 D. 盐酸和氢氧化钠反应
难度: 简单查看答案及解析
-
在不同条件下分别测得反应2SO2+O2
2SO3的化学反应速率,其中表示该反应进行得最快的是( )
A.v(SO2)=4mol/(L·min) B.v(O2)=3mol/(L·min)
C.v(SO2)=0.1mol/(L·s) D.v(O2)=0.1mol/(L·s)
难度: 简单查看答案及解析
-
在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应A(s)+2B(g)
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.混合气体的相对分子质量 D.C的物质的量
难度: 简单查看答案及解析
-
下列事实不能用勒夏特列原理解释的是( )
A.用排饱和食盐水的方法收集氯气
B.钢铁在潮湿的空气中比在干燥的空气中容易生锈
C.温度过高对合成氨不利
D.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
难度: 简单查看答案及解析
-
一定条件下,将NO(g)和O2(g)按物质的量之比2∶1充入反应容器,发生反应:2NO(g) + O2(g)
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如下图所示。下列说法正确的是
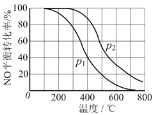
A. p1 < p2
B. 其他条件不变,温度升高,该反应的反应限度增大
C. 400℃、p1条件下,O2的平衡转化率为20%
D. 400℃时,该反应的化学平衡常数的数值为10/9
难度: 中等查看答案及解析
-
下列溶液一定呈碱性的是( )
A.pH=8的溶液 B.含有OH-离子的溶液
C.c(OH-)>c(H+)的溶液 D.NaCl溶液
难度: 简单查看答案及解析
-
25℃时,下列溶液中水的电离程度最小的是( )
A.pH=11的氨水 B.0.01mol/L的Ba(OH)2溶液
C.0.01mol/L的盐酸 D.pH=4的硫酸溶液
难度: 简单查看答案及解析
-
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数(25℃),若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2、NaCN+HF=HCN+NaF、NaNO2+HF=HNO2+NaF。由此可判断下列叙述中不正确的是( )
A.K(HF)=7.2×10-4
B.K(HNO2)=4.9×10-10
C.根据两个反应即可得出一元弱酸的强弱顺序为HF>HNO2>HCN
D.K(HCN)<K(HNO2)<K(HF)
难度: 简单查看答案及解析
-
某同学用0.1 mol/L 的盐酸滴定20.00 mL NaOH溶液,测定其浓度。下列操作正确的是
A. 需用NaOH溶液润洗锥形瓶
B. 用量筒量取20.00 mL NaOH溶液
C. 滴定前,使酸式滴定管尖嘴部分充满盐酸
D. 充分反应后,滴入酚酞溶液,观察是否到达滴定终点
难度: 简单查看答案及解析
-
常温下,某无色溶液中由水电离出来的c(H+)=1×10-12 mol·L-1,该溶液中一定能大量存在的离子组是
A.Na+、K+、MnO4-、SO42-
B.Mg2+、NH4+、SO42-、Cl-
C.Na+、Cl-、NO3-、SO42-
D.Na+、K+、CO32-、NO3-
难度: 中等查看答案及解析
-
如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )

A.两条曲线间任意点均有c(H+)·c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.XZ线上任意点均有pH=7
D.图中T1<T2
难度: 简单查看答案及解析
-
某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断错误的是( )
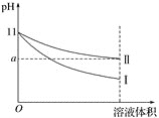
A. a值一定大于9
B. Ⅰ为NaOH溶液稀释时溶液的pH变化曲线
C. 完全中和稀释相同倍数后的两溶液,消耗相同浓度的稀H2SO4的体积V(NaOH)<V(氨水)
D. 稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
难度: 中等查看答案及解析
-
25℃时,关于下列溶液混合后溶液pH的说法中正确的是( )
A.pH=10与pH=12的NaOH溶液等体积混合,溶液的pH约为11
B.pH=5的盐酸溶液稀释1000倍,溶液的pH=8
C.pH=2的H2SO4与pH=12的NaOH溶液等体积混合,混合液pH=7
D.pH=12的NH3·H2O与pH=2的HCl溶液等体积混合,混合液pH=7
难度: 简单查看答案及解析
-
已知100℃时,0.01mol·L-1NaHSO4溶液中水电离的c(H+)=10-10mol·L-1,该温度下将pH=8的Ba(OH)2溶液V1L与pH=5的NaHSO4溶液V2L混合,所得溶液pH=7,则V1:V2为( )
A.2:9 B.9:2 C.1:9 D.1:2
难度: 简单查看答案及解析
-
已知反应2NO + 2H2 === N2 + 2H2O的速率方程为υ= kc2(NO)· c(H2)(k为速率常数),其反应历程如下:
① 2NO + H2 → N2+H2O2 慢
② H2O2 + H2 → 2H2O 快
下列说法不正确的是
A. 增大c (NO) 或c(H2),均可提高总反应的反应速率
B. c (NO) 、c(H2)增大相同的倍数,对总反应的反应速率的影响程度相同
C. 该反应的快慢主要取决于反应①
D. 升高温度,可提高反应①、②的速率
难度: 中等查看答案及解析
-
K2FeO4在水中不稳定,发生反应:4FeO42-+10H2O
4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如图所示。下列说法不正确的是
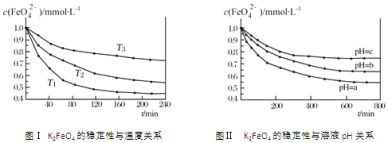
A. 由图Ⅰ可知K2FeO4的稳定性随温度的升高而减弱
B. 由图Ⅱ可知图中a>c
C. 由图Ⅰ可知温度:T1>T2>T3
D. 由图Ⅰ可知上述反应△H>0
难度: 中等查看答案及解析
-
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对
化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
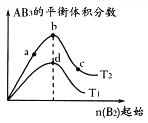
A.若
>
,达到平衡时b、d点的反应速率为
>
B.若
>
,则正反应一定是放热反应
C.达到平衡时
的转化率大小为:b>a>c
D.在
和
不变时达到平衡,
的物质的量大小为:c>b>a
难度: 中等查看答案及解析
-
中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如下图所示。

已知:几种物质中化学键的键能如下表所示。
化学键
H2O中H—O键
O2中O=O 键
H2中H—H键
H2O2中O—O键
H2O2中O—H键
键能kJ/mol
463
496
436
138
463
若反应过程中分解了2 mol水,则下列说法不正确的是
A. 总反应为2H2O
2H2↑+O2↑
B. 过程I吸收了926 kJ能量
C. 过程II放出了574 kJ能量
D. 过程Ⅲ属于放热反应
难度: 中等查看答案及解析