-
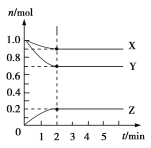
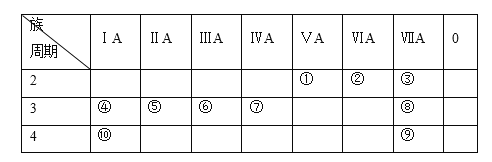
在元素周期表中,第一、二、三、四周期元素的种类分别是( )
A. 2、8、8、18 B. 2、8、18、18
C. 2、18、18、18 D. 2、8、18、32
难度: 简单查看答案及解析
-
下列变化属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变成白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A.①②④ B.②③ C.①④⑤ D.②④
难度: 简单查看答案及解析
-
下列关于元素周期表的说法,错误的是
A.元素周期表是元素按原子序数大小排列而成的
B.元素原子的电子层数等于其所在周期的周期序数
C.元素原子的最外层电子数等于其所在族的族序数
D.元素周期表是元素周期律的具体表现形式
难度: 中等查看答案及解析
-
在元素周期表中,从左到右共有18个纵行。第1纵行(除氢以外)为碱金属元素,稀有气体元素是第18纵行。下列说法正确的是( )
A.铝元素位于第3纵行
B.过渡元素在周期表中占10个纵行
C.第18纵行所有元素的最外层均有8个电子
D.第16纵行元素都是非金属元素
难度: 简单查看答案及解析
-
依据门捷列夫的元素周期表,人们总结出下面的元素化学性质的变化规律。该表中元素化学性质的变化表明( )
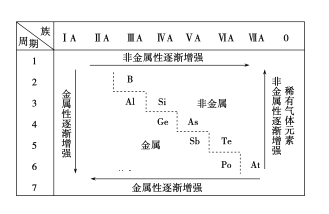
A.同周期元素的性质是相似的
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.第ⅠA族元素的金属性肯定比同周期的第ⅡA族元素的金属性弱
D.物质量变到一定程度必然引起质变
难度: 简单查看答案及解析
-
下列化学用语的书写,正确的是
A.氯原子的结构示意图:
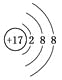
B.6个质子8个中子的碳元素的核素符号:12C
C.氯化镁的电子式:
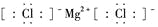
D.用电子式表示氯化氢的形成过程:
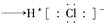
难度: 困难查看答案及解析
-
已知:

下列说法不正确的是
A.①和②变化过程中都会放出热量
B.氯原子吸引电子的能力强于钠原子和氢原子
C.①和②中的氯原子均得到1个电子达到8电子稳定结构
D.NaCl中含有离子键,HCl中含有共价键
难度: 中等查看答案及解析
-
下列各组物质中化学键的类型完全相同的是( )
A.NaCl MgCl2 Na2O
B.H2O Na2O CO2
C.CaCl2 NaOH H2SO4
D.NH4Cl H2O CO2
难度: 中等查看答案及解析
-
下列设备工作时,将化学能转化为热能的是( )
A
B
C
D




硅太阳能电池
锂离子电池
太阳能集热器
燃气灶
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列说法正确的是
A.反应条件是加热的反应都是吸热反应
B.化学反应除了生成新的物质外,还伴随着能量的变化
C.物质燃烧不一定是放热反应
D.放热的化学反应不需要加热就能发生
难度: 简单查看答案及解析
-
对于反应H2(g)+Cl2(g)=2HCl(g)的能量变化描述正确的是
A.成键过程中吸收能量
B.断键过程中吸收能量,成键过程中释放能量
C.断键过程中释放能量
D.断键过程中释放能量,成键过程中吸收能量
难度: 中等查看答案及解析
-
铜~锌原电池如图所示,电解质溶液为稀硫酸,下列说法不正确的是
A.铜电极上发生还原反应
B.锌电极是原电池的负极
C.电子从铜极经过外电路流向锌极
D.锌电极上的反应为Zn-2e— ="=" Zn2+
难度: 中等查看答案及解析
-
实验室用3.0 mol·L-1的硫酸溶液与锌粒反应制取氢气。下列措施中可能加大反应速率的是
A.适当降低温度 B.将锌粒改为锌粉
C.将所用硫酸换成98%的浓硫酸 D.加入少量醋酸钠固体
难度: 中等查看答案及解析
-
SO2的催化氧化反应(2SO2+O2
2SO3)是一个放热的反应。如果反应在密闭容器中进行,下列有关说法中正确的是
A.因为反应放热,所以升高温度会使反应速率减慢
B.通过调控反应条件,SO2可以100%地转化为SO3
C.当SO2与SO3的浓度相等时,反应达到平衡
D.使用催化剂的目的是加快反应速率,提高生产效率
难度: 中等查看答案及解析
-
对于a、b、c、d四块金属片,若a、b用导线相连浸泡在稀H2SO4中,电子由a流向b;c、d用导线相连浸泡在稀H2SO4时,d产生大量气泡;a、c用导线相连浸泡在稀CuSO4中时,c上附着上一层红色物质;d浸泡在b的硝酸盐溶液中,置换出b的单质。由这四种金属的活动顺序由大到小为( )
A.a>b>c>d B.a>c>d>b
C.c>a>b>d D.b>d>c>a
难度: 中等查看答案及解析