-
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项
实验
现象
结论
A
用硫酸酸化的H2O2溶液滴入到Fe(NO3)2溶液中,
溶液变成黄色
氧化性: H2O2强于Fe3+
B
蘸有浓氨水的玻璃棒靠近某溶液
有白烟产生
该溶液可能是浓盐酸
C
用铂丝蘸取少量某溶液进行焰色反应
火焰呈黄色
该溶液含钠元素不含钾元素
D
分别向含有酚酞的烧碱溶液中通入氯气、二氧化硫
溶液颜色都变浅
说明氯气和二氧化硫都有漂白性
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列对浓硫酸的叙述正确的是( )
A.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
B.浓硫酸具有强氧化性,SO2、H2、CO具有还原性,故浓硫酸不能干燥SO2、H2、CO
C.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
D.浓硫酸与亚硫酸钠反应制取SO2时,浓硫酸表现出强氧化性
难度: 中等查看答案及解析
-
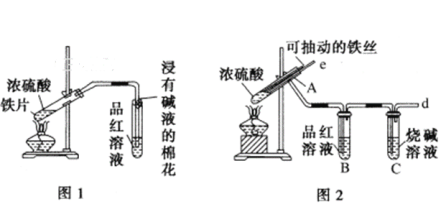
香烟烟雾中含有CO、CO2、SO2、H2O等气体,用①无水CuSO4 ②澄清石灰水③红热CuO ④生石灰 ⑤品红溶液 ⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时香烟烟雾通入药品的正确顺序是
A.①⑤②①④③
B.①⑤⑥②④③
C.③④②⑥⑤①
D.②⑤①④③⑥
难度: 中等查看答案及解析
-
检验 SO2 气体中是否混有 CO2 气体,可采用的方法是( )
A.通过品红溶液
B.通过澄清石灰水
C.先通过足量酸性 KMnO4 溶液,再通过澄清石灰水
D.先通过 NaOH 溶液,再通过澄清石灰水
难度: 中等查看答案及解析
-
为检验一种氮肥的成分,某学习小组的同学进行了以下实验:①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分是
A. NH4HCO3 B. NH4Cl C. (NH4)2CO3 D. NH4NO3
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的的是
选项
实验目的
实验操作
A
配制100mL 0.1mol·L-1 H2SO4溶液
用量筒量取20mL0.5000 mol·L-1 H2SO4溶液于烧杯杯中,加水80mL
B
除去Cl2中混有的少量HCl
将Cl2与HC1混合气体通过饱和NaHCO3溶液
C
除去KNO3固体中混杂的少量NaCl
将混合物固体制成热的饱和溶液,冷却结晶,过滤
D
验证稀硝酸能将Fe氧化为Fe3+
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某化学兴趣小组欲利用MnO2和浓盐酸及如图所示装置制备Cl2。下列分析中不正确的是
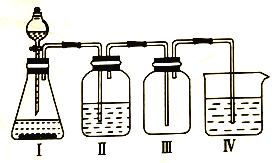
A.I中缺少加热装置
B.Ⅱ为净化Cl2的装置,其盛放的是NaOH溶液
C.Ⅲ为收集Cl2的装置
D.Ⅳ中处理多余的Cl2时,Cl2既作氧化剂,又作还原剂
难度: 简单查看答案及解析
-
化学与人类生产、生活、社会可持续发展密切相关,下列有关说法不正确的是
A. 高纯硅广泛应用于太阳能电池、计算机芯片,是一种重要的半导体材料
B. 氟利昂和NOx都能破坏臭氧层,从而导致“温室效应”
C. 中国是目前全球最大的稀土生产国和出口国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径
D. 华为发布的首款5G折叠屏手机,用镁铝合金制成的手机外壳具有轻便抗压的特点
难度: 简单查看答案及解析
-
某溶液中含有SO42-、SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是
①反应前后,溶液中离子浓度基本保持不变的有SO42-、Na+;②有胶状物质生成;③有气体产生;④溶液颜色发生变化; ⑤共发生了2个氧化还原反应。
A. ②③④ B. ①②③ C. ①③⑤ D. ②④⑤
难度: 困难查看答案及解析
-
化学与环境密切相关,下列有关说法不正确的是
A.酸雨是pH小于7的雨水
B.SO2、NO2都会导致酸雨的形成
C.目前工业废气脱硫应用最广泛的方法是石灰法
D.我国重点城市近年发布“空气质量日报”列入的首要污染物包括SO2、NO2、可吸入颗粒物
难度: 中等查看答案及解析
-
在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )
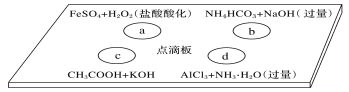
A. a反应:Fe2++2H++H2O2===Fe3++2H2O B. b反应:HCO3-+OH-===CO32-+H2O
C. c反应:H++OH-===H2O D. d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH4+
难度: 中等查看答案及解析
-
下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
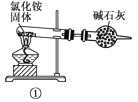
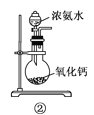
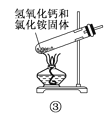
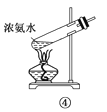
A. ①③ B. ②③
C. ①④ D. ②④
难度: 中等查看答案及解析
-
按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述不正确的是( )
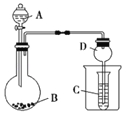
A.若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色
B.若A为醋酸,B为贝壳,C中盛Na2SiO3,则C中溶液中变浑浊
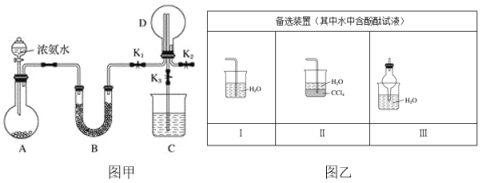
C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生沉淀后沉淀又溶解
D.实验仪器D可以起到防止溶液倒吸的作用
难度: 中等查看答案及解析
-
纯二氧化硅可用下列流程制得。下列说法不正确的是( )

A.X可用作木材防火剂
B.步骤Ⅱ的反应是Na2SiO3+H2SO4═H2SiO3↓+Na2SO4
C.步骤Ⅱ中的稀硫酸可用CO2来代替
D.步骤Ⅲ若在实验室完成,一般在蒸发皿中进行
难度: 中等查看答案及解析
-
二氧化硅是一种化工原料,可以制备一系列物质。下列说法正确的是( )
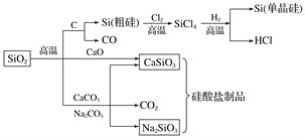
A.图中所有反应都不属于氧化还原反应
B.硅酸盐的化学性质稳定,常用于制造光导纤维
C.可用盐酸除去石英砂(主要成分为SiO2)中少量的碳酸钙
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
难度: 中等查看答案及解析
-
中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是
A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
难度: 简单查看答案及解析