-
放射性物质铱—192可使人的红细胞、白细胞、血小板严重偏低。则19277Ir中的中子数和质子数之差为( )
A. 115 B. 38 C. 269 D. 15
难度: 简单查看答案及解析
-
根据元素周期表判断下列描述正确的是( )
A. 元素周期表中,总共有16个纵行,16个族
B. 第IA族的元素又称为碱金属元素,第VIIA族的元素又称为卤族元素
C. 每个短周期都既包含金属元素也包含非金属元素
D. 在金属和非金属元素分界线附近可以寻找制作半导体材料的元素
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y原子的最外层有2个电子,Z的单质晶体是应用最广泛的半导体材料,W与X位于同一主族。下列说法正确的是
A.原子半径:r(W)> r(Z)> r(Y)> r(X)
B.由X、Y组成的化合物是离子化合物
C.Z的最高价氧化物对应水化物的酸性比W的强
D.W的简单气态氢化物的热稳定性比X的强
难度: 简单查看答案及解析
-
下列关于物质性质变化的比较,不正确的是( )
A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH D.金属性强弱:Na>Mg>Al
难度: 中等查看答案及解析
-
下列各组物质中化学键的类型相同的是( )
A.HCl、MgCl2、NH4Cl B.NH3、H2O、CO2
C.CO、Na2O、CS2 D.CaCl2、NaOH、N2O
难度: 简单查看答案及解析
-
下列有关化学用语表达正确的是
A. 35Cl−和37Cl−离子结构示意图均可以表示为:
B. HClO的结构式:H−Cl−O
C. HF的电子式:
D. 质子数为92、中子数为146的U原子:
难度: 简单查看答案及解析
-
①、②、③三种原子的原子结构可用如图来形象表示:
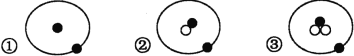
其中
表示质子或电子,
表示中子,下列有关叙述错误的是( )
A.①、②、③互为同位素
B.①、②、③属于同种元素
C.①、②、③的质量数相同
D.①、②、③形成的单质具有还原性
难度: 简单查看答案及解析
-
下列物质中,属于共价化合物的是( )
A.I2 B.NH4Cl C.NaCl D.HNO3
难度: 简单查看答案及解析
-
U是重要的工业原料,铀浓缩一直为国际社会关注。下列有关
U的说法正确的是( )
A.
U原子核中含有2个中子 B.
U原子核外有143个电子
C.
U与
U为同一核素 D.
U与
U互为同位素
难度: 简单查看答案及解析
-
X + 的核外电子排布为 2、8、8,则X位于周期表的位置是( )
A. 第四周期第 IA 族 B. 第三周期第 0 族
C. 第三周期第 IA 族 D. 第三周期第 VIIA 族
难度: 简单查看答案及解析
-
23Na与23Na+比较,相同的是
A.微粒半径 B.化学性质 C.最外层电子数 D.中子数
难度: 简单查看答案及解析
-
2016年11月30日,国际纯粹与应用化学联合会(IUPAC)公布了118号元素符号为Og,至此元素周期表的七个周期均已填满。下列关于
的说法错误的是
A.原子序数为118 B.中子数为179
C.核外电子数为118 D.Og的相对原子质量为297
难度: 简单查看答案及解析
-
Ne是最早发现的Ne元素的稳定同位素,汤姆逊(J.J.Thomson)和阿斯通(F.W.Aston)在1913年发现了
Ne。下列有关说法正确的是( )
A.
Ne和
Ne是同分异构体 B.
Ne和
Ne属于不同的核素
C.
Ne和
Ne的性质完全相同 D.
Ne转变为
Ne为化学变化
难度: 简单查看答案及解析
-
下列各表为周期表的一部分(表中数字为原子序数),其中正确的是( )
A.
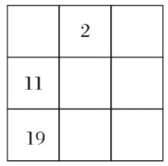 B.
B.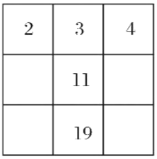
C.
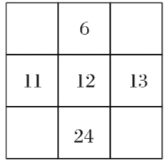 D.
D.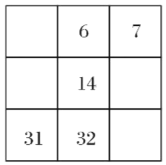
难度: 简单查看答案及解析
-
短周期元素
、
、
在周期表中的位置如图所示。已知
、
两元素的原子序数之和是
元素的4倍,则
、
、
分别是( )
A.
、
、
B.
、
、
C.
、
、
D.
、
、
难度: 中等查看答案及解析
-
稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法错误的是
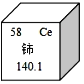
A.铈的原子序数是58 B.铈属于非金属元素
C.铈原子中的质子数是58 D.铈的相对原子质量是140.1
难度: 简单查看答案及解析
-
下列下列说法正确的是
A.F-、Cl-、Br-、I-的还原性逐渐增强
B.HF、HC1、HBr、HI的沸点逐渐升高
C.K可以从NaCl溶液中置换出金属
D.碱金属单质在空气中燃烧生成的都是过氧化物
难度: 简单查看答案及解析
-
下列叙述错误的是( )
A. 13C和14C属于同一种元素,它们互为同位素
B. 6Li和7Li的电子数相等,中子数也相等
C. 14C和14N的质量数相等,中子数不相等
D. 1mol
U的中子数比1mol
U的中子数少3NA个
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 在共价化合物中一定含有共价键
B. 含有离子键的化合物一定是离子化合物
C. 含有共价键的化合物一定是共价化合物
D. 化学反应过程中,反应物分子内的化学键断裂,产物分子的化学键形成
难度: 中等查看答案及解析
-
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
A. 气态氢化物的稳定性:HX>H2Y>ZH3 B. 非金属性:Y<X<Z
C. 原子半径:X>Y>Z D. 原子序数:Z>Y>X
难度: 中等查看答案及解析
-
下列各分子中,化学键类型不同的是
A.H2O、CO B.MgF2、H2O C.KOH、Mg(OH)2 D.HCl、HBr
难度: 简单查看答案及解析
-
在元素周期表中,分别与周期数、主族序数相同的一组是()
①质子数 ②核电荷数 ③电子层数 ④原子序数 ⑤最外层电子数
A.③⑤ B.②③ C.③④ D.①⑤
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.共价化合物和离子化合物中,一定都含有非金属元素
B.阴阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距相当小
C.失电子难的原子获得电子的能力一定强
D.含有共价键的化合物必是共价化合物
难度: 中等查看答案及解析
-
下列叙述中错误的是( )。
A.带相反电荷离子之间的相互吸引力称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间也可能形成离子键
难度: 简单查看答案及解析
-
下列有关氢化物的叙述中正确的( )
A.稳定性:H2S>HF B.HCl的电子式为
C.一个D2O分子所含的中子数为8 D.在卤化氢中HF最稳定
难度: 简单查看答案及解析
-
下列各组物质中所含化学键类型相同的是
A.NaF、NH4Cl B.NaOH、NaClO C.CaO、Na2O2 D.MgCl2、Mg(OH)2
难度: 中等查看答案及解析
-
下列表示正确的是( )
A.核素14C的质子数为14
B.氯原子的结构示意图:
C.H、D、T互为同位素
D.氨水的电离方程式:NH3·H2O
NH4++OH-
难度: 简单查看答案及解析
-
五种短周期主族元素A、B、C、D、E的原子序数依次增大,A2属于绿色燃料,C的氧化物用于生产光导纤维,D元素原子的核电荷数是同主族上一周期元素的2倍,B、C为同周期元素,B、D原子最外层电子数之和等于E的最外层电子数. 根据以上叙述,下列说法中正确的是
A.五种元素中有两种金属元素
B.元素C、D、E的最高价氧化物对应水化物的酸性增强
C.元素D、E分别与元素A形成化合物的稳定性:A2D>AE
D.元素B、D、E的简单离子半径大小为:B>D>E
难度: 中等查看答案及解析
-
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
A.X、Y、Z、W的原子半径依次减小
B.W与X元素的单质在常温下不反应
C.W的气态氢化物的沸点一定低于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素同周期,X的金属性在同周期元素中最强;Y原子的电子层数与最外层电子数相等;Z元素在地壳中的含量居于第二位;W的最高价氧化物的水化物的化学式为HnWO2n+2。下列说法正确的是( )
A.简单离子半径:X<Y<W
B.Y、Z两种元素的氧化物均具有两性
C.X、W分别形成的氢化物中所含化学键种类相同
D.Z、W形成化合物的电子式为:

难度: 中等查看答案及解析