-
某研究性学习小组,为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于下图,根据图中数据,下列推论最不合理的是
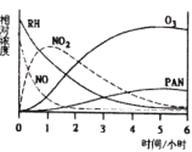
A.NO的消失的速率比RH快
B.NO转化为NO2
C.RH和NO2转化为PAN和O3
D.O3转化为PAN
难度: 中等查看答案及解析
-
下列叙述中正确的是 ( )
A.Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6×6.02×1023
B.常温常压下,8.8g CO2和N2O混合物中所含有的原子总数为0.6×6.02×1023
C.标准状况下,3.36L溴乙烷中含有的溴离子数目为0.15×6.02×1023
D.在1L 0.2mol/L的硫酸铁溶液中含有的三价铁离子数为0.4×6.02×1023
难度: 中等查看答案及解析
-
锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe
Sb4O6+6FeS,
②Sb4O6+6C
4Sb+6CO↑。关于反应①、②的说法正确的是
A.反应①、②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3molFeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1
难度: 中等查看答案及解析
-
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是( )
A.Na2SiO3 B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2 D.SiO2
难度: 简单查看答案及解析
-
化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中正确的是( )
A.K37C1O3与浓盐酸(HC1)在加热条件时生成氯气的化学方程式:K37C1O3+6HC1=K37C1+3C12↑+3H2O
B.表示氢气燃烧热的热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H=-241.8kJ/mol
C.将1mL—2mL氯化铁饱和溶液滴加到20mL沸水中所发生反应的离子方程式: Fe3++3H2O
Fe(OH)3(胶体)+3H+
D.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH—=NH3↑+H2O
难度: 中等查看答案及解析
-
如图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是 ( )
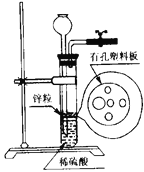
①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤ B.①②⑥ C.①②⑤ D.①②④
难度: 中等查看答案及解析
-
下列关于“最多”“最少”的说法中不正确的是( )。
A.在盐酸与氢氧化钠溶液的中和热测定的实验过程中,最少需要测定并记录温度的次数是3次
B.在硫酸铜晶体中结晶水含量测定的实验中,在实验过程中最少称量4次
C.在某有机物分子中含n个—CH2—,m个
,a个—CH3,其余为羟基,则含羟基的个数最多为m - a + 2
D.在有机物
分子中处于同一平面内的碳原子数最多有13个
难度: 困难查看答案及解析
-
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则溶液中MgCl2与Al2(SO4)3的物质的量浓度之比为( )
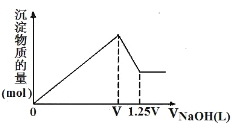
A.1:1 B.1:2
C.3:2 D.2:1
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A.石油经蒸馏分离成为汽油、煤油和柴油等产品是利用物质的沸点不同的原理
B.硝酸钾和氯化钾浓溶液降温结晶得到硝酸钾晶体是利用它们的溶解度随温度变化而不同的原理
C.为迅速除去乙酸乙酯中的乙酸,加入足量的NaOH并加热
D.沙里淘金是利用了物质的密度不同,从而达到提取黄金的目的
难度: 简单查看答案及解析
-
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是
A.S2Cl2的结构式为Cl—S—S—Cl
B.S2Cl2为含有极性键和非极性键的极性分子
C.S2Br2与S2Cl2结构相似,熔沸点S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
难度: 中等查看答案及解析
-
若阿伏加德罗常数为NA,下列说法正确的是( )
A.在60gSiO2中,含Si—O键的数目是2NA
B.32gN2H62+和C2H6的混合物中,共含有电子数为18NA
C.标准状况下,22.4L NO与11.2L O2混合物容器中共有NA个NO2分子
D.1L 0.1mol/L Na2SO4溶液中,含有的离子数不是3NA
难度: 困难查看答案及解析
-
下列离子方程式正确的是( )
A.将少量SO2气体通入NaClO溶液中:SO2+2ClO—+H2O=SO32—+2HClO
B.惰性电极电解氯化镁溶液:2Cl—+2H2O
Cl2↑+H2↑+2OH—
C.氯化铝溶液中滴加足量氨水:Al3++4OH—=AlO2—+2H2O
D.在氟化银溶液中滴入盐酸:Ag++F —+H++Cl—=AgCl↓+HF
难度: 中等查看答案及解析
-
下列说法正确的是 ( )
A.氢镍碱性电池原理为H2+2NiO(OH)=2Ni(OH)2,则该电池负极反应式为:H2—2e—+2OH—=2H2O
B.在测定中和热的实验中,盐酸物质的量一般要大于氢氧化钠物质的量,这样才能保证氢氧化钠中和完全
C.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
D.已知S(s)+O2(g)=SO2(g);△H1 S(g)+O2(g)=SO2(g);△H2,则△H1<△H2
难度: 中等查看答案及解析
-
25℃时,在25mL 0.1mol·L-1 NaOH溶液中,逐滴加入0.2mol·L-1 CH3COOH溶液,溶液pH的变化曲线如下图所示。下列分析中正确的是( )
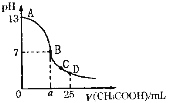
A.C点c(CH3COO—)>c(Na+)>c(H+)>c(OH—)
B.B点的横坐标a=12.5
C.D点c(CH3COO—)+c(CH3COOH)=c(Na+)
D.曲线上A、B间任一点,溶液中都有:c(Na+)>c(CH3COO—)>c(OH—)>c(H+)
难度: 中等查看答案及解析
-
普拉西坦是一种改善记忆、抗健忘的中枢神经兴奋药,其结构如下图,下列关于普拉西坦的说法正确的是( )
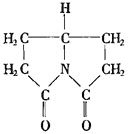
A.它既有酸性,又有碱性
B.它的二氯取代物有两种
C.它可以发生水解反应
D.分子中C、N、O原子均处于同一平面
难度: 中等查看答案及解析
-
恒温恒压下1 mol A和n mol B在一个容积可变的容器中发生如下反应:
A(g)
2B(g) + 2C(g),一段时间后达到平衡,生成a mol C。则下列说法中正确的是
A.物质A、B的转化率之比一定是1∶2
B.若起始时放入3 mol A+3n mol B,则达平衡时生成3a mol C
C.起始时刻和达平衡后容器中的压强比为 (1+n)/(1+n-a/2)
D.当v正(A) =2v逆(C)时,可断定反应达平衡
难度: 中等查看答案及解析
-
中央电视台《生活315:排毒基真能排毒吗》的节目中报道,一种名叫“排毒基强离子排毒仪”的产品正在市场热销。该仪器像一个普通电动脚盆,使用时往注满水的盆中放入双脚,加一些精盐,通电启动仪器,过一段时间,盆中开始出现绿色、红褐色的絮状物。下列说法正确的是
A.绿色、红褐色的絮状物质就是从脚底排出的体内毒素
B.绿色、红褐色的絮状物质是氢氧化亚铁和氢氧化铁
C.此电动脚盆仪器一定是用惰性电极制成的
D.往注满水的盆中加一些精盐的目的是降低溶液的导电性
难度: 简单查看答案及解析
-
2008年2月14日中央电视台报道,美国探测发现,在土卫六上的碳氢化合物的储量是地球上的几百倍。对此,有关说法不正确的是( )
A.碳氢化合物就是我们通常所说的烃
B.这一发现可以为我们提供足够的化石燃料,从而减少开发新能源的投资
C.从石油中可以获得重要的有机化工原料—乙烯
D.碳氢化合物中氢的质量分数越高,当其质量相等时完全燃烧消耗的O2越多
难度: 简单查看答案及解析