-
下列关于实验操作的叙述中正确的是( )
A.从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶
B.在中和滴定的实验过程中,目光应注视滴定管中的液面
C.用胶头滴管向试管中滴加液体,一定要将滴管伸入试管中
D.可燃性气体点燃之前必须验纯
难度: 简单查看答案及解析
-
下列各组溶液中每种溶质的物质的量浓度均为0.1 mol/L:①H2S ②NaHS ③Na2S ④H2S和NaHS混合液。下列说法正确的是( )
A.溶液pH由大到小的是: ③>②>①>④
B.c(S2―) 由大到小是:②>③>①>④
C.在H2S 和NaHS混合液中:2c(Na+)=c(H2S) + c(HS―) + c(S2―)
D.在NaHS溶液中:c(H+) + c(Na+)=c(OH―) + c(HS―) + c(S2―)
难度: 简单查看答案及解析
-
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。
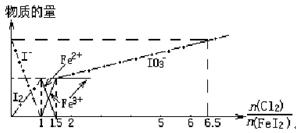
下列结论错误的是( )
A.Cl2、I2、IO3-、Fe3+的氧化性依次减小
B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5
D.若溶液的体积不变,则溶液的pH减小
难度: 简单查看答案及解析
-
现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算pH时假定溶液体积没有变化):
①向其中一份固体中加入100mL 2.0mol·L-1的NaOH溶液,加热使其充分反应后过滤,测得滤液的pH=14;
②向另一份固体中加入100mL 4.0 mol·L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且pH=1。
则②产生气体的体积(标准状况)为( )
A.2.352L B.2.448L C.2.688L D.2.856L
难度: 简单查看答案及解析
-
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:
3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
关于该反应的说法中正确的组合是( )
① 氧化剂是H3AsO3
② 还原性:Cl->As;
③ 每生成1molAs,反应中转移电子的物质的量为3mol;
④ M为OH-;
⑤ SnCl62-是氧化产物。
A.只有①③ B.①③⑤ C.①②③④ D.①②④⑤
难度: 简单查看答案及解析
-
将5.6g铁放入含有x mol FeCl3和y molCuCl2的混合溶液中,充分反应后,固体粉末仍为5.6g。则x: y可能是( )
A.3:7 B.8:7 C.1:7 D.1:1
难度: 简单查看答案及解析
-
下列实验过程中产生的变化与对应的图形相符合的是( )

难度: 简单查看答案及解析
-
某溶液中只可能含有下列离子中的几种:K+、NO3一、SO42-、NH4+、CO32-、SO32-,取200ml。该溶液分成两等份,进行以下实验:( )
(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL
(2)第二份先加足量的盐酸无现象,再加足量的BaCl2,得到2.33g固体,则该溶液中
A.可能含有K+、CO32-
B.一定含有K+且c(K+)≥0.1mol/L
C.一定不含有NO3一
D.肯定含有NO3一、SO42-、NH4+
难度: 简单查看答案及解析