-
向浓度均为0.010mol·L-1的Na2CrO4、NaBr和NaCl的混合溶液中逐滴加入0.010mol·L-1的AgNO3溶液。[已知Ksp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=1.12×10-12,Ksp(AgBr)=5.35×10-13,Ag2CrO4为砖红色],下列叙述正确的是
A. 原溶液中n(Na+)=0.040mol
B. Na2CrO4 可用作AgNO3溶液滴定Cl-或Br-的指示剂
C. 生成沉淀的先后顺序是AgBr一Ag2CrO4一AgCl
D. 出现Ag2CrO4沉淀时,溶液中c(Cl-):c( Br-)=177:535
难度: 中等查看答案及解析
-
下列说法不正确的是
A.可直接根据Ksp的数值大小比较难溶物在水中的溶解度
B.AgCl易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl)
C.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中
不变
D.常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变
难度: 中等查看答案及解析
-
已知常温下,AgBr的Ksp=4.9×10-13mol2·L-2、AgI的Ksp=8.3×10-17mol2·L-2下列说法正确的是:
A.常温下AgI水溶液中,Ag+和I-浓度的乘积是一个常数
B.常温下,在任何含AgI固体的溶液中,c(Ag+)=c(I-)且Ag+与I-浓度的乘积等于8.3×10-17mol2·L-2
C.常温下,将1mL 1.0×10-2mol/L的KI与AgNO3溶液等体积混合,则生成AgI沉淀所需AgNO3溶液的最小浓度为3.32×10-14 mol/L
D.向AgI饱和溶液中加入AgBr固体,c(I-)不变,Ksp值不变
难度: 中等查看答案及解析
-
用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是( )
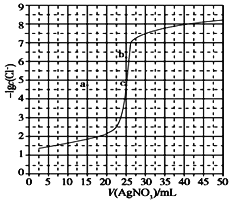
A.根据曲线数据计算可知Ksp(AgCl)的数量级为10-10
B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl)
C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
难度: 困难查看答案及解析
-
一定温度下,溴化银在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
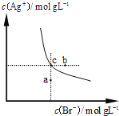
A.向溴化银悬浊液中加入溴化钠溶液,溴化银的Ksp减小
B.图中a点对应的是不饱和溶液
C.向c点对应的溶液中加入少量0.1 mol·L-1 AgNO3溶液,则c(Br-)增大
D.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点
难度: 中等查看答案及解析
-
已知p(A)=-lgc(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
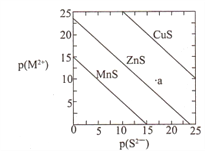
A.a点无ZnS沉淀生成
B.可用MnS除去MnCl2溶液中混有的少量ZnCl2
C.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)增大
D.CuS和MnS共存的悬浊液中,
难度: 困难查看答案及解析