-
在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好完全沉淀(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为_______ mol·L−1,此时溶液中c(CrO42−)等于__________ mol·L−1。(已知Ag2 CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。
高二化学填空题中等难度题查看答案及解析
-
实验室测定水体中氯离子含量,实验过程如下:向水样中加入K2CrO4溶液作指示剂,用0.0010 mol·L-1AgNO3溶液滴定至终点。已知:Ag2CrO4为不溶于水的砖红色沉淀;常温下Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)= 1.8×10-12。回答下列问题:
(1)滴定时,应使用____________(填“酸式”或“碱式”) 滴定管。
(2)滴定达到终点的标志是___________________________________________。
(3)实验过程中测得数据如下表:
编号
1
2
3
V(水样)/mL
10.00
10.00
10.00
V(AgNO3)/mL
3.75
4.01
3.99
计算水样中氯离子的含量为_______________mg/L(保留2位小数)
(4)滴定结束后:
①当溶液中的残余c(Cl-)=1.8×10-5mol/L,则此时溶液中c(CrO42-)=____________ mol·L-1。
②已知2AgCl+ CrO42-
2Cl-+Ag2CrO4,计算出该反应的平衡常数为____________。
(5)下列情况会造成实验测定结果偏低的是____________。(填标号)
A.锥形瓶洗涤后未干燥 B.滴定前,未使用标准液润洗滴定管
C.滴定管滴定前仰视读数,滴定后俯视读数
D.滴定管滴定前尖嘴部分充满溶液,滴定结束时滴定管尖嘴有气泡
高二化学填空题中等难度题查看答案及解析
-
自来水中氯离子的测定对人体健康有重要意义,实验室常用莫尔法测定水体中氯离子含量。实验过程如下:向水样中加入K2CrO4 (黄色) 溶液作指示剂,用AgNO3溶液滴定至终点。已知:Ag2CrO4为不溶于水的砖红色沉淀;常温下Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)= 1.8×10-12。
回答下列问题:
(1)滴定时,应使用____________(填“酸式”或“碱式”) 滴定管,原因是_______________________。
(2)水样应调至中性或弱碱性,强酸性时加入K2CrO4溶液发生反应的离子方程式是___________________________________________。
(3)滴定达到终点的标志是___________________________________________。
(4)实验过程中测得数据如下表:
编号
1
2
3
V(水样)/mL
10.00
10.00
10.00
c(AgNO3)/ mol·L-1
0.0010
V(AgNO3)/mL
3.75
4.01
3.99
计算水样中氯离子的含量为_______________mg/L(保留2位小数)
(5)滴定结束后:
①当溶液中的残余c(Cl-)=1.8×10-5mol/L,则此时溶液中c(CrO42-)=____________。
②已知2AgCl+ CrO42-
2Cl-+Ag2CrO4,计算出该反应的平衡常数为____________。
(6)下列情况会造成实验测定结果偏低的是____________。(填标号)
A.锥形瓶洗涤后未干燥
B.滴定前,未使用标准液润洗滴定管
C.酸式滴定管滴定前仰视读数,滴定后俯视读数
D.酸式滴定管滴定前尖嘴部分充满溶液,滴定结束时滴定管尖嘴有气泡
高二化学综合题中等难度题查看答案及解析
-
①已知t ℃时AgCl的Ksp=2×10-10;②Ag2CrO4是一种橙红色的固体。在t ℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A. 在t℃时,用AgNO3标准溶液滴定20mL未知浓度的KCl溶液,可以采用K2CrO4溶液为指示剂
B. 在饱和Ag2CrO4溶液中加入K2CrO4固体可使溶液由Y点到X点
C. 在t ℃时,以0.01 mol·L-1 AgNO3溶液滴定20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液, CrO42-先沉淀
D. 在t ℃时,反应Ag2CrO4(s)+2Cl-(aq)
2AgCl(s)+ CrO42- (aq)的平衡常数K=2.5×105
高二化学单选题中等难度题查看答案及解析
-
(11分)氧化还原滴定法是科研和生产中测定溶液中物质浓度的常用方法。
⑴莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银滴定待测液,进而测定溶液中Cl-的浓度 [Ksp(AgCl) =1.56×10-10,Ksp(Ag2CrO4)=1.10×10-12,Ag2CrO4为砖红色]
①滴定终点的现象是_________________;
②硝酸银标准液应装在 ________式滴定管中滴定。
③已知该滴定适宜的酸度范围是pH 6.5~10.5,但当溶液中有铵盐存在,c(NH4+)<0.05mol/L时,应将溶液的pH控制在6.5~7.2。下列有关说法你认为合理的有__________。
a.若溶液pH<6.5,则Cr2O72—+H2O
2CrO42—+2H+平衡左移,导致Ag2CrO4沉淀过迟,影响实验结果
b.若溶液中有铵盐存在时,当pH>7.2,则有可能因为生成[Ag(NH3)2]+,影响实验结果
c.滴定时应剧烈摇动,以使被AgCl沉淀吸附的Cl- 及时释放出来,防止滴定终点提前
⑵氧化还原滴定是水环境监测常用的方法,可用于测定废水中的化学耗氧量(单位:mg/L——每升水样中还原性物质被氧化需O2的质量)。某废水样100.00mL,用硫酸酸化后,加入0.01667mol/L的K2Cr2O7溶液25.00mL,使水样中的还原性物质在一定条件下完全被氧化。然后用0.1000mol/L的FeSO4标准溶液滴定剩余的Cr2O72-,实验数据记录如下:
实验数据
实验序号
FeSO4溶液体积读数/mL
滴定前
滴定后
第一次
0.10
16.20
第二次
0.30
15.31
第三次
0.20
15.19
①完成离子方程式的配平:
___Cr2O72-+___Fe2++____ _______ ____Cr3++____Fe3++____H2O
②计算废水样的化学耗氧量。 (写出计算过程,结果精确到小数点后一位。)
高二化学实验题困难题查看答案及解析
-
沉淀滴定和中和滴定的原理相同,如用AgNO3溶液滴定溶液中的Cl-的含量时常以CrO为指示剂,这是因为AgCl的溶解度比Ag2CrO4的溶解度________的缘故(填“大”或“小”),其实难溶性银盐较多,溶度积如下表:
银盐
性质
AgCl
AgI
AgCN
Ag2CrO4
AgSCN
沉淀颜色
白
黄
白
砖红
白
溶度积:
1.8×10-10
8.3×10-17
1.2×10-10
1.2×10-12
1.0×10-12
若用AgNO3去滴定KSCN溶液,可选用为滴定的合适指示剂有( )
A.NaCl B.KI C.NaCN D.Na2CrO4
刚好达到滴定终点时,发生的离子反应方程式为______________________。
高二化学填空题困难题查看答案及解析
-
已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,
Ksp(Ag2CrO4)=c2(Ag+)·c(CrO42-)=1.6×10-12,现用0.01 mol/L AgNO3溶液滴定0.01 mol/L KCl和0.001 mol/L K2CrO4混合溶液,通过计算回答:
(1)Cl-、CrO42-先生成沉淀的是________。
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是________mol/L。(设混合溶液在反应中体积不变)
高二化学填空题简单题查看答案及解析
-
已知:Ksp(AgCl)=c(Ag+)•c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=c2(Ag+)•c(CrO42-)=1.6×10-12,现用0.01mol/L AgNO3溶液滴定0.01mol/L KCl和0.001mol/L K2CrO4混合溶液,通过计算回答:
(1)Cl-、CrO42-先生成沉淀的是______.
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是______mol/L.(设混合溶液在反应中体积不变)高二化学解答题中等难度题查看答案及解析
-
在T ℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是
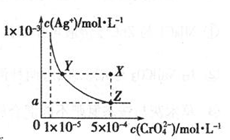
A.向饱和Ag2CrO4溶液中加入固体K2CrO4能使溶液由Y点变为X点
B.T℃时,在Y点和Z点,Ag2CrO4的Ksp相等
C.T℃时,Ag2CrO4 的 Ksp数值为 1×10-11
D.图中a=
×10-4
高二化学选择题简单题查看答案及解析
-
常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑C2O42-的水解)。下列叙述正确的是
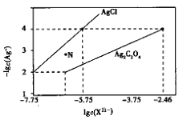
A. Ag2C2O4+2Cl-
2AgCl+C2O42-的平衡常数为109.04
B. N点表示AgCl的不饱和溶液
C. 向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D. Ksp(Ag2C2O4)的数量级等于10-7
高二化学单选题困难题查看答案及解析