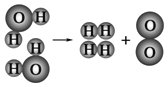
-
下列关于化学键的说法,正确的是( )
A.构成单质的分子中一定含有共价键
B.由非金属元素组成的化合物可能是离子化合物
C.非极性键只存在单质分子里
D.不同元素组成的多原子分子里的化学键一定是极性键
难度: 简单查看答案及解析
-
下图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子,则该物质是( )

A.CH3CHO B.CH3CH2OH
C.CH3COOH D.CH3OCH3
难度: 简单查看答案及解析
-
下列过程中共价键被破坏的是( )
A.碘升华 B.食盐熔化
C.水电解生成氢气和氧气 D.水结成冰
难度: 简单查看答案及解析
-
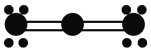
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是

A.分子中N、O间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物资含有6.02×
个原子
难度: 中等查看答案及解析
-
用电子式表示化合物形成过程的下列各式中,正确的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
能证明BeCl2是共价化合物的实验事实是( )
A. BeCl2的水溶液能导电 B. BeCl2的水溶液显酸性
C. BeCl2在熔融状态下不导电 D.在高温时有BeCl2分子存在
难度: 简单查看答案及解析
-
下列每组物质中含有的化学键类型相同的是( )
A.NaCl、HCl、H2O、NaOH
B.Cl2、Na2S、HCl、CO2
C.HBr、CCl4、H2O、CO2
D.Na2O2、H2O2、H2O、O2
难度: 中等查看答案及解析
-
下列有关事实及原因的分析中,错误的是
事实
原因
A.
分子内不同化学键之间存在键角
共价键具有方向性
B.
比Na稳定
的最外层为稳定的电子层结构而Na不是
C.
不含金属元素的化合物均是共价化合物
非金属元素间不能形成离子键
D.
分子比
分子稳定
键的键能比
键的大
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列关于化学键的叙述中,正确的是( )
A.只由非金属元素组成的化合物中,一定是共价化合物
B.某固体中,存在金属元素,则该物质一定是离子化合物
C.具有离子键的化合物,是离子化合物
D.具有共价键的化合物,是共价化合物
难度: 简单查看答案及解析
-
下列关于化学键的说法中,正确的是( )
A.凡含离子键的化合物,一定含金属元素
B.金属元素与非金属元素间一定形成离子键
C.构成单质分子的微粒一定含有共价键
D.由非金属元素组成的化合物不一定是共价化合物
难度: 简单查看答案及解析
-
下列有关化学键的说法正确的有几句( )
①离子键就是阴、阳离子之间的静电吸引
②只含有共价键的物质一定是共价化合物
③非金属气态单质中一定含非极性键
④仅含两种非金属元素的化合物一定是共价化合物
⑤原子间通过极性键结合成分子的物质,一定是共价化合物
⑥酒精溶于水的过程中共价键发生断裂
⑦在形成离子键的过程中一定会有电子的得失
A.1 B.2 C.3 D.4
难度: 简单查看答案及解析
-
下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.2
B.
C.
D. NH4Cl=NH3↑+HCl↑
难度: 简单查看答案及解析
-
下列4组原子序数的元素,彼此间能形成共价键的是( )
A.6和16 B.8和13 C.17和19 D.12和35
难度: 简单查看答案及解析
-
某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是( )

A.X原子可能为第ⅤA族元素
B.Y原子一定为第ⅠA族元素
C.该分子中既含有极性共价键又含有非极性共价键
D.从圆球的大小分析,该分子可能为N2F4
难度: 中等查看答案及解析
-
在通常情况下,稀有气体很难与其他元素发生化学反应,其原因是
A.稀有气体最外层电子数均为8个,很稳定
B.稀有气体的电子层数比较多,很稳定
C.稀有气体的最外层电子数均达到稳定结构
D.稀有气体的原子核所带电荷较多
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.三聚氰酸(C3H3N3O3)的结构式为
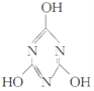 ,它属于共价化合物
,它属于共价化合物B.只含H、N、O三种元素的化合物,可能是离子化合物,也可能是共价化合物
C.NaHCO3、HCOONa均含有离子键和共价键
D.化合物MgO、SiO2、SO3中化学键的类型相同
难度: 简单查看答案及解析
-
下列变化化学键未被破坏的是( )
A.Cl2溶于水 B.NaCl固体熔化 C.H2与Cl2反应 D.干冰气化
难度: 简单查看答案及解析
-
南京理工大学团队成功合成了能在室温下稳定存在的五氮阴离子盐
,五氮阴离子
是制备全氮类物质
的重要中间体。下列说法正确的是
A.
属于化合物
B.
中含四种离子
C.每个
中含有35个电子
D.
中既含极性键又含非极性键
难度: 简单查看答案及解析
-
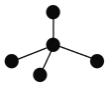
如图所示的X、Y、Z、W四种短周期元素的原子最外层电子数之和为22,下列说法正确的是
A.X、Y、W三种元素最低价氢化物的沸点依次升高
B.Z、X、W三种元素氧化物对应水化物的酸性依次增强
C.由X、W和氢三种元素形成的化合物中只含共价键
D.X、Z形成的二元化合物是一种新型无机非金属材料
难度: 中等查看答案及解析
-
下列关于化合物和化学键类型的叙述正确的是( )
HClO
Na2O2
NaCl
NH4Cl
A
共价化合物
共价键
离子化合物
离子键
离子化合物
离子键
共价化合物
共价键
B
共价化合物
共价键
离子化合物
共价键
离子化合物
离子键
离子化合物
共价键
C
共价化合物
共价键
离子化合物
离子键、共价键
离子化合物
离子键
离子化合物
离子键、共价键
D
共价化合物
离子键
离子化合物
离子键、共价键
离子化合物
离子键
离子化合物
离子键、共价键
A.A B.B C.C D.D
难度: 简单查看答案及解析