-
环境问题是实现科学发展必须正确面对的问题,下列说法不正确的是
A. 煤经气化和液化两个物理过程,可变为清洁能源
B. “酸雨”、“臭氧层受损”、“光化学烟雾”都与氮氧化物有关
C. 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体
D. 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
难度: 中等查看答案及解析
-
下列各组溶液中,可能大量共存的离子组有
A. 加入Al粉后反应产生H2的溶液中:NH4+、Na+、SiO32-、HCO3-
B. 滴加甲基橙试液后呈红色的溶液中: Na+、 CO32-、 K+、 AlO2-
C. 水电离产生的c(OH-)=1×11-11mol/L的溶液中:Al3+、SO42-、NO3-、Cl-
D. 含有大量I—的溶液中:K+、Mg2+、ClO-、SO42-
难度: 困难查看答案及解析
-
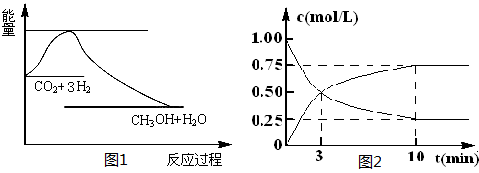
反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如下图所示,E1表示反应A+B→X的活化能。 下列有关叙述正确的是
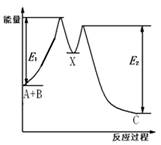
A. E2表示反应X→C的活化能
B. 反应A+B→C的△H<0
C. X是反应A+B→C的催化剂
D. 加入催化剂可改变反应A+B→C的焓变
难度: 中等查看答案及解析
-
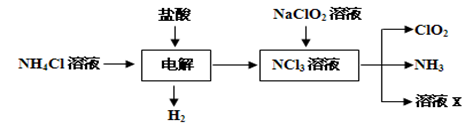
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是
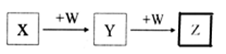
A. 若W是单质铁,则Z溶液可能是FeCl2溶液
B. 若W是氢氧化钠,则X与Z可反应生成Y
C. 若X是碳酸钠,则W可能是盐酸
D. 若W为氧气,则Z与水作用(或溶于水)一定生成一种强酸
难度: 困难查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A. 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑
B.硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-=NH3·H2O
C.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3—=Fe3++2H2O+NO↑
D.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O
Al(OH)3(胶体)+3H+
难度: 困难查看答案及解析
-
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是
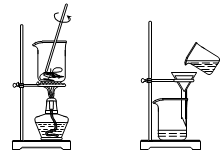
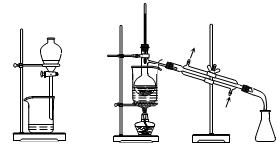
A.将海带灼烧 B.过滤含I-溶液 C.放出碘的苯溶液 D.分离碘并回收苯
难度: 中等查看答案及解析
-
一定量的锌与密度为1.85g/cm3,质量分数为98%,体积50mL 的浓H2SO4充分反应后,锌完全溶解,同时生成标准状况下的气体16.8 L。将反应后的溶液稀释至0.5 L,测得溶液中c(H+)=0.1mol•L-1。则生成的气体中H2和SO2的体积比为( )
A.4︰1 B.1︰2 C.1︰4 D.3︰1
难度: 中等查看答案及解析