-
将Na2O2投入FeCl3溶液中,可观察到的现象是 ( )
①生成白色沉淀 ②生成红褐色沉淀 ③有气泡产生
④因为Na2O2具有漂白性,所以FeCl3溶液褪色
A. ①④ B. ②③ C. ①③ D. 仅②
难度: 中等查看答案及解析
-
制备(NH4)2Fe(SO4)2•6H2O的实验中,需对过滤出产品的母液pH<1进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A.通入过量Cl2:Fe2+、H+、NH4+、Cl-、SO42-
B.加入过量NaClO溶液:NH4+、Fe2+、H+、SO42-、ClO-
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42-、OH-
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42-、Cl-、ClO-、OH-
难度: 中等查看答案及解析
-
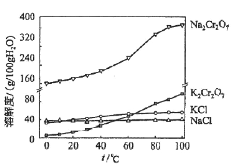
下列有关物质性质的比较,结论正确的是
A. 溶解度:Na2CO3<NaHCO3
B. 热稳定性:HCl<PH3
C. 沸点:C2H5SH<C2H5OH
D. 碱性:LiOH<Be(OH)2
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是
A.中子数为10的氧原子:
B.Mg2+的结构示意图:
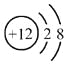
C.硫化钠的电子式:
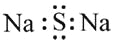
D.甲酸甲酯的结构简式:C2H4O2
难度: 中等查看答案及解析
-
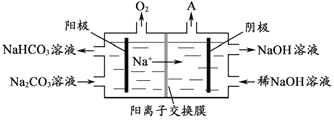
我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na
2Na2CO3+C。下列说法错误的是( )

A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:3CO2+4e-=2CO32-+C
D.充电时,正极反应为:Na++e-=Na
难度: 中等查看答案及解析
-
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y
2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于( )
A. 33% B. 40% C. 50% D. 65%
难度: 中等查看答案及解析
-
改变0.1
二元弱酸
溶液的pH,溶液中的
、
、
的物质的量分数
随pH的变化如图所示[已知
]。
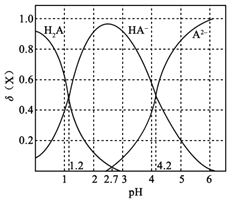
下列叙述错误的是
A. pH=1.2时,
B.
C. pH=2.7时,
D. pH=4.2时,
难度: 困难查看答案及解析


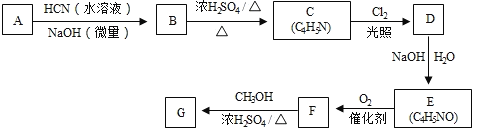
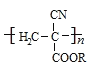 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下: