-
下列自然现象与化学变化无关的是
A. 雷雨肥庄稼 B. 植物光合作用
C. 形成臭氧层空洞 D. 冰雪消融
难度: 简单查看答案及解析
-
下列化学电池不易造成环境污染的是
A.锌锰电池 B.氢氧燃料电池 C.镍镉电池 D.铅蓄电池
难度: 简单查看答案及解析
-
在元素周期表中金属与非金属的分界处,可以找到
A.合金材料 B.催化剂 C.农药 D.半导体材料
难度: 简单查看答案及解析
-
下列物质既属于铵盐,又属于碳酸盐的是 ( )
A.NH3 B.(NH4)2CO3
C.NH4NO3 D.K2SO4
难度: 简单查看答案及解析
-
分离苯和水的混合物可利用 ( )
A.萃取 B.蒸发 C.分液 D.蒸馏
难度: 简单查看答案及解析
-
鉴别FeCl3溶液和Fe(OH)3胶体,下列方法中最简单有效的是( )
A.观察能否产生丁达尔现象 B.加热煮沸
C.加入足量的盐酸 D.加入足量的NaOH溶液
难度: 简单查看答案及解析
-
“绿色化学”是21世纪化学科学发展的重要方向之一,其核心是从源头上减少和消除工业生产对环境的污染。你认为“绿色化学”是指化学工业生产中( )
A.将化工厂建在远离城市的郊区
B.在化工厂种草、种树,使其成为花园工厂
C.不使用任何化学物质
D.少用或不用有害物质以及少排或不排放有害物质
难度: 简单查看答案及解析
-
Fe2O3+3CO
2Fe+3CO2 是高炉炼铁的主要反应,该反应的还原剂是
A.Fe2O3 B.CO C.Fe D.CO2
难度: 简单查看答案及解析
-
能正确表示下列化学反应的离子方程式是( )
A.碳酸钙与盐酸反应:CO32―+2H+=CO2↑+H2O
B.硫酸溶液加入氢氧化钡溶液中: Ba2++SO42-=BaSO4↓
C.碳酸氢钠溶液与氢氧化钠溶液混合:HCO3―+OH―= CO32-+H2O
D.氯气通入氯化亚铁(FeCl2)溶液中:Fe2++Cl2=Fe3++2Cl―
难度: 简单查看答案及解析
-
下列各组离子能同时在溶液中大量存在的是( )
A.CO32-、H+ B.CO32-、OH-
C.Ba2+、SO42- D.H+、OH-
难度: 简单查看答案及解析
-
国际上不提倡伊朗浓缩铀,因为铀
是制造原子弹的燃料。
原子核内含有中子数为
A.92 B.235 C.143 D.327
难度: 简单查看答案及解析
-
下列各组物质中,互为同系物的一组是( )
A.麦芽糖和蔗糖 B.乙烷和丙烷
C.12C和14C D.氧气和臭氧
难度: 简单查看答案及解析
-
下列说法错误的是 ( )
A.高纯度石英可用来制造光导纤维
B.棉花的主要成分是纤维素
C.原电池将电能转化为化学能
D.不锈钢是一种铁合金
难度: 简单查看答案及解析
-
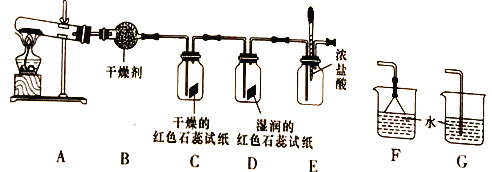
下列各组物质发生反应,有红棕色气体产生的是 ( )
A.Na和H2O B.Na2O2和H2O
C.Ca(OH)2和NH4Cl D.Cu和浓HNO3
难度: 简单查看答案及解析
-
已知苯在一定条件下能发生反应,此反应属于 ( )
+3H2
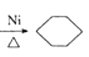
A.取代反应 B.加成反应 C.聚合反应 D.氧化反应
难度: 简单查看答案及解析
-
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是 ( )
A.CuCl2 B.Fe C.Al2O3 D.Na2CO3
难度: 中等查看答案及解析
-
下列物质中,物质的量最多的是(NA表示阿伏加德罗常数的值) ( )
A.标准状况下8g H2 B.标准状况下11.2 LCl2
C.常温常压下88gCO2 D.3NA个H2O
难度: 简单查看答案及解析
-
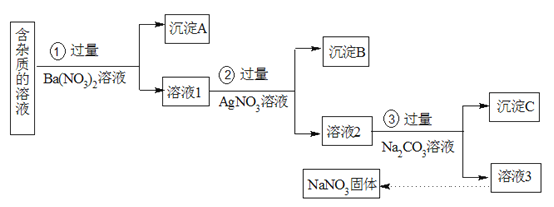
下列实验方法或实验结论不正确的是( )
A.用KSCN溶液检验某溶液中是否含有Fe3+
B.用盐酸除去NaOH溶液中的杂质Na2CO3
C.某无色溶液加入盐酸酸化无明显现象,再滴加氯化钡溶液,有白色沉淀产生,此溶液中含有SO42-
D.不能用排水法收集NH3
难度: 中等查看答案及解析
-
离子化合物是离子通过离子键结合成的化合物。下列物质不属于离子化合物的是( )
A.MgF2 B.NaOH C.H2O D.NaCl
难度: 简单查看答案及解析
-
下列物质中,不能发生酯化反应的是 ( )
A.乙醇(CH3CH2OH) B.乙酸(CH3COOH)
C.甘氨酸(H2N-CH2COOH) D.甲烷(CH4)
难度: 简单查看答案及解析
-
下列各组材料中,不能组成原电池的是 ( )
选项
A
B
C
D
两极材料
锌片、铜片
铜片、银片
锌片、石墨
铁片、铜片
插入溶液
蔗糖溶液
硝酸银溶液
稀硫酸
稀盐酸
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列物质中,不属于高分子化合物的是( )
A.淀粉 B.葡萄糖 C.蛋白质 D.纤维素
难度: 简单查看答案及解析
-
下列化学反应中,属于氧化还原反应的是( )
A. NH3+HCl=NH4Cl B. CaCO3
CaO+CO2↑
C. CuO+H2SO4=CuSO4+H2O D. 2Na2O2+2H2O=4NaOH+O2↑
难度: 中等查看答案及解析
-
工业上制硫酸的一步重要反应是2SO2(g)+O2(g)
2SO3(g),此反应在某条件下的某密闭反应容器中达到化学平衡状态。下列有关说法不正确的是 ( )
A.此时,SO2的转化率达到最大程度
B.此时,SO2的消耗速率等于SO2的生成速率
C.此时,SO3的浓度保持不变
D.该反应达到化学平衡状态后反应停止
难度: 简单查看答案及解析