-
已知氢化铵(NH4H)与NH4Cl的结构相似,又知NH4H与水反应有H2生成,下列有关叙述中不正确的是( )
①NH4H是离子化合物,含有离子键和共价键 ②NH4H溶于水,所形成的溶液显酸性
③NH4H与水反应时,NH4H是氧化剂 ④NH4H固体投入少量水中,有两种气体产生
A.①② B.②③ C.①②③ D.全部
难度: 中等查看答案及解析
-
下列物质属于天然高分子化合物的是( )
A.葡萄糖 B.油脂 C.蔗糖 D.淀粉
难度: 简单查看答案及解析
-
W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。下列叙述正确的是
A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>W
C.元素X的含氧酸均为强酸 D.Y的氧化物水化物为强碱
难度: 简单查看答案及解析
-
下列说法正确的是
A.石油的炼制过程都是化学变化过程
B.石油分馏目的是将含碳原子数较多的烃先气化经冷凝而分离出来
C.石油经过常、减压分馏、裂化等工序炼制后即能制得纯净物
D.石油分馏出来的各馏分仍是多种烃的混合物
难度: 简单查看答案及解析
-
下列物质中,含有非极性键的共价化合物是( )
A.CH3CH3 B.Na2O2 C.NaCl D.N2
难度: 简单查看答案及解析
-
正确掌握化学用语是学好化学的基础,下列有关化学用语表示正确的是( )
A.中子数为10的氧原子:
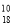 O
OB.Na2S的电子式:
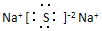
C.乙酸的球棍模型:
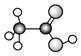
D.次氯酸的电子式:
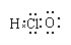
难度: 简单查看答案及解析
-
如下图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列关于该装置的说法正确的是
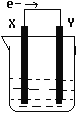
A.外电路电流方向为:X—外电路—Y
B.若两极分别为铁棒和碳棒,则X为碳棒,Y为铁棒
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两极都是金属,则它们的活动性顺序为X>Y
难度: 简单查看答案及解析
-
利用金属活性的不同,可以采取不同的冶炼方法冶炼金属。下列反应所描述的冶炼方法不可能实现的是( )
A.2Al2O3(熔融)
 4Al+3O2↑
4Al+3O2↑B.Fe2O3+3CO
 2Fe+3CO2
2Fe+3CO2C.Fe+CuSO4=FeSO4+Cu
D.2KCl(水溶液)
 2K+Cl2↑
2K+Cl2↑难度: 中等查看答案及解析
-
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是( )
A.减小压强能增大反应速率 B.增大压强能减小反应速率
C.使用适当的催化剂能增大反应速率 D.升高温度对反应速率无影响
难度: 中等查看答案及解析
-
利用下列反应不能制得括号中纯净物质的是( )
A.乙烯与水反应(乙醇)
B.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
C.液溴与苯用溴化铁作催化剂反应(溴苯)
D.乙烯与氯气反应(1,2-二氯乙烷)
难度: 中等查看答案及解析
-
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.143
0.086
0.102
0.074
主要化合价
+2
+3
+2
+6、-2
-2
A.L2+、R2-的核外电子数相等
B.M 与T 形成的化合物既能与强酸反应又能与强碱反应
C.氢化物的稳定性为H2T<H2R
D.单质与浓度相等的稀盐酸反应的速率为Q>L
难度: 中等查看答案及解析
-
某反应由两步反应A⇌B⇌C构成,它的反应能量曲线如反应过程如图所示,下列有关叙述正确的是( )
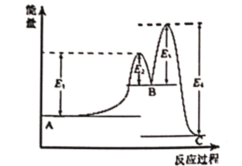
A.两步反应均为吸热反应
B.三种化合物中B最稳定
C.吸热反应一定需要加热
D.A反应生成C实现了化学能转化为热能
难度: 中等查看答案及解析
-
关于化学能与其他能量相互转化的说法正确的是( )
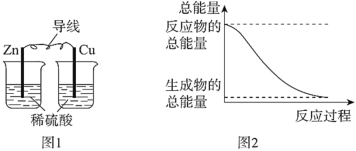
A.图1所示的装置能将化学能转变为电能
B.图2所示的反应为吸热反应
C.化学反应中能量变化的主要原因是化学键的断裂与形成
D.中和反应中,反应物的总能量比生成物的总能量低
难度: 中等查看答案及解析
-
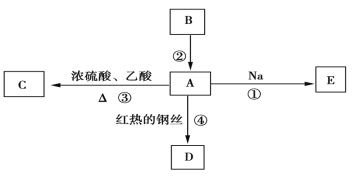
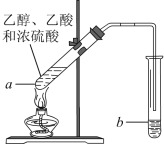
下列叙述正确的是( )。
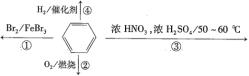
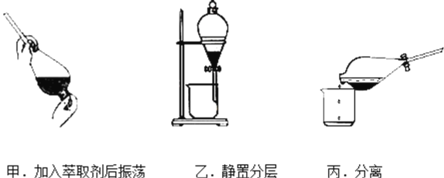
A.反应①为取代反应,有机产物与水混合后有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1mol苯最多与3molH2发生加成反应,因为一个苯分子含有三个碳碳双键
难度: 困难查看答案及解析
-
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。研究的燃料电池可分为镁—空气燃料电池,镁—海水燃料电池,镁—过氧化氢燃料电池,镁—次氯酸盐燃料电池。如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是
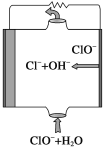
A.放电过程中OH−移向正极
B.电池的总反应式为Mg+ClO−+H2O=Mg(OH)2↓+Cl−
C.镁电池中镁均为负极,发生氧化反应
D.镁—过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e−=2H2O
难度: 中等查看答案及解析
-
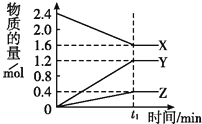
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g)。不能判断该分解反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)。不能判断该分解反应已经达到化学平衡的是( )A.密闭容器中二氧化碳的体积分数不变
B.密闭容器中气体的总物质的量不变
C.密闭容器中混合气体的密度不变
D.υ(NH3)正=2 υ(CO2)逆
难度: 中等查看答案及解析
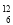 C和
C和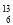 C C.CH3CH2CH2CH3和CH4
C C.CH3CH2CH2CH3和CH4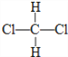 和
和 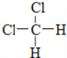 E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和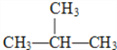
 海带灰
海带灰 滤液
滤液
 I2
I2