-
在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是
A. 称取粗盐后,把粗盐研磨细
B. 溶解时搅拌,加速粗盐溶解
C. 称量精盐前,把精盐固体转移到纸上
D. 蒸发时搅拌,防止局部温度过高,造成液体飞溅
难度: 中等查看答案及解析
-
小刘对某溶液所含溶质的记录,合理的是( )
A.NaNO3 AlCl3 HCl ZnSO4
B.NH4Cl K2SO4 KOH Na2CO3
C.K2CO3 NaCl KNO3 H2SO4
D.BaCl2 HCl CaCl2 NH3•H2O
难度: 困难查看答案及解析
-
下列关于化肥的说法不正确的是
A.化肥对提高农作物的产量具有重要作用
B.氯化钾(KCl)和磷酸氢二铵[(NH4)H2PO4]都属于复合肥料
C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味
D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
难度: 简单查看答案及解析
-
关于碳酸钠的说法错误的是( )
A.易溶于水 B.可用于洗涤油污 C.受热易分解 D.可用于制造普通玻璃
难度: 中等查看答案及解析
-
(2018湘潭)碳酸钠的俗称是( )
A.烧碱 B.纯碱 C.消石灰 D.食盐
难度: 简单查看答案及解析
-
(2018昆明)下列属于钾肥的是( )
A.Ca3(PO4)2 B.KCl C.CO(NH2)2 D.(NH4)2HPO4
难度: 简单查看答案及解析
-
下列化肥中,利用其物理性质即可与其他化肥区别开来的一种是( )
A.硫酸铵 B.磷矿粉 C.尿素 D.硝酸钾
难度: 中等查看答案及解析
-
某兴趣小组的同学进行“粗盐中难溶性杂质的去除”实验。下图是实验过程中的部分操作其中正确的是( )
A.
 取一定量粗盐 B.
取一定量粗盐 B.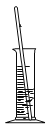 溶解 C.
溶解 C.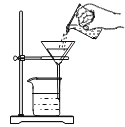 过滤 D.
过滤 D.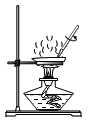 蒸发结晶
蒸发结晶难度: 简单查看答案及解析
-
(2018遵义改编)物质是变化的,下列物质在一定条件下不能实现一步转化的是( )
A.Mg→MgO→MgCl2
B.Fe2O3→Fe→FeCl2
C.CaCO3→Ca(OH)2→CaSO4
D.Cu→CuO→CuSO4
难度: 中等查看答案及解析
-
(2018宿迁)下列各组离子在水溶液中,能大量共存的是( )
A.Cu2+、Mg2+、NO
 、OH-
、OH-B.H+、SO
 、CO
、CO 、Ba2+
、Ba2+C.K+、NO
 、Cl-、Na+
、Cl-、Na+D.H+、NO
 、Ca2+、OH-
、Ca2+、OH-难度: 简单查看答案及解析
-
下列有关碳酸钠的反应中,恰好完全反应后所得溶液中溶质总质量增大的是( )
A.碳酸钠溶液与稀盐酸混合
B.碳酸钠溶液与氢氧化钙溶液混合
C.碳酸钠溶液与氯化钡溶液混合
D.将CO2通入氢氧化钠溶液中
难度: 中等查看答案及解析
-
(2018烟台改编)下列实验方案不能达到实验目的的是( )
选项
实验目的
实验方案
A
除去粗盐水中的Mg2+、Ca2+、SO
 ,得到精盐水
,得到精盐水依次加入过量的BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后过滤,向滤液中加入适量稀盐酸
B
检验久置空气中的NaOH固体是否变质
取适量样品加水充分溶解,滴加CaCl2溶液
C
分离铁粉和铜粉的混合物
加足量稀硫酸,充分反应后,过滤
D
除去MnO2中少量的KCl
加水充分溶解,过滤,洗涤,干燥
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2 B.Y可能是H2O
C.相对分子质量大小:X>Y D.Y可能是Na2SO4
难度: 简单查看答案及解析
-
甲、乙、丙三种物质间只通过一步反应就能实现如箭头所指方向的转化,下列不符合要求的甲、乙、丙依次为( )
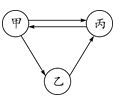
A.O2、CuO、H2O
B.Na2CO3、Na2SO4、NaOH
C.FeSO4、FeCl2、Fe
D.CaCO3、CaCl2、CO2
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的的是( )
选项
实验目的
实验操作
A
分离Ca(OH)2和CaCO3固体粉末
加水溶解、过滤
B
除去CO2气体中少量HCl气体
通过NaOH溶液
C
检验废水中是否含有SO42-
滴加BaCl2溶液
D
鉴别溶液:BaCl2、NaOH、HCl、MgSO4
将组内物质相互混合,观察现象
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
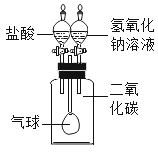
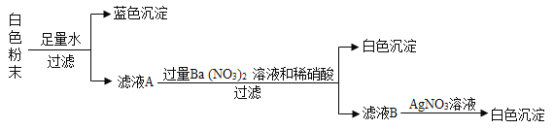
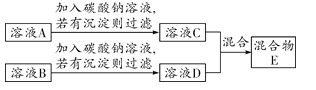
实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )

A. 甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B. 若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C. D物质可能是气体,也可能是沉淀
D. 溶液B中的溶质一定只含有NaOH和甲
难度: 困难查看答案及解析
-
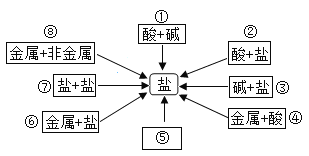
某同学在学习了金属及其化合物之间的转化规律后,给制了可以通过一步反应制取MgSO4的思维导图,其中所选用的物质错误的是

A.①—Mg B.②—MgCl2 C.③—H2SO4 D.④—Mg(OH)2
难度: 简单查看答案及解析
-
(2018哈尔滨)实验室有一包含杂质的碳酸氢钠样品100 g(杂质不含钠元素,受热不变化)其中钠元素质量分数为23%, 180 ℃时,将样品加热一段时间后称得固体质量为87.6 g,则分解的碳酸氢钠占原碳酸氢钠的质量分数为(2NaHCO3
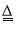 Na2CO3+H2O+CO2↑)( )
Na2CO3+H2O+CO2↑)( )A.33.6% B.40% C.47.3% D.60%
难度: 困难查看答案及解析
-
(2018孝感)某固体混合物由硫化钠(Na2S)和亚硫酸钠(Na2SO3)两种物质组成。已知该固体混合物中氧元素的质量分数为22%。则该固体混合物中钠元素的质量分数为( )
A.23% B.46% C.50% D.78%
难度: 困难查看答案及解析
 Na2CO3+H2O+CO2↑等。
Na2CO3+H2O+CO2↑等。