-
检验淀粉、蛋白质、葡萄糖溶液,依次可分别使用的试剂和对应的现象正确的是
A.碘水,变蓝色 ;浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀
B.浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色
C.新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色
D.碘水,变蓝色 ;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色
难度: 简单查看答案及解析
-
下列反应中Na2O2,只表现强氧化性的是
A.2Na2O2+2H2O=4NaOH+O2↑
B.Na2O2+MnO2=Na2MnO4
C.2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑
D.5Na2O2+2KMnO4+8H2SO4=5Na2SO4+K2SO4+2MnSO4+8H2O+5O2↑
难度: 简单查看答案及解析
-
一种溶液中大量存在以下主要离子:
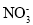 、
、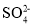 、Fe3+、H+、M,这些离子的物质的量之比为n(
、Fe3+、H+、M,这些离子的物质的量之比为n(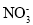 ):n(
):n(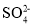 ):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M离子可能是
):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M离子可能是A.S2- B.Ca2+ C.Cl- D.Mg2+
难度: 中等查看答案及解析
-
ag铁粉与含有H2SO4的CuSO4溶液完全反应后,得到ag铜,则参加反应的CuSO4与H2SO4的个数之比为( )
A.1:7 B.7:1 C.7:8 D.8:7
难度: 中等查看答案及解析
-
下列各离子组合在指定条件下能够常量(浓度大于0.01mol·L-1)共存的是
溶液外观
离子浓度或pH
离子组
A
无色
水电离c(OH-)=1×10-10mol·L-1
Br-、I-、
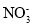 、Al3+
、Al3+B
透明
pH=2
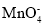 、K+、
、K+、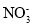 、Mg2+
、Mg2+C
透明
pH=13,c(
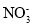 )=1×10-2mol·L-1
)=1×10-2mol·L-1[Ag(NH3)2]+、Na+、OH-、
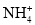
D
淡蓝色
水电离c(OH-)=1×10-10mol·L-1
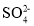 、Cu2+、Fe3+、Cl-
、Cu2+、Fe3+、Cl-A.A B.B C.C D.D
难度: 中等查看答案及解析
-
用足量的CO还原某金属氧化物,得到76.8g金属,将生成的气体通入足量澄清石灰水中,得到60g沉淀,则该氧化物是
A.FeO B.Fe2O3 C.CuO D.Cu2O
难度: 中等查看答案及解析
-
下列物质的制备方法中正确的是
A.稀硫酸和碳酸钙反应制备二氧化碳
B.在煮沸的NaOH溶液中滴加饱和FeCl3溶液制备Fe(OH)3胶体
C.在MnO2固体中滴入3%H2O2制备氧气
D.实验室中用铁和稀硝酸制备H2
难度: 中等查看答案及解析
-
下列说法正确的是
A.硅广泛用于光纤通讯
B.工艺师利用盐酸刻蚀石英制作工艺品
C.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4褪色
D.久置于空气中的氢氧化钠溶液,加盐酸时有气体生成
难度: 中等查看答案及解析
-
下图是碳循环中的一部分。下面对该图示的理解不正确的是
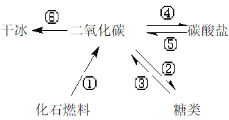
A.2010年坎昆气候会议讨论的议题主要涉及反应① B.反应②是在植物体内完成的
C.反应③是造成大气中CO2浓度逐渐升高的主要原因 D.反应④、⑥是人类缓解温室效应的措施
难度: 简单查看答案及解析
-
下列有关物质鉴别或检验方法的说法中正确的是
A.若某溶液中加入KSCN溶液,颜色无明显变化,再滴加少量氯水,溶液变血红色,证明原溶液中有Fe2+
B.用KI溶液可以鉴别马铃薯中是否含有淀粉
C.某溶液中加入Ba(NO3)2溶液,有白色沉淀生成,再加入稀盐酸白色沉淀不溶解,可说明原溶液中必含有
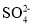
D.只用盐酸不能区别Na2SO3、Na2CO3、NaAlO2、Na2SO4四种溶液
难度: 中等查看答案及解析
-
下列实验设计及对应的离子方程式书写均正确的是
A.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
B.用食醋除去暖水瓶中的水垢(主要成分是CaCO3):CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
C.实验室用氨水吸收少量SO2:NH3·H2O+SO2=
 +
+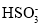
D.工业上用氯气和石灰乳制漂白粉:Cl2+OH-=Cl-+ClO-+H2O
难度: 中等查看答案及解析
-
足量的Cu和1 mol·L-1的稀硝酸反应,如果NO的浓度下降0.2 mol·L-1,则溶液中c(H+)同时下降(假定反应前后溶液体积不变)( )
A.0.2 mol·L-1
B.0.8 mol·L-1
C.0.6 mol·L-1
D.0.4 mol·L-1
难度: 中等查看答案及解析
-
在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2
 SiCl4
SiCl4 Si
SiB.FeS2
 SO2
SO2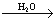 H2SO4
H2SO4C.N2
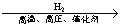 NH3
NH3 NH4Cl(aq)
NH4Cl(aq)D.MgCO3
 MgCl2(aq)
MgCl2(aq) Mg
Mg难度: 中等查看答案及解析
-
下列“实验结论”与“实验操作和现象”相符合的一组是
选项
实验操作和现象
实验结论
A
向苯酚浊液中滴加
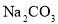 溶液,浊液变清
溶液,浊液变清苯酚的酸性强于
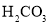 的酸性
的酸性B
在
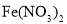 溶液中滴加酸化的
溶液中滴加酸化的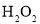 溶液,浅绿色变黄色
溶液,浅绿色变黄色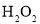 具有氧化性
具有氧化性C
向废
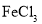 蚀刻液X中加入少量铁粉,铁粉溶解,未出现红色固体
蚀刻液X中加入少量铁粉,铁粉溶解,未出现红色固体X中一定不含

D
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝不滴落下来
氧化铝的熔点高于铝的熔点
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:
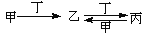 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是A.若甲为焦炭,则丁可能是O2 B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸 D.若甲为NaOH溶液,则丁可能是CO2
难度: 困难查看答案及解析
-
在温热气候条件下,浅海地区有厚层的石灰石沉积,而深海地区却很少。下列解析不正确的是
A.与深海地区相比,浅海地区水温较高,有利于游离的CO2增多、石灰石沉积
B.与浅海地区相比,深海地区压强大,石灰石岩层易被CO2溶解,沉积少
C.深海地区石灰石岩层的溶解反应为:CaCO3(s)+H2O(l)+CO2(aq)===Ca(HCO3) 2(aq)
D.海水呈弱碱性,大气中CO2浓度增加,会导致海水中
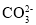 浓度增大
浓度增大难度: 中等查看答案及解析
-
下列说法错误的是
A.铁、锰、铬以及他们的合金称为黑色金属材料
B.用铬酸做氧化剂可以使铝表面的氧化膜产生美丽的颜色
C.可溶性铜盐有毒,但在生命体中,铜是一种不可缺少的微量元素
D.钠与水反应、镁与沸水反应、红色的铁与高温水蒸气反应均生成碱和氢气
难度: 中等查看答案及解析
-
下列有关物质性质与用途对应关系合理的是
A.硫酸铜溶液可以使蛋白质变性,可用来浸泡毛豆以保持新鲜绿色
B.浓H2SO4有脱水性,可用作干燥剂
C.NaHCO3能与酸反应,可用于治疗胃酸过多
D.SO2具有氧化性,可用于漂白纸浆
难度: 中等查看答案及解析
-
如图是硫元素价态与含硫元素物质类别的二维坐标图,其中B、C、D、E分子中均只含有一个S原子。下列说法错误的是
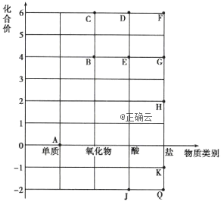
A.B、C分子中中心原子的杂化类型相同且通入
 溶液能够生成同一种沉淀
溶液能够生成同一种沉淀B.H代表的某种钠盐可与D反应生成A和B
C.G可代表多种钠盐,其中一种酸式盐的水溶液显酸性,抑制水的电离
D.F位置某盐的化学式为
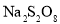 ,每个
,每个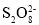 中过氧键数目为2
中过氧键数目为2难度: 困难查看答案及解析
-
明矾的化学式为KAl(SO4)2∙12H2O,其水溶液呈酸性。向明矾溶液中逐滴滴入氢氧化钡溶液至过量,则
A.有可能产生两种沉淀 B.不可能立即出现沉淀
C.不可能只有一种沉淀 D.有可能变为澄清溶液
难度: 中等查看答案及解析
-
国际纯粹与应用化学联合会(IUPAC)自2018年7月开始,通过每月评选,向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。其中,华东师范大学姜雪峰教授被IUPAC遴选为硫元素代言人,苏州大学刘庄教授被遴选为汞元素代言人,为中国青年化学家赢得了世界荣耀。下列有关硫、汞及其化合物的说法正确的是
A.S2与S8互为同位素
B.汞是常温、常压下唯一以液态存在的金属,俗称水银
C.硫在自然界中只有化合态形式
D.加热条件下,硫粉与铜反应直接化合生成CuS
难度: 中等查看答案及解析
-
高磷鲕状赤铁矿(主要含有
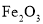 、少量
、少量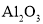 、CaO,
、CaO,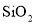 等)是我国一种重要的沉积型铁矿资源,以高磷鲕状赤铁矿为原料制备纯度较高的铁红,其流程如图所示。下列说法错误的是
等)是我国一种重要的沉积型铁矿资源,以高磷鲕状赤铁矿为原料制备纯度较高的铁红,其流程如图所示。下列说法错误的是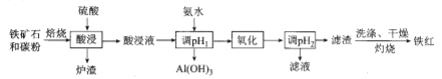
A.铁红可用于油漆、油墨、建筑物着色剂
B.酸浸液遇
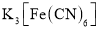 溶液生成蓝色沉淀
溶液生成蓝色沉淀C.洗涤滤渣时要用玻璃棒不断搅拌
D.氧化时选用的试剂可以是
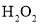 、NaClO溶液
、NaClO溶液难度: 中等查看答案及解析
-
SO2属于严重的大气污染物,可用H2与SO2高温反应消除SO2的污染,其反应原理可分为两步,过程如图所示:
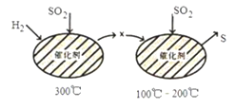
下列说法正确的是
A.SO2排放到空气中会形成pH≈5.6的酸雨
B.可用CuSO4溶液检验是否有X气体生成
C.在100℃~200℃温度时发生的是置换反应
D.工业上可用浓硝酸处理工业尾气中的SO2
难度: 中等查看答案及解析
-
下列化学方程式或离子方程式正确的是( )
A.用醋酸去除水垢:CaCO3+2H+=Ca2++H2O+CO2↑
B.甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2
 HCOOH+Cu2O↓+2H2O
HCOOH+Cu2O↓+2H2OC.实验室用液溴和苯在催化剂作用下制溴苯:
 +Br2
+Br2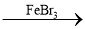
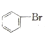 +HBr
+HBrD.将CO2通入苯酚钠溶液:2
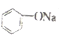 +CO2+H2O→2
+CO2+H2O→2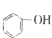 +Na2CO3
+Na2CO3难度: 中等查看答案及解析
-
北京大学和中国科学院的化学工作者成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是
A.K3C60晶体中既有离子键又有极性键 B.K3C60晶体的熔点比C60晶体的熔点低
C.该晶体熔化时能导电 D.C60分子中碳原子采取sp3杂化
难度: 中等查看答案及解析