-
地壳中含量最多的金属元素是( )
A.Al B.O C.Si D.Fe
难度: 简单查看答案及解析
-
有新物质产生的物质变化是( )
A.粮食发酵 B.切割玻璃 C.湿衣晒干 D.粉碎废纸
难度: 简单查看答案及解析
-
物质名称与化学式都正确的是( )
A.氧化二氮:N2O B.碳酸:CO3 C.碳酸氢铵:NH4HCO3 D.氯化钾:KCl2
难度: 简单查看答案及解析
-
液态水变成气态时体积膨胀,此过程中水分子发生的变化是( )
A.体积增大 B.质量增大 C.个数最多 D.间距增大
难度: 简单查看答案及解析
-
按目前上海市生活垃圾分类标准,废弃的电器属于( )
A.湿垃圾 B.有害垃圾 C.可回收物 D.干垃圾
难度: 简单查看答案及解析
-
表示两个氢分子的符号是( )
A.2HCl B.2H C.H2 D.2H2
难度: 简单查看答案及解析
-
能在氧气中燃烧并生成黑色固体的物质是( )
A.红磷 B.木炭 C.氢气 D.铁丝
难度: 简单查看答案及解析
-
干冰的用途是利用其化学性质的是( )
A.人工降雨 B.无水灭火 C.保存食物 D.舞台“雾气缭绕”
难度: 中等查看答案及解析
-
“火上浇油”可以使燃烧更剧烈,其主要原理是( )
A.增加易燃物 B.增大氧气浓度
C.提高可燃物的着火点 D.增大物质的接触面积
难度: 简单查看答案及解析
-
在常温下,向 pH=3 的苹果汁中不断地加水,则该苹果汁的 pH 变化情况正确的是( )
A.不断变小 B.一直变大 C.可能等于 6 D.可能等于 8
难度: 简单查看答案及解析
-
放入水中不能形成溶液的物质是( )
A.面粉 B.味精 C.蔗糖 D.酒精
难度: 简单查看答案及解析
-
镁带在氧气中燃烧化学方程式书写正确的是( )
A.Mg+O2
 MgO2 B.2Mg+CO2
MgO2 B.2Mg+CO2  2MgO+C
2MgO+CC.2Mg+O2↑
 2MgO D.2Mg+O2
2MgO D.2Mg+O2  2MgO
2MgO难度: 简单查看答案及解析
-
根据化学方程式 S+O2
 SO2,无法获得的信息是( )
SO2,无法获得的信息是( )A.反应前后反应物和生成物的种类 B.参加反应硫和二氧化硫的质量比
C.化学反应速率的快慢程度 D.反应发生所需要的条件
难度: 简单查看答案及解析
-
对“混合物”理解错误的是( )
A.一定由多种物质组成 B.一定有多种分子组成
C.可能由一种元素组成 D.可能由多种原子组成
难度: 简单查看答案及解析
-
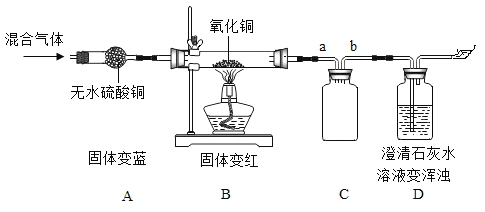
检验一瓶二氧化碳气体中是否混有少量一氧化碳,正确操作方法是( )
A.点燃气体,观察气体是否燃烧
B.通入灼热的氧化铜,观察固体颜色是否变化
C.闻气体的气味,是否闻到有特殊气味
D.倒入少量澄清的石灰水,观察溶液是否变浑浊
难度: 中等查看答案及解析
-
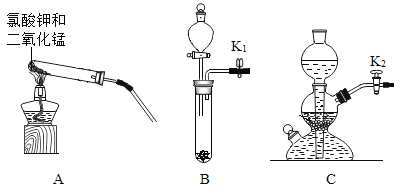
如图是气密性检查的实验操作,实验失败主要原因是( )
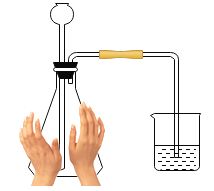
A.烧杯中的水太少
B.手捂得不够紧,导致热量不够
C.锥形瓶中没有水,导致长颈漏斗没有液封
D.导气管的橡皮管处没有弹簧夹
难度: 中等查看答案及解析
-
对 1mol N2 的理解错误的是( )
A.它与 1mol O2 所含的原子个数相同 B.与 CO 的摩尔质量相等,都是 28
C.含有 2mol 氮原子 D.约含 6.02×1023 个 N2
难度: 简单查看答案及解析
-
等物质的量的下列燃料,完全燃烧后得到二氧化碳质量最多的是( )
A.C3H6 B.C2H4 C.CH4 D.C
难度: 中等查看答案及解析
-
t℃时,在 5g 水中不断加入固体物质A,溶液质量变化情况如图所示,有关说法正确的是( )

A.t℃时,A物质的溶解度是 80g/100g 水
B.溶液 2、3都属于饱和溶液
C.溶液 1、2、3 溶质的质量分数依次增大
D.无法判断 A 物质溶解度受温度影响大小
难度: 中等查看答案及解析
-
Ca(HCO3)2
 CaCO3 +CO2 +H2O,是石灰岩溶洞形成的主要反应。将 1molCa(HCO3)2 加热 t2 秒时停止加热。如图表示 0→t2 秒过程中固体的物质的量随时间变化情况(该过程的 CaCO3 不分解)。说法错误的是( )
CaCO3 +CO2 +H2O,是石灰岩溶洞形成的主要反应。将 1molCa(HCO3)2 加热 t2 秒时停止加热。如图表示 0→t2 秒过程中固体的物质的量随时间变化情况(该过程的 CaCO3 不分解)。说法错误的是( )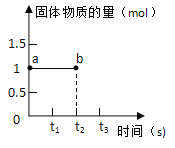
A.0→t2 反应阶段,固体 a、b 的物质的量不变
B.0→t2 反应阶段,固体a、b 的质量变小
C.a、b 两点固体中钙元素物质的量一定相等
D.固体a、b 中所含碳元素物质的量的比值一定为 2:1
难度: 困难查看答案及解析
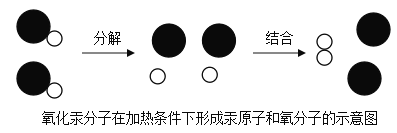
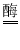 6X+6H2O,该反应生成物 X表示的物质是_______。1mol 果糖分子中碳原子的质量与______________g 蔗糖(C12H22O11)中碳原子质量相同。
6X+6H2O,该反应生成物 X表示的物质是_______。1mol 果糖分子中碳原子的质量与______________g 蔗糖(C12H22O11)中碳原子质量相同。