-
空气成分中,约占体积分数0.03%的气体是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化碳
难度: 简单查看答案及解析
-
下列元素中,人体摄入量过低会引起贫血的是
A.Fe B.Zn C.Na D.Ca
难度: 简单查看答案及解析
-
生活中常见的下列物品,主要是用有机合成材料制作的是( )
A.塑料玩具 B.纸箱 C.不锈钢水龙头 D.玻璃瓶
难度: 简单查看答案及解析
-
净水过程中可加入的吸附剂是
A.活性炭 B.生石灰 C.熟石灰 D.烧碱
难度: 中等查看答案及解析
-
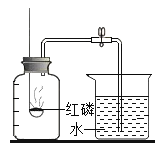
在氧气中燃绕,产生明亮蓝紫色火焰的是( )
A.硫 B.红磷 C.铁丝 D.氯气
难度: 简单查看答案及解析
-
一定条件下,能与二氧化碳反应的是
A.木炭 B.一氧化碳 C.氧化铜 D.氧气
难度: 困难查看答案及解析
-
从环保的角度考虑,下列燃料中最理想的是( )
A.煤 B.酒精 C.氢气 D.天然气
难度: 简单查看答案及解析
-
生铁是使用最多的金属材料,下列关于生铁的认识,正确的是( )
A.组成:只有铁元素,属于单质
B.性质:与橡胶类似,有较好的弹性
C.用途:可用于生产不锈钢
D.制备:常用铁矿石和焦炭化合而成
难度: 简单查看答案及解析
-
NH4NO3可作化肥,某NH4NO3溶液的pH=4.下列有关NH4NO3的说法,错误的是( )
A.属于氨肥
B.久施可能造成土壤酸化
C.氮元素只显+5价
D.可由氨水和硝酸反应得到
难度: 简单查看答案及解析
-
为了确定某化肥的种类,下列探究过程发生了化学变化的是
A.观察其外观,为白色晶体 B.闻其气味,无明显气味
C.测其溶解性,可溶于水 D.加熟石灰研磨,有刺激性气味
难度: 简单查看答案及解析
-
甲维盐(C56H81NO15)是种杀虫剂。 下列有关甲维盐的说法,正确的是( )
A.C、H、N、O四种元素的质量比为12:1:14:16
B.相对分子质量的计算式为12×56+1×81+14×1+16×15
C.C、H、N、O四种原子的个数比为56:81:15:15
D.氧元素的质量分数为:
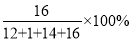
难度: 简单查看答案及解析
-
如图为某粒子的结构示意图,下列说法正确的是( )
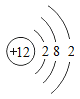
A.该粒子有12个质子
B.该粒子第一层的2个电子能量最高
C.该粒子已达到相对稳定结构
D.该粒子是阳离子
难度: 简单查看答案及解析
-
如图为某反应的微观示意图,“
 ”、“
”、“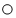 ”、“
”、“ ”各表示种原子,下列说法不正确的是( )
”各表示种原子,下列说法不正确的是( )
A.反应物有剩余
B.生成物都是化合物
C.反应前后分子总数不变
D.反应前后各元素的化合价都没有改变
难度: 中等查看答案及解析
-
下列化学方程式中,书写正确的是( )
A.
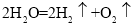
B.
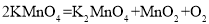
C.
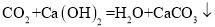
D.
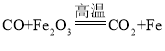
难度: 简单查看答案及解析
-
下列做法正确的是( )
A.油锅着火,用锅盖盖灭
B.用湿布包住菜刀,防止其生锈
C.为延长食品的保质期,用福尔马林(甲醛的水溶液)作防腐剂
D.不慎将浓硫酸沾到皮肤上,立即用大量水冲洗,再涂上3.5﹣5%的氢氧化钠溶液
难度: 中等查看答案及解析
-
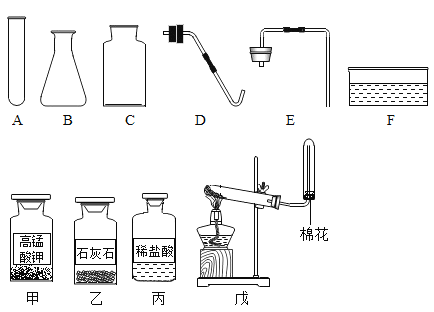
下列实验操作正确的是( )
A.
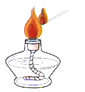 点燃酒精灯
点燃酒精灯B.
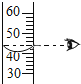 量筒读数
量筒读数C.
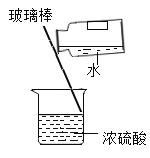 稀释浓硫酸
稀释浓硫酸D.
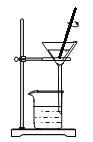 过滤
过滤难度: 中等查看答案及解析
-
室温下,对某固体物质的溶液进行如图所示的恒温蒸发操作。下列说法不正确的是
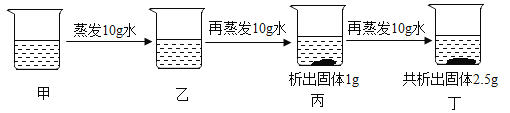
A.乙溶液为不饱和溶液
B.甲和乙溶液的溶质质量相等
C.丙和丁溶液的溶质质量分数相等
D.室温下该物质的溶解度为
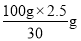
难度: 中等查看答案及解析
-
下列物质的性质与用途,正确且有对应关系的是( )
性质
用途
A
二氧化碳不燃烧,也不支持燃烧
干冰制造舞台烟雾效果
B
NaHCO3能与盐酸反应成NaCl、CO2和H2O
小苏打用于面点发酵
C
稀有气体通电时可以发出不同颜色的光
稀有气体用于制造多用途的电光源
D
甲烷密度小,极难溶干水
天然气用作燃料
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
除去下列物质中混有的少量杂质(据号内为杂质),所用方法正确的是( )
A.CO2(H2O):通过装有氢氧化钠的干燥管
B.CuSO4溶液(H2SO4):加入过量的铜粉,静置,过滤
C.NaCl(MgSO4):加入足量的水溶解,过滤,蒸发结晶
D.FeCl2溶液(CuCl2):加入过量的铁粉,静置,过滤
难度: 中等查看答案及解析
-
下列实验,现象正确且可得到相应结论的是( )
实验操作
现象
结论
A
在电解器的玻璃管中加满水,接通直流电
两极玻璃管中有气体生成,体积比为1:2
水是混合物
B
在加热条件下,将H2通入装有CuO粉末的试管中
红色粉末变为黑色
H2具有还原性
C
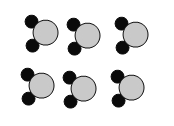
向充满CO2的软塑料瓶中倒入
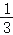 体积的水,立即盖紧并振荡
体积的水,立即盖紧并振荡塑料瓶变扁
CO2能溶于水,并和水反应生成碳酸
D
在导电性测试装置的小烧杯中加入适量稀盐酸,观察
装置中的小灯泡变亮
盐酸中有能自由移动的离子
A.A B.B C.C D.D
难度: 简单查看答案及解析
 氢原子
氢原子  氧原子)
氧原子)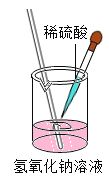
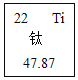
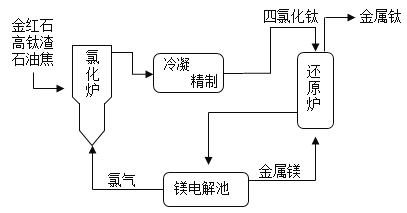
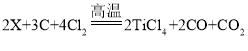 ,其中X是_____。
,其中X是_____。