-
生活中常常会发生一些变化,下列不属于化学变化或化学性质的是()
A.生活中用煮沸的方法降低水的硬度
B.镁粉用于制作照明弹
C.溶洞的形成
D.冰箱中放置活性炭
难度: 简单查看答案及解析
-
下面是对某一主题知识进行归纳的情况,其中完全正确的是()
A区别物质的方法
B安全知识
白酒和白醋——闻气味
空气、二氧化碳、氧气——用带火星的木条
硝酸铵、生石灰、无水硫酸铜、氯化钠四种白色
固体——用水区分
不锈钢、青铜、水银——合金
档案材料失火——用泡沫灭火器
误食少量重金属盐溶液——立即喝牛奶
C.日常生活中的化学知识
D.下列排序正确的是
食品中常用的干燥剂——生石灰
人体缺钙——幼儿易患佝偻病,老人易患骨质疏松
合成材料——合成橡胶、塑料、合成纤维
利用金属的年代:

碳元素的化合价:
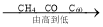
物质在水中的溶解性:
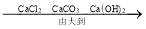
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
以下说法正确的是()
A.具有相同质子数的一类原子是同种元素
B.用硫酸铜溶液浸泡粽叶包粽子
C.饱和溶液析出晶体,溶质质量分数一定改变
D.有机物都含有碳、氢元素
难度: 简单查看答案及解析
-
以下说法不正确的是()
A.某无色溶液中滴加足量稀盐酸无明显现象,再加BaCl2溶液,产生白色沉淀,证明无色溶液中一定SO42-离子
B.除去粗盐水中的Mg2+、Ca2+、SO42-,得到精盐水,依次加入过量的Na2CO3溶液、BaCl2溶液、NaOH溶液,充分反应后过滤
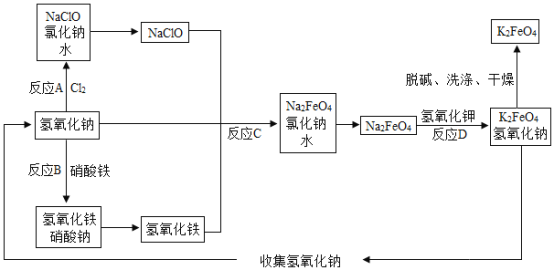
C.在一定条件下,利用石灰石、水、纯碱可制得烧碱
D.等质量、等质量分数的氢氧化钠溶液和稀硫酸溶液混合,取反应后溶液三份于试管中,分别滴入硫酸铜、氯化铁、氯化钡三种溶液,明显现象为蓝色沉淀、红褐色沉淀、白色沉淀
难度: 困难查看答案及解析
-
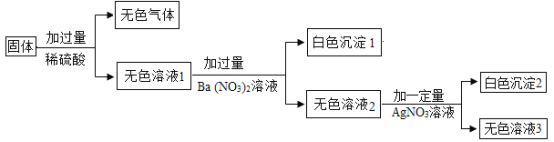
一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、氯化钙、硝酸铜、碳酸钠中的一种或几种。为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取149g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是()
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钾、硝酸铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
难度: 困难查看答案及解析
-
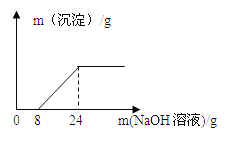
下面有关量的变化图像与其对应叙述相符的是()
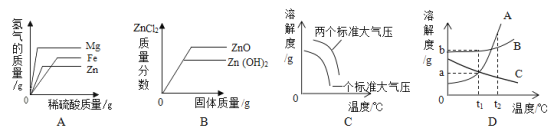
A.分别向相同质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸,三种金属与硫酸反应的剧烈程度:Mg>Zn>Fe
B.向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2所得氯化锌溶液的溶质质量分数与消耗固体质量
C.气体溶解度与温度和压强的关系
D.将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,所得溶液的质量质量分数为:B> A=C
难度: 困难查看答案及解析