-
《新修本草》是中国古代著名的中药学著作,记载药物844种。其中有关用“青矾”制备“绛矾”的描述:“本来绿色,新出窟未见风者,正如瑠璃……烧之赤色,故名绛矾矣。”据此推测,“青矾”的主要成分为
A. Fe2O3 B. FeSO4·7H2O C. Na2SO4·10H2O D. CuSO4·5H2O
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 用浓盐酸分别和MnO2、KClO3反应制备1mol氯气,转移的电子数均为2NA
B. 1molH2O最多可形成4NA个氢键
C. 常温下, pH=2的H2SO4溶液1L中,硫酸和水电离的H+总数为0.01NA
D. 常温常压下, O2与O3的混合气体16g,分子总数为NA
难度: 中等查看答案及解析
-
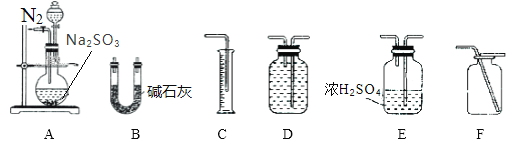
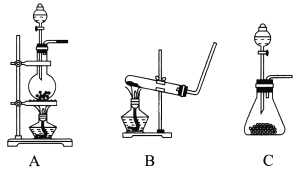
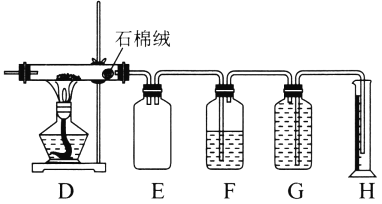
用下列实验装置进行相应的实验,能达到实验目的的是( )
选项
A
B
C
D
装置


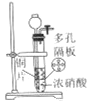
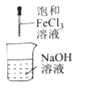
目的
制备Fe(OH)2
除去CO2中的SO2
制取少量的NO气体
制取氢氧化铁胶体
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
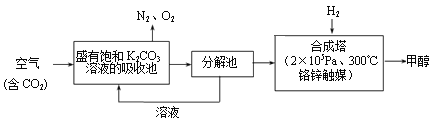
美国康奈尔大学的研究人员提出的可呼吸二氧化碳电池入选美国2016年十大创新术。 电池的工作原理如图所示。下列说法不正确的是( )
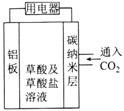
A. 该装置可将化学能转变成电能
B. 正极的电极反应式为2CO2+2e-=C2O42-
C. 利用该装置不但可减少CO2的排放,还可利用二氧化碳资源
D. 该装置中的两电极材料均被消耗,需定期补充、更换
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W、N的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y的次外层电子数是其电子总数的1/4,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是( )
A. Y和W与X形成的简单化合物的热稳定性:X2Y>X2W
B. 离子半径由大到小的顺序为Y2-< Z2+ < N-< W2-
C. ZX2和NY2中化学键一致,且微粒个数之比均为1∶2
D. 盐酸加入硫化钠中生成有臭鸡蛋气味的气体,可证明非金属性:N > W
难度: 中等查看答案及解析
-
常温下,下列有关溶液的说法正确的是
A. pH相等的①NH4Cl ②NH4Al(SO4)2 ③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×10−10,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A−)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3−)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F−) >c(K+ ) − c(CH3COO−)
难度: 中等查看答案及解析
-
CPAE是蜂胶的主要活性成分,其结构简式如图所示。下列说法不正确的是( )
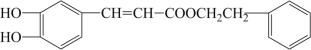
A. CPAE能发生取代反应、加成反应
B. CPAE能使酸性高锰酸钾溶液褪色
C. CPAE可与氢氧化钠溶液发生反应
D. CPAE在酸性条件下水解得到相对分子质量较小的有机物的同分异构体共有9种
难度: 中等查看答案及解析
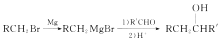 (R、R'均代表烃基或氢原子)
(R、R'均代表烃基或氢原子)