-
(10分)Na2SO3固体在实验室中长期保存易变质。
(1)实验室中欲检验Na2SO3固体样品是否已经变质,最简单的方法为________。
(2)选用以下装置和药品,通过测定生成SO2的质量,可计算m1 gNa2SO3固体样品的纯度。
反应原理:H2SO4(浓)+Na2SO3 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
供选用的药品:①浓硫酸 ②浓硝酸 ③碱石灰 ④氮气
供选用的装置如下(同一装置可重复选用),将所选仪器按连接顺序从左至右依次填入下表,并填入仪器中对应所加的试剂(不用填A装置中的药品;根据需要填写,可不填满)。
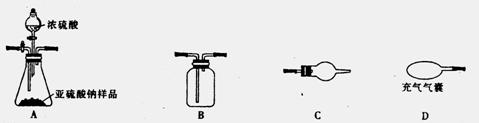
| 实验装置(填字母) | D | | | C | | | |
| 装置中所盛药品(填序号) | ④ | | | | | | |
(3)实验结束后,若测得A装置质量减少了m2 g,B装置增重了m3 g,上表中已知的C装置增重了m4 g,则该Na2SO3固体样品的纯度为________。
-
Na2SO3是一种重要的化工原料,但较易变质。
(1)实验室中欲检验Na2SO3固体样品是否已经变质,最简单的方法为_________________。
(2)某小组同学欲在实验室测定某Na2SO3样品的纯度。
方案一:通过测定生成SO2的质量,可计算mg Na2SO3固体样品的纯度。利用下列装置进行实验。
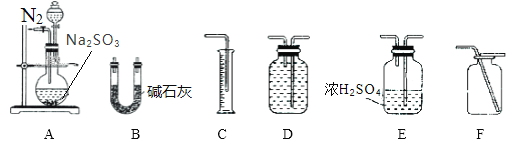
①选择装置A和B进行实验时,为使结果更精确还应选择装置_________________,装置A中反应前后通入N2的目的是_________________。
②实验结束后,若测得B装置增重了m1 g,则该Na2SO3固体样品的纯度为__________。
方案二:利用高锰酸钾溶液滴定亚硫酸钠溶液,实现定量测定。称取a g样品,置于烧杯中;加入适量蒸馏水,使样品溶解,然后配制成250 mL溶液;准确量取25.00 mL溶液置于锥形瓶中;用0. 1 000mol/L的酸性KMnO4溶液进行滴定,经多次滴定,达到滴定终点时,平均消耗20.00 mL溶液。
③反应原理为(用离子方程式表示)_________________。
④滴定时,通常不需要加入指示剂,理由是_________________;达到滴定终点读取数据时,若俯视液面,则测定结果_________________(填“偏高”、“偏低”、“无影响”)。
-
下列实验方案能达到实验目的的是( )
| 实验目的 | 实验方案 |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| B | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2 mL 1 mol/L NaOH溶液中先加入3滴1 mol/L MgCl2溶液,再加入3滴1 mol/L FeCl3溶液 |
A. A B. B C. C D. D
-
下列实验方案能达到实验目的的是
| 实验目的 | 实验方案 |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| B | 证明酸性条件下H2O2氧化性强于I2 | 向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝;再加入10%的H2O2溶液,溶液立即变蓝色 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2 mL1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
A. A B. B C. C D. D
-
过氧化钠保存不当容易变质。
(1)某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液,证明过氧化钠已经变质。
(2)检验样品中还有过氧化钠的方法是 ________。
(3)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设
计用下图装置来测定过氧化钠的质量分数。
 上图中的E和F构成量气装置,用来测定O2的体积。
上图中的E和F构成量气装置,用来测定O2的体积。
①写出装置A和B中发生反应的离子方程式:
装置A:, 装置B:。
②NaOH的作用是________。
③本实验中测量气体体积时应注意的事项有
。
④他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品
中过氧化钠的质量分数为________。
-
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,可以实现实验目的的是( )
A.测所得溶液的pH
B.取溶液滴入酚酞观察是否变红
C.取溶液加入盐酸观察是否有气泡
D.取溶液加入CuSO4观察是否有沉淀
-
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,可以实现实验目的是( )
A.测所得溶液的pH
B.取溶液滴入酚酞观察是否变红
C.取 溶液加入盐酸观察是否有气泡
溶液加入盐酸观察是否有气泡
D.取溶液加入CuSO4观察是否有沉淀
-
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )
A.Na+、Fe3+、K+、ClO— 都可在该物质的溶液中大量共存
B.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
C.向0.1 mol·L-1该物质的溶液中逐滴滴加0.1 mol·L-1 NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如下图所示
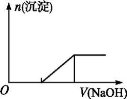
D.向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42- 完全沉淀的离子方程式为:Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓
-
实验室有一瓶久置的Na2SO3固体试剂,已部分变质,为测定其纯度,实验设计与操作如下,请回答问題:
(1)Na2SO3变质的原因(用化学方程式表示)___________。
(2)取一定量的样品溶于水,加入过量的BaCl2溶液,然后过滤(如图)、洗涤、干燥、称量,其中洗涤沉淀的具体操作为___________。
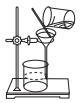
(3)实验时用BaCl2比用CaCl2好,写出两点理由:___________。
-
由下列实验及现象不能推出相应结论的是
| 选项 | 实验 | 现象 | 结论 |
| A | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加入足量稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品己变质 |
| B | 向硅酸钠溶液中滴加1滴酚酞溶液,然后逐滴加入稀盐酸至红色变浅并接近消失时停止 | 试管里出现凝胶 | 非金属性:Cl>Si |
| C | 向盛有浓氨水的锥形瓶中通入氧气, 并将灼热的铂丝置于液面上方 | 铂丝保持红热,且瓶内有白烟产生 | 氨水易挥发 |
| D | 将金属钠放入燃烧匙中,点燃,迅速伸入集满SO2的集气瓶 | 产生大量黄色的烟,且瓶内有白色颗粒生成 | SO2具有氧化性 |
A. A B. B C. C D. D


 上图中的E和F构成量气装置,用来测定O2的体积。
上图中的E和F构成量气装置,用来测定O2的体积。
