-
能源是可以直接或经转换提供人类所需的光、热、动力等任意形式能量的载能体资源。确切而简单地说,能源是自然界中能为人类提供某种形式能量的物质资源,人类的一切经济活动和生存都依赖于能源的供给。下列对能源的认识错误的是
A.阳光、风力、潮汐、流水都属于能源
B.氢气、太阳能、地热能都属于绿色能源
C.天然气、乙醇、氢气都属于可再生能源
D.煤、石油、太阳能都属于一次能源
难度: 简单查看答案及解析
-
分子式为
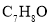 的有机物,分子中含苯环,且不能与
的有机物,分子中含苯环,且不能与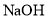 溶液反应的结构有(不含立体异构)( )
溶液反应的结构有(不含立体异构)( )A.1种 B.2种 C.3种 D.4种
难度: 简单查看答案及解析
-
下列实验方案不能达到实验目的的是( )
选项
实验目的
实验方案
A
制取少量氨气
将浓氨水滴入碱石灰中
B
加快氧气的生成速率
在过氧化氢溶液中加入少量
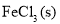
C
检验亚硫酸钠溶液是否变质
取样,加入足量用硝酸酸化的硝酸钡溶液
D
制备少量氯化氢气体
向浓盐酸中滴加浓硫酸
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
糖类、油脂和蛋白质是人体生命所需的基础化学物质,同时为生命活动提供能量保障。下列有关说法不正确的是( )
A.淀粉和纤维素互为同分异构体,两者水解的最终产物相同
B.医用酒精具有杀菌性能,是因为它可使蛋白质变性
C.纤维素能通过酯化反应得到醋酸纤维,是因为纤维素分子中含有羟基
D.植物油氢化得到的硬化油不易变质,是因为氢化过程中发生了加成反应
难度: 简单查看答案及解析
-
在铁棒上镀铜的实验装置如图所示,下列判断不正确的是
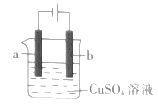
A.a极上发生还原反应
B.b极只能用纯铜
C.CuSO4溶液可以换成氯化铜溶液
D.该实验过程中阴离子种类保持不变
难度: 简单查看答案及解析
-
根据如图所示的实验所得的推论不合理的是( )
已知,苯酚的熔点为43℃。
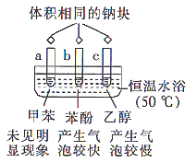
A.试管
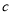 中钠沉在底部,说明密度:乙醇<钠
中钠沉在底部,说明密度:乙醇<钠B.苯酚中羟基上的氢原子比甲苯中甲基上的氢原子更活泼
C.苯酚中羟基的活性比乙醇中羟基的活性强
D.试管
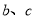 中生成的气体均为
中生成的气体均为 ,说明苯酚和乙醇均显酸性
,说明苯酚和乙醇均显酸性难度: 简单查看答案及解析
-
短周期元素
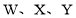 在元素周期表中的位置如图,元素
在元素周期表中的位置如图,元素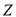 的焰色反应为紫色。下列说法正确的是( )
的焰色反应为紫色。下列说法正确的是( )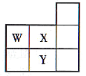
A.
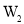 的沸点比
的沸点比 的高
的高B.
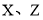 形成的化合物的水溶液呈碱性
形成的化合物的水溶液呈碱性C.
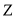 与
与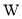 形成的化合物中一定不含共价键
形成的化合物中一定不含共价键D.
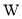 分别与
分别与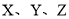 形成的化合物中,
形成的化合物中,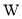 的化合价相同
的化合价相同难度: 中等查看答案及解析
-
羧酸和醇发生酯化反应的过程如下图所示:
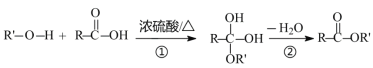
可见酯化反应不是简单的取代反应,步骤①和②的有机反应类型为( )
A.①为加成反应,②为消去反应 B.①为氧化反应,②为还原反应
C.①为取代反应,②为消去反应 D.①为加成反应,②为氧化反应
难度: 中等查看答案及解析
-
实验室可利用反应Na2S+H2NCN+2H2O
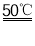 CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是
CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是
A.装置B中盛放的试剂为饱和NaHS溶液
B.装置C可用水浴加热
C.持续通入H2S,有利于提高反应液中硫脲的含量
D.为获得硫脲晶体可将烧瓶中的反应液蒸发至干
难度: 中等查看答案及解析
-
180℃时,将0.5 mol H2和1 mol CO2通入1L的恒容密闭容器中,反应生成甲醇蒸气(
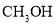 )和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示。下列说法中不正确的是( )
)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示。下列说法中不正确的是( )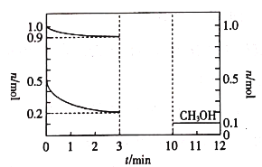
A.该反应的化学方程式:
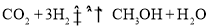
B.在0~3 min内,
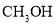 的平均反应速率为
的平均反应速率为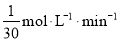
C.在3~10 min内,反应仍未达到平衡状态
D.10 min时,再通入0.5 mol H2和1 mol CO2,可提高H2和CO2的转化率
难度: 中等查看答案及解析
-
盆栽鲜花施用S诱抗素制剂,可以保证鲜花盛开。S诱抗素的分子结构简式如下图所示。下列关于该分子的说法错误的是( )
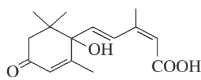
A.不能发生水解反应 B.可以发生酯化反应
C.既可以发生氧化反应又可以发生还原反应 D.共平面的碳原子可能有15个
难度: 中等查看答案及解析
-
有机化合物分子中基团之间的相互影响会导致物质的化学性质不同。下列事实不可以用上述观点解释的是( )
A.苯不能与溴水发生取代反应,而苯酚能与溴水发生取代反应
B.乙醇不能与碱发生中和反应,而乙酸能与碱发生中和反应
C.2-甲基-1-丙醇能发生消去反应,2,2-二甲基-1-丙醇不能发生消去反应
D.乙烷不能使高锰酸钾溶液褪色,而甲苯能使高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
25℃时,向20mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1的NaOH溶液,(忽略反应前后溶液体积变化)原溶液中部分粒子的物质的量随滴入NaOH溶液体积的变化如图所示。下列说法不正确的是
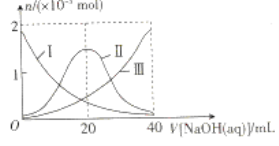
A.II表示的是HA-的物质的量的变化曲线
B.NaHA水溶液显碱性
C.
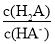 的值随若V[NaOH(aq)]的增大而减小
的值随若V[NaOH(aq)]的增大而减小D.当V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.05mol•L-1
难度: 困难查看答案及解析
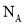 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )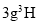 中含有的中子数为
中含有的中子数为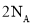 B.
B.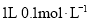 碳酸钠溶液中含有的
碳酸钠溶液中含有的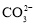 数目为
数目为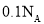
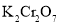 被还原为
被还原为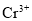 时,转移的电子数为
时,转移的电子数为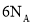 D.
D.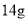 乙烯中含有的共用电子对的数目为
乙烯中含有的共用电子对的数目为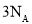
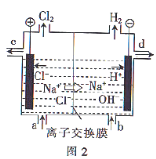
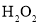 的绿色方法,其反应原理为
的绿色方法,其反应原理为 ,装置如图所示,下列说法错误的是( )
,装置如图所示,下列说法错误的是( )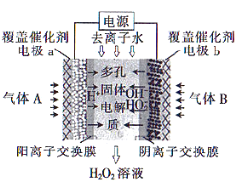
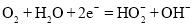
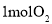 通过电路中的电子为
通过电路中的电子为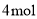
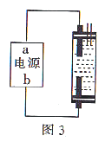
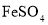 溶液,再与等物质的量的
溶液,再与等物质的量的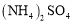 反应,制备补血剂硫酸亚铁铵晶体
反应,制备补血剂硫酸亚铁铵晶体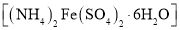 。已知:硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
。已知:硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。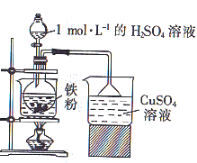
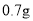 铁粉,用
铁粉,用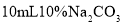 溶液煮沸洗净,加入烧瓶中,再加入
溶液煮沸洗净,加入烧瓶中,再加入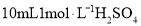 溶液反应。
溶液反应。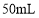 乙醇中,析出晶体。用95%的酸性乙醇溶液洗涤晶体两次,用滤纸吸干,即可得到硫酸亚铁铵晶体。
乙醇中,析出晶体。用95%的酸性乙醇溶液洗涤晶体两次,用滤纸吸干,即可得到硫酸亚铁铵晶体。 的
的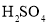 溶液的仪器名称是_________。若用98%的浓硫酸来配制
溶液的仪器名称是_________。若用98%的浓硫酸来配制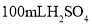 溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、________、________。图示装置中的加热方式是______。
溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、________、________。图示装置中的加热方式是______。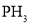 气体,因此需使用封闭装置。用
气体,因此需使用封闭装置。用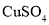 溶液吸收
溶液吸收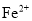 发生氧化还原反应:
发生氧化还原反应: 。现称取
。现称取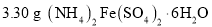 (相对分子质量为392)产品(杂质只有
(相对分子质量为392)产品(杂质只有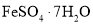 ,相对分子质量为278)溶于稀硫酸中,然后用
,相对分子质量为278)溶于稀硫酸中,然后用 的酸性高锰酸钾溶液滴定,达到终点时消耗了
的酸性高锰酸钾溶液滴定,达到终点时消耗了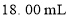 酸性高锰酸钾溶液。
酸性高锰酸钾溶液。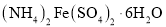 的质量分数为________(保留4位有效数字)。
的质量分数为________(保留4位有效数字)。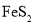 ,杂质不与盐酸反应)为原料制备三氯化铁晶体
,杂质不与盐酸反应)为原料制备三氯化铁晶体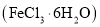 的工艺流程如图所示:
的工艺流程如图所示: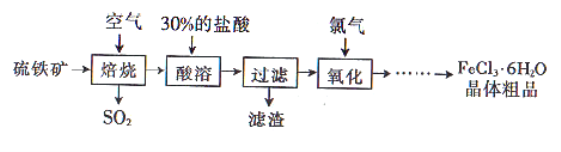
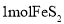 ,被氧化转移
,被氧化转移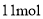 电子,则该反应的氧化产物为_____________。
电子,则该反应的氧化产物为_____________。 ,另取“焙烧”后的烧渣少许,用________(从上述试剂中选择,填标号)溶解,将所得溶液滴入______________(从上述试剂中选择,填标号)中,若_________,则说明“酸溶”后的溶液中含
,另取“焙烧”后的烧渣少许,用________(从上述试剂中选择,填标号)溶解,将所得溶液滴入______________(从上述试剂中选择,填标号)中,若_________,则说明“酸溶”后的溶液中含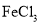 溶液中得到
溶液中得到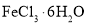 的操作包括_______、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________________。
的操作包括_______、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________________。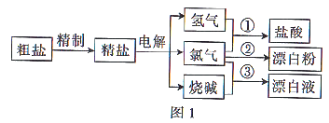
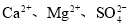 等杂质离子,欲用
等杂质离子,欲用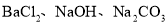 、盐酸进行精制,则这些试剂的加入顺序依次为
、盐酸进行精制,则这些试剂的加入顺序依次为 、________、_________、________。
、________、_________、________。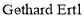 证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如下:
证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如下: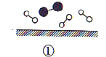


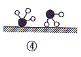
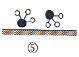
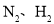 分子中均是单键 B.②→③需要吸收能量
分子中均是单键 B.②→③需要吸收能量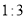 时,平衡时混合物中氨的体积分数
时,平衡时混合物中氨的体积分数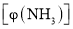 与温度的变化关系如图所示。
与温度的变化关系如图所示。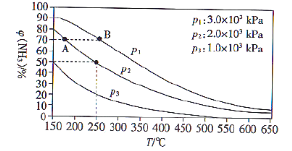
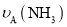 和
和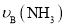 表示从反应开始至达到平衡状态A、B时的化学反应速率,则
表示从反应开始至达到平衡状态A、B时的化学反应速率,则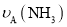 __________(填“>”“<”或“=”)
__________(填“>”“<”或“=”)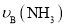 。
。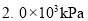 时,
时,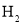 的转化率为___________(结果保留三位有效数字)%。
的转化率为___________(结果保留三位有效数字)%。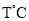 时,在
时,在 的恒容密闭容器中加入
的恒容密闭容器中加入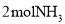 ,此时压强为
,此时压强为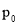 ,用
,用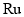 催化氨气分解,若平衡时氨气的转化率为50%,则该温度下反应
催化氨气分解,若平衡时氨气的转化率为50%,则该温度下反应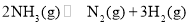 ,用平衡分压代替平衡浓度表示的化学平衡常数
,用平衡分压代替平衡浓度表示的化学平衡常数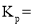 __________(用含
__________(用含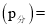 气体总压
气体总压 体积分数]
体积分数]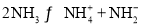 ,常温下
,常温下 ,常温下,将一定量的金属钠投入
,常温下,将一定量的金属钠投入 液氨中,待反应结束后,收集到标准状况下
液氨中,待反应结束后,收集到标准状况下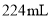 氢气。忽略溶液体积的变化,则恢复到室温时所得溶液中
氢气。忽略溶液体积的变化,则恢复到室温时所得溶液中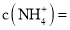 ______
______ 。
。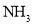 消除
消除 污染,其反应原理为
污染,其反应原理为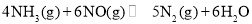 (1)
(1)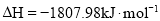 。在刚性容器中,
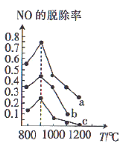
。在刚性容器中,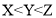 ),在相同时间内不同温度条件下,得到
),在相同时间内不同温度条件下,得到 时对应的曲线为_________(填“a”“b”或“c”)。
时对应的曲线为_________(填“a”“b”或“c”)。 的脱除率均先升高后降低的原因为__________。
的脱除率均先升高后降低的原因为__________。