-
下列物质中,既含有离子键,又含有非极性共价键的是
A. Na2O2 B. CaCl2 C. NH4Cl D. H2O
难度: 简单查看答案及解析
-
下列离子中半径最大的是( )
A.Na+ B.Mg2+ C.O2- D.F-
难度: 简单查看答案及解析
-
Na和Na+两种微粒中,不相同的是( )
①核内质子数②核外电子数③最外层电子数④核外电子层数
A.①② B.②③ C.③④ D.②③④
难度: 中等查看答案及解析
-
有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
难度: 中等查看答案及解析
-
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为( )
A.HX B.H2X C.XH4 D.XH3
难度: 简单查看答案及解析
-
与OH-具有相同质子数和电子数的微粒是( )
A.F- B.Cl- C.NH3 D.NH
难度: 简单查看答案及解析
-
恒温、恒容的条件下对于N2(g)+3H2(g)
 2NH3(g)的反应,达到化学平衡状态的标志为
2NH3(g)的反应,达到化学平衡状态的标志为A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的压强不变
D.N2、H2、NH3分子数之比为1:3:2的状态
难度: 中等查看答案及解析
-
元素周期表中,在金属元素与非金属元素的分界线附近最容易找到的材料是( )
A.制催化剂的材料 B.耐高温、耐腐蚀的合金材料
C.制农药的材料 D.半导体材料
难度: 简单查看答案及解析
-
元素的性质随着原子序数的递增呈现周期性的变化的根本原因是( )
A.元素相对原子质量的递增,量变引起质变
B.元素的金属性和非金属性呈周期性变化
C.元素原子核外电子排布呈周期性变化
D.元素化合价呈周期性变化
难度: 中等查看答案及解析
-
下列物质的电子式书写正确的是( )
A. N2的电子式:
 B. Na2O2的电子式:
B. Na2O2的电子式:
C. CO2的电子式:
 D. NH4Cl的电子式:
D. NH4Cl的电子式:
难度: 简单查看答案及解析
-
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
A. 质子数c>b B. 原子半径X<W
C. 离子半径Y2-<Z- D. 离子的氧化性W3+>X+
难度: 中等查看答案及解析
-
下列属于吸热反应的是( )
A.金属钠与水的反应 B.氢气燃烧
C.浓硫酸的稀释 D.Ba(OH)2·8H2O和NH4Cl(固体)混合
难度: 简单查看答案及解析
-
在如图所示的原电池中,下列说法正确的是
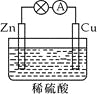
A.负极发生还原反应
B.正极反应为 Cu-2e-=Cu2+
C.电子由铜片通过导线流向锌片
D.反应一段时间后,溶液的酸性减弱
难度: 简单查看答案及解析
-
决定化学反应速率的主要因素是:
A.催化剂 B.反应物的性质
C.温度 D.压强
难度: 中等查看答案及解析
-
100ml 1mol/L的盐酸跟过量锌片反应,为加快反应速率。又不影响生成氢气的总量,可采用的方法是:( )
A.加入适量的2mol/L的盐酸
B.加入数滴CuSO4溶液
C.加入适量的蒸馏水
D.将反应装置放入冰水中冷却
难度: 中等查看答案及解析
-
下列说法中正确的是
A.C4H10有3种同分异构体
B.相对分子质量相同、结构不同的两种化合物互为同分异构体
C.同分异构体之间的转化是化学变化
D.
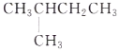 和
和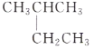 互为同分异构体
互为同分异构体难度: 简单查看答案及解析
 3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算:
3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算: