-
科学家观测到固体催化剂表面“抓取”一氧化碳分子和氧原子配对生成二氧化碳分子的过程。下列关于碳的氧化物的说法正确的是
A.CO与CO2均为酸性氧化物 B.CO是煤气的主要成分之一
C.CO2是弱电解质 D.大量CO2的排放可导致酸雨的形成
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是
A.氟原子的结构示意图:
B.邻硝基甲苯的结构简式:
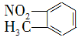
C.质子数为27、中子数为33的Co原子:
Co
D.H2O2的电子式:
难度: 中等查看答案及解析
-
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1Ca(NO3)2溶液中:Na+、NH4+、CO32-、CH3COO-
B.能使甲基橙变红的溶液中:K+、Na+、NO3-、Cl-
C.3%H2O2溶液中:Fe2+、H+、SO42-、Cl-
D.0.1 mol·L-1KSCN溶液中:Fe3+、NH4+、Br-、SO42-
难度: 中等查看答案及解析
-
下列物质性质与应用对应关系正确的是
A.液氨汽化时吸收大量的热,可用作制冷剂
B.硅酸钠溶液呈碱性,可用作木材防火剂
C.NaHCO3能与碱反应,可用作焙制糕点的膨松剂
D.Fe比Cu活泼,可用FeCl3溶液腐蚀线路板上的Cu
难度: 中等查看答案及解析
-
下列实验方法或装置正确的是

A.用图1所示装置制取乙烯
B.用图2所示方法验证HCl气体易溶于水
C.用图3所示方法探究固体表面积对反应速率的影响
D.用图4所示方法检验溴乙烷与NaOH醇溶液共热产生乙烯
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol·L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA
B.标准状况下,11.2 L CCl4中含有的分子数目为0.5NA
C.28 g聚乙烯中含有的碳原子数目为2NA
D.1 mol CH3+中含有的电子数目为11NA
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是
A.向FeCl3溶液中滴加HI溶液:Fe3++2I-===Fe2++I2
B.向AlCl3溶液中加入过量的氨水:Al3++4NH3·H2O===AlO2-+4NH4++2H2O
C.向稀NH4HCO3溶液中加入过量NaOH溶液:NH4++OH-===NH3·H2O
D.向苯酚钠溶液中通入少量CO2:

难度: 中等查看答案及解析
-
X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是
Y
Z
M
W
A.原子半径:W>Y>Z>M>X
B.热稳定性:XM>X2Z,沸点:X2Z>YX3
C.X、Y、Z三种元素形成的化合物中不可能含离子键
D.ZM2、YM3、WM4分子中每个原子最外层均满足8电子结构
难度: 中等查看答案及解析
-
下列各组物质中,物质之间通过一步反应就能实现如图所示变化的是
选项
甲
乙
丙
丁
A
N2
NH3
NO
NO2
B
Na
Na2O
NaOH
Na2O2
C
SiO2
SiF4
H2SiO3
Na2SiO3
D
Al
AlCl3
Al2O3
NaAlO2
难度: 中等查看答案及解析
-
下列图示与对应的叙述相符的
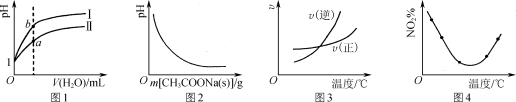
A.图1表示相同温度下,相同体积、pH均为1的盐酸和醋酸溶液分别加水稀释时溶液pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B.图2表示CH3COOH溶液中逐步加CH3COONa固体后,溶液pH的变化
C.图3表示某可逆反应正、逆反应速率随温度变化,则该反应的正反应是吸热反应
D.图4表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:
2NO2(g)
N2O4(g),相同时间后测得NO2体积分数的曲线,则该反应的正反应ΔH<0
难度: 中等查看答案及解析
-
下列说法正确的是
A.SiO2(s)+2C(s)===Si(s)+2CO(g)只能在高温下自发进行,则该反应ΔH>0
B.电镀时,镀层金属跟直流电源的负极相连
C.锅炉内壁上沉积的CaSO4可先用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
D.向100 mL纯水中滴加1 mL浓硫酸,水的离子积常数Kw减小
难度: 中等查看答案及解析
-
某种合成药物中间体X的结构简式如图所示。下列说法正确的是

A.X分子中不存在手性碳原子
B.一定条件下,X可以发生加聚反应
C.1 mol X跟足量浓溴水反应,最多消耗1 mol Br2
D.1 mol X跟足量NaOH溶液反应,最多消耗3 mol NaOH
难度: 中等查看答案及解析
-
在探究SO2性质的实验中,下列说法正确的是
A.SO2气体通入NaOH溶液中,产生倒吸现象,说明SO2极易溶于水
B.SO2气体通入溴水中,溴水的颜色褪去,说明SO2具有漂白性
C.SO2气体通入酸性KMnO4溶液中,溶液的颜色变浅,说明SO2具有还原性
D.SO2气体通入Ba(NO3)2溶液中,溶液出现浑浊现象,说明有BaSO3沉淀生成
难度: 中等查看答案及解析
-
下列溶液中微粒的物质的量浓度关系正确的是
A.常温下0. 1 mol·L-1的下列溶液中:① NH4Al(SO4)2、② NH4Cl、③ CH3COONH4,c(NH4+)由大到小的顺序为②>①>③
B.常温下0.4 mol·L-1CH3COOH溶液和0.2 mol·L-1 NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
C.0.1 mol·L-1 Na2CO3溶液与0.2 mol·L-1 NaHCO3溶液等体积混合所得溶液中:
c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+)
D.0.1 mol·L-1的氨水与0.05 mol·L-1 H2C2O4溶液等体积混合所得溶液中:
c(NH4+)+c(NH3·H2O)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4)
难度: 极难查看答案及解析
-
已知反应O2(g)+2Cl2(g)
2Cl2O(g);ΔH>0。在三个恒温、恒容的密闭容器中分别充入1 mol O2与2 mol Cl2,测得平衡时O2的转化率如下表:
容器编号
温度/℃
容器体积/L
平衡时O2转化率
平衡时压强/Pa
①
200
V1
50%
p1
②
200
V2
70%
p2
③
350
V3
50%
p3
下列说法正确的是
A.起始反应速率:③>①>②
B.平衡时压强:p1<p2
C.容器体积:V1<V3
D.若实验②中O2和Cl2用量均加倍,则平衡时O2的转化率小于70%
难度: 困难查看答案及解析
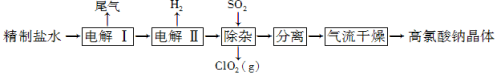
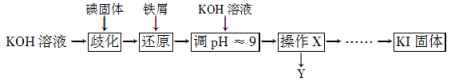

 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: