-
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见 ( )
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为NH4HCO3+HCl→NH4Cl+CO2↑+H2O ΔH=+Q kJ·mol-1
难度: 简单查看答案及解析
-
某短周期元素X,其原子的电子层数为n,最外层电子数为2n+1。下列有关元素X的说法错误的是 ( )
A. 元素X不可能是金属元素
B. 元素X的气态氢化物不一定是电解质
C. 元素X一定能形成化学式为KXO3的含氧酸钾盐
D. 工业上制取X的单质时一定采用氧化还原反应
难度: 中等查看答案及解析
-
下列说法正确的是 ( )
A. ⅠA族元素的金属性比ⅡA族元素的金属性强
B. ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C. 同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D. 第三周期元素的离子半径从左到右逐渐减小
难度: 简单查看答案及解析
-
反应 A+B→C(ΔH<0)分两步进行:①A+B→X (ΔH >0),②X→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
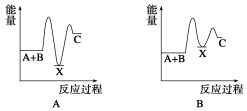

难度: 简单查看答案及解析
-
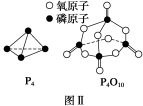
某分子的球棍模型如下图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是( )

A.X原子可能为第ⅤA族元素
B.Y原子一定为第ⅠA族元素
C.该分子中既含有极性共价键又含有非极性共价键
D.从圆球的大小分析,该分子可能为N2F4
难度: 简单查看答案及解析
-
海水中含有氯化镁,从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳,②在引入海水的水渠中加石灰乳,沉降、过滤、洗涤沉淀物,③将沉淀物与盐酸反应,结晶过滤、干燥产物,④将得到的产物熔融后电解。关于提取镁,下列说法不正确的是( )
A.此法的优点之一是原料丰富
B.进行①②③步骤的目的是从海水中提取MgCl2
C.第④步电解时同时会产生氯气
D.以上提取镁的过程中涉及到的反应有分解反应、化合反应和置换反应
难度: 中等查看答案及解析
-
金属材料在日常生活、生产中有着广泛的运用,下列关于金属的说法不正确的是( )
A.越活泼的金属越难冶炼
B.合金的性质与其成分金属的性质不完全相同
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.工业上金属Mg、Al都是用电解其熔融的氯化物制得的
难度: 中等查看答案及解析
-
某二元酸(H2A)在水中的电离方程式为H2A===H++HA-,HA-
H++A2-(25 ℃时Ka=1.0×10-2),下列有关说法中正确的是( )
A.H2A是弱酸
B.稀释0.1 mol/L H2A溶液,因电离平衡向右移动而导致c(H+)增大
C.在0.1 mol/L的H2A溶液中,c(H+)=0.12 mol/L
D.若0.1 mol/L NaHA溶液中c(H+)=0.02 mol/L,则0.1 mol/L的H2A中c(H+)<0.12 mol/L
难度: 简单查看答案及解析
-
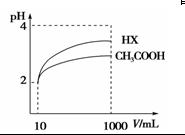
下列事实中,能证实一元酸HR是弱电解质的是( )
A.HR溶液和KCl溶液不发生反应
B.能与水以任意比例互溶
C.0.1 mol·L-1 的HR溶液中c(R- ) =0.01 mol·L-1
D.HR属于共价化合物
难度: 简单查看答案及解析
-
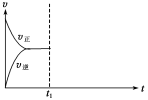
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:
N2(g)+3H2(g)
2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
A.10到15秒内c(NH3) 增加量等于0.25mol •L—1
B.10秒内氨气的平均反应速率为0.025mol•L—1·s—1
C.达平衡后,分离出少量NH3,v正 增大
D.该反应的逆反应的活化能不小于92.2kJ•mol—1
难度: 简单查看答案及解析
-
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: NH2COONH4(s)
2NH3(g)+CO2(g)不能判断该分解反应已经达到化学平衡的是( )
A. v(NH3)正= 2v(CO2)逆 B.密闭容器中总压强不变
C.密闭容器中氨气的体积分数不变 D.密闭容器中混合气体的密度不变
难度: 简单查看答案及解析
-
化学用语是学习化学重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-= Cl2 ↑
B.碱性氢氧燃料电池的负极反应式:O2 + 2H2O + 4e—= 4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e- = Cu2+
D.钢铁发生电化腐蚀的正极反应式:Fe -2e- = Fe2+
难度: 中等查看答案及解析
-
利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是( )
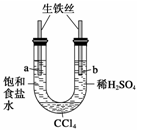
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的pH增大,b处溶液的pH减小
D.a、b两处具有相同的电极反应式:Fe-2e-===Fe2+
难度: 中等查看答案及解析
-
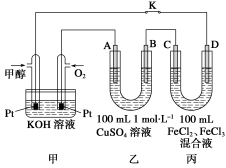
利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,错误的是( )

A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为:Cu2++2e-===Cu
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处时溶液中各离子浓度都不会发生变化
难度: 简单查看答案及解析
-
太阳能光伏发电系统是被称为“21世纪绿色光源”的半导体照明(LED)系统(如图)。已知发出白光的LED是将GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成。下列说法中不正确的是( )
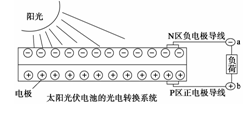
A.光伏发电是将太阳能转变为电能
B.Ga与N在元素周期表中不处于同一主族
C.YAG中钇显+3价
D.上图中N区半导体为负极,P区半导体为正极,电流从a流向b
难度: 困难查看答案及解析
-
今有室温下四种溶液,有关叙述不正确的是( )
①
②
③
④
pH
11
11
3
3
溶液
氨水
氢氧化钠溶液
醋酸
盐酸
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH:①>②>④>③
C.溶液中水的电离程度③>④
D.VaL④溶液与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb=11∶9
难度: 中等查看答案及解析
-
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔)4Na+O2↑+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOHFe3O4+2H2↑+4Na↑。下列有关说法正确的是( )

A.电解熔融氢氧化钠制钠,阳极发生电解反应2OH--2e-===H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数不同
D.目前工业上常用电解熔融氯化钠法制钠(如上图),电解槽中石墨极为阴极,铁为阳极
难度: 困难查看答案及解析
-
锂空气电池放电时的工作原理如图所示。下列叙述正确的( )
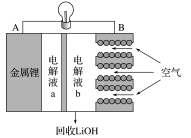
A.放电时Li+由B极向A极移动
B.电池放电反应为4Li+O2 +2H2O===4LiOH
C.正极反应式为O2+4H++4e-===2H2O
D.电解液a可以为LiCl水溶液
难度: 中等查看答案及解析
-
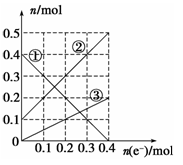
.在密闭容器中,5 mol H2与2 mol CO2发生反应:3H2(g)+CO2(g)
CH3OH(g)+H2O(g)。反应达到平衡时,改变温度(T)和压强(p),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示。下列说法错误的是( )
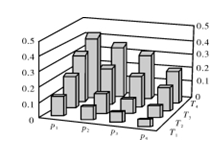
A.P1>P2>P3>P4
B.甲醇的物质的量分数越高,反应的平衡常数越大
C.若T1> T2> T3>T4,则该反应为放热反应
D.缩小容积,可以提高CH3OH在混合物中的质量分数
难度: 中等查看答案及解析
-
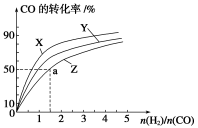
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
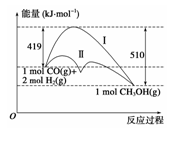
A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH减小
难度: 中等查看答案及解析