-
氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:4Al(s)+3O2(g)=2Al2O3(s)△H1,4Al(s)+2O3(g)=2Al2O3(s)△H2 ,3O2(g)=2O3(g)△H3 则( )
A.△H2-△H1=△H3
B.△H1+△H2=△H3
C.△H1-△H2=△H3
D.△H2+△H1+△H3=0难度: 中等查看答案及解析
-
绿色萤光蛋白(green fluorescent protein),简称GFP,这种蛋白质最早是从一种水母中发现.GFP在蓝色波长范围的光线激发下,会发出绿色萤光.下列关于GFP的推论正确的是( )
A.组成元素包括C、H、O、N、F、Ne
B.在一定条件下可水解生成氨基酸
C.可以通过加聚反应获得
D.滴加AgNO3溶液可使GFP从溶液中析出,再加蒸馏水后析出物又会溶解难度: 中等查看答案及解析
-
NA表示阿伏伽德罗常数,某氯气样品由
分子组成,下列说法正确的是( )
A.0.1mol中有0.2NA个氯原子
B.37g该氯气样品含NA个氯气分子
C.11.2L该氯气样品质量是37g
D.0.1NA个氯气分子溶于水形成1000 mL溶液,溶液中c(Cl-)=0.2mol/L难度: 中等查看答案及解析
-
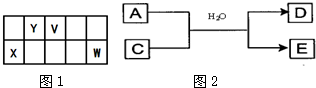
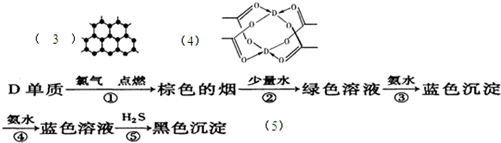
如图所示,集气瓶内充满某混合气体,将滴管内的水挤入集气瓶后,烧杯中的水会进入并充满集气瓶,集气瓶内气体可能是( )
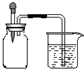
A.O2、NO2
B.H2、O2
C.N2、H2
D.NO2、NO难度: 中等查看答案及解析
-
锂离子电池已经成为应用最广泛的可充电电池.某种锂离子电池的结构示意图:其中两极区间的隔膜只允许Li+通过.电池充电时的总反应化学方程式为:LiC2=Li1-xC2+xLi.关于该电池的推论错误的是( )

A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-=xLi+
C.充电时,负极(C)上锂元素被氧化
D.充电时,有电能转化为化学能难度: 中等查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:NH3•H2O⇌NH4++OH-.往其中加入少量0.01mol•L-1 NaOH溶液,保持不变的是( )
A.c(NH4+)
B.c(OH-)
C.c
D.c(NH4+)•c(OH-)难度: 中等查看答案及解析
-
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图的坐标曲线来表示,下列推论错误的是( )
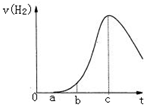
A.t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B.t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低
D.t=c时反应处平衡状态难度: 中等查看答案及解析