-
石墨烯是由碳原子构成具有片状结构的新型纳米材料(结构示意图如下),可通过剥离石墨而成,具有极好的应用前景。下列说法正确的是
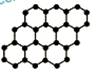
A.石墨烯是一种有机化合物
B.0.0012kg石墨烯中含有0.6mol质子
C.不用其它试剂,利用丁达尔现象即可区分石墨和石墨烯
D.剥离石墨属于物理变化过程
难度: 中等查看答案及解析
-
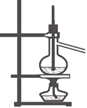
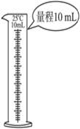
完成下列实验所选择的试剂、装置或仪器(部分夹持装置已略去)正确的是
A B C D
实 验 洗涤沉淀 用酒精提取溴水中的Br2 分离CCl4和苯的混合物 准确量取9.50 mL水
装置或仪器
难度: 中等查看答案及解析
-
在pH=1的溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+ 、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl- D.Ba2+、HCO3-、NO3-、K+
难度: 中等查看答案及解析
-
由以下两种途径制铜:(1)CuO
CuSO4
Cu (2)Zn
H2
Cu 假设每一步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法正确的是
A.消耗等物质的量的Zn、H2SO4、CuO
B.所有反应类型都相同
C.过程中产生的ZnSO4质量相同
D.只有CuO消耗的质量相同
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,NA个分子所占的体积约为22.4 L
B.标准状况下,2.24L CH4和NH3混合气体中含有的电子数目为NA
C.0.1 mol·L-1的K2SO4溶液中阴、阳离子总数为0.3NA
D.标准状况下,22.4L氢气和氦气混合气体中含有的原子总数为2NA
难度: 中等查看答案及解析
-
下列溶液中的氯离子数目与50 mL 1 mol·L-1的AlCl3溶液中氯离子数目相等的是
A.150 mL 1 mol·L-1的KClO3 B.150 mL 3 mol·L-1的KCl
C.75 mL 2 mol·L-1的CaCl2 D.75 mL 2 mol·L-1的NH4Cl
难度: 中等查看答案及解析
-
下列说法中正确的是
A.用苯萃取碘水中的碘时,应先打开上端玻璃塞再将苯层从分液漏斗下口放出
B.用湿润的红色石蕊试纸检验氨气
C.稀释浓硫酸时,应将浓硫酸沿玻璃棒缓慢注入盛水的量筒中
D.用广泛pH试纸测得0.1 mol·L-1 NH4Cl溶液的pH=5.2
难度: 中等查看答案及解析
-
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是
A.将0.1 mol氨气充分溶解在1 L水中
B.将10g 1 mol·L-1的硫酸与90 g水混合
C.将8g三氧化硫溶于水并配成1 L溶液
D.将16g CuSO4·5H2O溶于水并配成1 L溶液
难度: 中等查看答案及解析
-
仅用下表提供的实验器材(规格和数量不限),能完成相应实验的一项是
实验器材(省略夹持装置) 相应实验
A 试管、胶头滴管 用稀盐酸、Na2CO3溶液比较盐酸与碳酸的酸性强弱
B 烧杯、玻璃棒、胶头滴管、滤纸 用盐酸除去硫酸钡中的少量碳酸钡
C 烧杯、玻璃棒、胶头滴管、容量瓶 用固体氯化钠配制0.5mol/L的溶液
D 烧杯、玻璃棒、蒸发皿 硫酸铜溶液的浓缩结晶
难度: 中等查看答案及解析
-
在体积相同的两个密闭容器中分别充满C2H4、C3H6气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A.两种气体的压强相等 B.C2H4比C3H6的质量小
C.两种气体的分子数目相等 D.两种气体所含的原子数目相等
难度: 中等查看答案及解析
-
某同学在实验室中进行如下实验:
编号
I
II
III
实验



现象
没有明显变化,溶液仍为无色
有白色沉淀生成,溶液为蓝色
有无色气体放出
以下结论正确的是
A.I中混合前后溶液中各离子种类、个数均不变
B.II中反应前后溶液中Cu2+ 、Cl-浓度均未变
C.II中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同
D.III中发生的反应属于置换反应,不属于离子反应
难度: 中等查看答案及解析
-
在标准状况下有:①6.72 L CH4;②3.01×1023个氯化氢分子;③13.6 g硫化氢;④0.2 mol氨气。四种气体中含有的氢原子数大小顺序为
A.①>③>④>② B.②>③>④>①
C.①>④>②>③ D.②>③>①>④
难度: 中等查看答案及解析
-
离子方程式BaCO3+2H+== CO2↑+H2O+ Ba2+中的H+不能代表的物质是
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A.⑤ B.④⑤ C.②③⑤ D.②④⑤
难度: 中等查看答案及解析
-
合成氨工业生产中所用的α—Fe催化剂的成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时混合物中铁的质量分数约为
A.70.0% B.77.8% C.72.4% D.75.0%
难度: 中等查看答案及解析
-
有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验,从实验可以判断:
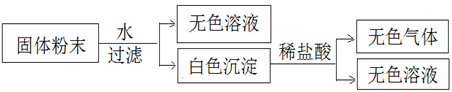
A.该固体粉末中一定不含有BaCl2
B.该固体粉末中一定含有KNO3
C.它的组成可能是CaCO3、BaCl2、CuSO4
D.它的组成一定是CaCO3、Na2SO4、KNO3
难度: 中等查看答案及解析
-
有一定体积CH4、C2H6、C3H8组成的混合气体,是同温同压下H2密度的15倍。则混合气体中CH4、C2H6、C3H8的体积比不可能是:
A.2∶1∶2 B.2∶3∶1 C.1∶4∶1 D.5∶3∶5
难度: 中等查看答案及解析
-
实验中常用Na2CO3溶液、NaOH溶液、BaCl2溶液作为除杂试剂除去粗盐中含有的泥沙、Ca2+、Mg2+、Fe3+、SO42-等杂质。下列除杂试剂添加顺序不合理的是
A. NaOH溶液→BaCl2溶液→Na2CO3溶液
B. BaCl2溶液→NaOH溶液→Na2CO3溶液
C. BaCl2溶液→Na2CO3溶液→NaOH溶液
D. Na2CO3溶液→BaCl2溶液→NaOH溶液
难度: 中等查看答案及解析
-
20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是
A.20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0 mol·L-1
B.20℃时,将29.8 gKCl溶于87.6 g水中可得饱和溶液
C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变
难度: 中等查看答案及解析
-
有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子(不考虑难溶物自身的溶解),同时生成一种阴、阳离子个数比为1:1的白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是________.
A.Na+ B.Mg2+ C.Cu2+ D.Ag+
(2)三种正盐的化学式分别是:A________,B________,C________
(3) A、B、C同时溶于水时反应的离子方程式为________
难度: 中等查看答案及解析
