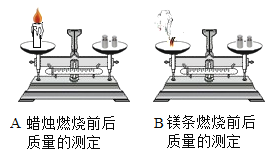
-
生活中“低钠盐”“高钙奶”中的“钠”和“钙”是指
A. 元素 B. 单质 C. 原子 D. 分子
难度: 简单查看答案及解析
-
通过下列操作和现象,得出的结论可靠的是
A. 测量蜡烛燃烧后的长度,发现明显短于燃烧前,说明蜡烛发生了化学变化
B. 用湿润的烧杯罩在火焰上方,观察到烧杯壁上有液滴,说明蜡烛燃烧时有水产生
C. 用涂有澄清石灰水的烧杯罩住蜡烛熄灭时产生的白烟,发现石灰水变浑浊,说明白烟是二氧化碳
D. 点燃两支相同的蜡烛,用烧杯将其中一支罩在桌面上,一段时间后烧杯中的蜡烛熄灭,另一支继续燃烧,说明空气中有物质参与了燃烧
难度: 中等查看答案及解析
-
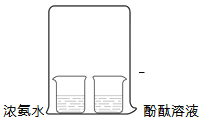
王安石用“遥知不是雪,为有暗香来”描写梅花,能从远处闻到花香的原因是
A. 分子质量很小 B. 分子在不断运动
C. 分子间有间隔 D. 分子由原子构成
难度: 简单查看答案及解析
-
钠原子的原子核内有11个质子和12个中子,该原子的核外电子数为
A. 1 B. 23 C. 11 D. 12
难度: 简单查看答案及解析
-
下列操作或措施符合实验安全的是
A. 加热时试管口对着他人
B. 用嘴吹灭酒精灯
C. 酒精洒在桌上燃烧时,立即用湿抹布扑盖
D. 用水冷却加热后的试管
难度: 中等查看答案及解析
-
人类认识化学经历了漫长的过程。下列物质的出现过程正确的顺序是
①火 ②青铜器 ③火药 ④纳米材料
A. ①②③④ B. ①③②④ C. ②③④① D. ④③②①
难度: 简单查看答案及解析
-
空气是宝贵的自然资源,空气中体积分数约占21%的是
A.稀有气体 B.氮气 C.二氧化碳 D.氧气
难度: 简单查看答案及解析
-
给试管里的物质加热时,切忌将试管底部接触灯芯的原因是
A. 易使试管底部熔化
B. 会使酒精燃烧不充分
C. 会使酒精灯熄灭
D. 灯芯处温度低,易使热的试管骤冷而破裂
难度: 简单查看答案及解析
-
下列反应属于化合反应的是( )
A. 氧化汞
汞+氧气 B. 氢气+氧化铜
铜+水
C. 乙醇+氧气
水+二氧化碳 D. 碳+氧气
二氧化碳
难度: 简单查看答案及解析
-
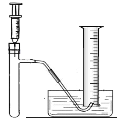
下列实验操作中,正确的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列物质中,属于化合物的是
A. 空气 B. 氧气 C. 矿泉水 D. 四氧化三铁
难度: 中等查看答案及解析
-
下列符号能表示2个氧分子的是
A. 2O2 B. O2 C. 2O D. 2O2-
难度: 中等查看答案及解析
-
下列物质的用途中,主要利用其物理性质的是
A. 氢气用于填充气球 B. 红磷燃烧测空气中氧气含量
C. 氮气用于食品防腐 D. 氧气供给呼吸
难度: 中等查看答案及解析
-
下列元素符号书写正确的是
A. 锰Mn B. 钠NA C. 钙Cu D. 铝AL
难度: 简单查看答案及解析
-
下列物质的化学式书写不正确的是
A. 氧气O2 B. 二氧化硫SO2 C. 氧化铁FeO D. 氯化钠NaCl
难度: 中等查看答案及解析
-
铬在元素周期表中信息如图所示,下列有关铬元素的说法正确的是
A. 原子序数是24 B. 属于非金属元素
C. 一个铬原子核外有28个电子 D. 相对原子质量为52.00g
难度: 简单查看答案及解析
-
下列方法能区分氮气和二氧化碳两瓶气体的是
A. 闻气味 B. 观察颜色
C. 倒入适量澄清的石灰水 D. 将燃着的木条伸入集气瓶中
难度: 简单查看答案及解析
-
空气中氧气含量测定的实验装置如右图所示。下列有关说法正确的是
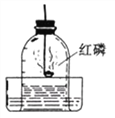
A. 燃烧匙中的红磷可以换成硫或木炭
B. 燃烧匙中的红磷越多,水位上升越高
C. 选用过量的红磷是因为反应可以耗尽O2,生成固态的P2O5
D. 本实验可以证明空气中含有N2、O2、CO2和稀有气体
难度: 中等查看答案及解析
-
如图为尿素【CO(NH2)2】中各元素质量分数的示意图,其中表示氮元素质量分数的是( )
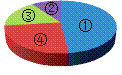
A. ① B. ② C. ③ D. ④
难度: 中等查看答案及解析
-
观察蜡烛燃烧过程中的变化,下列说法不正确的是
A. 蜡烛燃烧的过程中,既有物理变化也有化学变化
B. 蜡烛燃烧的过程中,既有物质变化也有能量变化
C. 燃烧后的气体使澄清石灰水变浑浊,发生的是化学变化
D. 燃烧后的气体在干燥烧杯壁上冷凝成液滴时,发生的是化学变化
难度: 困难查看答案及解析
-
下列关于实验操作和目的的说法中,不正确的是
A. 用小刀切割蜡烛,以研究石蜡的硬度
B. 将石蜡放入水中,研究石蜡的密度,以及能否溶于水
C. 用火柴去点蜡烛刚熄灭时产生的白烟,以研究白烟能否燃烧
D. 将火柴梗迅速平放入火焰中(如下图所示)约1秒后取出,以研究火柴梗能否燃烧
难度: 困难查看答案及解析
-
进一步对蜡烛燃烧进行探究,下列推断中不合理的是
A. 单独点燃制作烛芯用的棉线,棉线很快燃尽,说明蜡烛燃烧时不仅是棉线在燃烧
B. 固态石蜡很难被点燃,说明燃烧可能需要一定的条件
C. 由于空气几乎不含碳元素,澄清石灰水变浑浊说明碳元素来自石蜡
D. 石蜡燃烧生成水和二氧化碳,说明石蜡中一定含有碳、氢、氧三种元素
难度: 中等查看答案及解析
-
下图为载人航天器工作仓中气体成分的微观示意图,已知在同温同压下,气体的体积之比等于分子个数之比,下列说法不合理的是
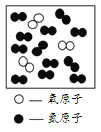
A. 1个氧分子是由2个氧原子构成的
B. 氧分子和氮分子能均匀混合,是因为航天器处于失重状态
C. 航天器工作仓内氮气与氧气的体积比与地表空气接近
D. 航天器工作仓中充氮气可避免发生火灾后燃烧过于剧烈
难度: 中等查看答案及解析