-
分类法是化学研究的重要方法。以下分类不正确的是
A. 合金:生铁、青铜、硬铝 B. 氧化物: 水、二氧化锰、五氧化二磷
C. 碱: 纯碱、生石灰、苛性钠 D. 合成材料:塑料、合成橡胶、合成纤维
难度: 简单查看答案及解析
-
下列图标中,属于中国国家节能标志的是( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
空气是人类宝贵的自然资源,下列有关空气成分的说法错误的是( )
A. 液氮可以做制冷剂 B. 氧气可以做火箭发射的燃料
C. 稀有气体可制成多种用途的电光源 D. 二氧化碳是植物光合作用必须的物质
难度: 简单查看答案及解析
-
下列实验操作正确的是 ( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关的化学用语表达正确的是( )
A. 五个氢原子:H5 B. 三个水分子:3H2O
C. 四个钙离子:2Ca+2 D. 四个铵离子:4NH3+
难度: 中等查看答案及解析
-
大蒜中含有的一种有效成分“硫化丙烯”(C3H6S)具有一定的杀菌食疗作用。下列有关硫化丙烯的说法正确的是( )
A. 硫化丙烯的相对分子质量为74 B. 硫化丙烯分子中碳、氢、硫元素质量比为3:6:1
C. 硫化丙烯中硫元素质量分数最大 D. 硫化丙烯是由3个碳原子、6个氢原子和1个硫原子构成
难度: 中等查看答案及解析
-
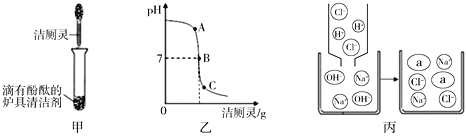
A 和 B 反应生成 C 和 D 的微观示意图如图所示:
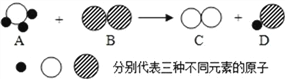
则下列说法正确的是 ( )
A. 该化学反应属于置换反应
B. 恰好完全反应时,反应前后各原子种类不变,数目减少
C. 反应前后三种元素的化合价都没有改变
D. 恰好完全反应时 A 与 B 两物质的化学计量数之比为 1:1
难度: 中等查看答案及解析
-
下列依据实验目的所设计的实验方案中,正确的是( )
选项
实验目的
实验方案
A
除去NaCl溶液中的Na2CO3
加适量稀硫酸
B
除去CaO中的CaCO3
加水溶解,过滤
C
除去CO2中的HCl气体
将混合气体通入NaOH溶液
D
除去KNO3溶液中的KCl
加适量的AgNO3溶液,过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列图象正确的是( )
A.
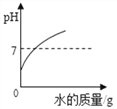 稀释浓硫酸
稀释浓硫酸B.
 电解水一段时间
电解水一段时间C.
 等质量的 Mg 和 Fe 与足量同浓度稀盐酸反应
等质量的 Mg 和 Fe 与足量同浓度稀盐酸反应D.
 浓盐酸露置空气中
浓盐酸露置空气中难度: 困难查看答案及解析