-
下列说法错误的是
A. “臭氧空洞”的形成可能与含氯的氟代烷的使用有关
B. 钢铁在干燥的环境中更容易发生“吸氧腐蚀”
C. 在船身上装有锌块,是利用了牺牲阳极的阴极保护法保护船体
D. 石油的裂解和裂化可以得到气态烯烃
难度: 中等查看答案及解析
-
下列关于有机物命名不正确的是
A.
对二甲苯
B. 2,3-二甲基-3-乙基戊烷
C.
异丁烯
D. (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷
难度: 中等查看答案及解析
-
关于有机物,下列说法正确的是
A.
含有3种官能团
B. 己烷有4种同分异构体
C.
和
分子组成相差一个-CH2-,因此是同系物关系
D. 烷烃的沸点随着碳原子数目的增多而增大
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 乙烯与苯都能发生加成反应,所以都能使溴水褪色
B. 对氯甲苯可以发生氧化反应、取代反应、消去反应
C. 可以用重结晶的方法提纯苯甲酸
D. 检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色
难度: 中等查看答案及解析
-
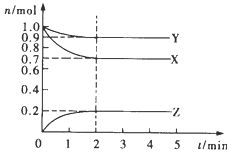
某可逆反应正向反应过程中能量变化如图,下列说法正确的是

A. 该反应为吸热反应
B. 加入催化剂,反应速率增大,E1减小,E2减小,反应热不变
C. 增大压强,平衡正向移动,K增大
D. 当反应υ正(B)∶υ正(D)=2∶1时,到达平衡状态
难度: 中等查看答案及解析
-
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是
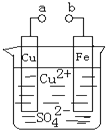
A. a 和 b 不连接时,铁片上会有金属铜析出
B. 无论 a 和 b 是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
C. a 和 b 分别连接直流电源正、负极,铜片上发生的反应为:Cu-2e-=Cu2+
D. a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
难度: 中等查看答案及解析
-
室温下,将1.000 mol/L盐酸滴入20.00 mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是
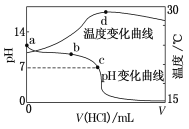
A. a点由水电离出的c(H+)=1.0×10-14 mol/L
B. b点:c(NH4+)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)=c(NH4+)
D. d点前,溶液温度上升的主要原因是NH3·H2O电离放热
难度: 中等查看答案及解析