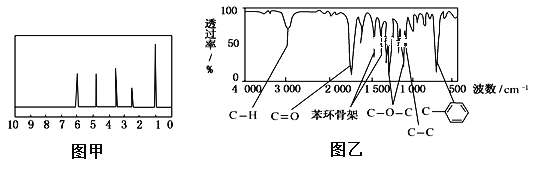
-
下列叙述正确的是( )
A. 使用催化剂能够降低化学反应的反应热(△H)
B. 金属发生吸氧腐蚀时,被腐蚀的速率和氧气浓度无关
C. 原电池中发生的反应达平衡时,该电池仍有电流产生
D. 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小
难度: 简单查看答案及解析
-
分子式为C8H11N的有机物,分子内含有苯环和氨基(—NH2)的同分异构体共有 ( )
A. 13种 B. 12种 C. 14种 D. 9种
难度: 困难查看答案及解析
-
将有机物完全燃烧,生成CO2和H2O。将12 g 该有机物的完全燃烧产物通过浓H2SO4,浓H2SO4增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O C. C3H8O D. C3H8
难度: 中等查看答案及解析
-
X、Y、Z、M、N代表五种金属。有以下化学反应:
①水溶液中:X+Y2+===X2++Y
②Z+2H2O(冷)===Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M-2e-===M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
A. M<N<Y<X<Z B. N<M<X<Y<Z C. N<M<Y<X<Z D. X<Z<N<M<Y
难度: 简单查看答案及解析
-
化学反应中通常伴随着能量变化,下列说法中错误的是( )
A. 二次电池放电时将电能转化为化学能 B. 原电池将化学能转化为电能
C. 煤燃烧时并不能将化学能全部转化为热能 D. 镁条燃烧时将部分化学能转化为光能
难度: 简单查看答案及解析
-
下列有关电化学的说法正确的是( )
A. 铜锌原电池工作时外电路电子由锌极流向铜极,内电路电子由铜极流向锌极
B. 电解精炼铜时阴极发生还原反应
C. 用铜作电极电解后的硫酸铜溶液中,加入一定量的氧化铜即可恢复溶液的成分和浓度
D. 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
难度: 中等查看答案及解析
-
铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
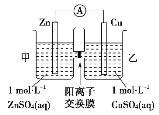
A. 锌电极上发生的反应:Zn2++2e-===Zn
B. 电池工作一段时间后,甲池的c(SO
)减小
C. 电流由锌电极经电流表流向铜电极
D. 电池工作一段时间后,乙池溶液的总质量增加
难度: 中等查看答案及解析
-
有一种新型的乙醇电池,它用磺酸类质子溶剂,在200 ℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为C2H5OH+3O2===2CO2+3H2O,电池示意如图,下列说法不正确的是( )
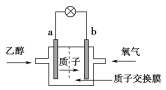
A. a极为电池的负极
B. 电池工作时,电流由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为4H++O2+4e-===2H2O
D. 电池工作时,1 mol乙醇被氧化时就有6 mol电子转移
难度: 中等查看答案及解析
-
如图是四种燃料电池的工作原理示意图,其中正极反应生成水的是
A. 固体氧化物燃料电池
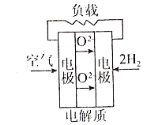
B. 碱性氢氧化物燃料电池
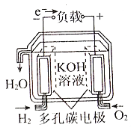
C. 质子交换膜燃料电池
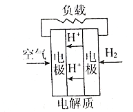
D. 熔融盐燃料电池
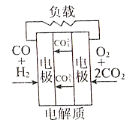
难度: 中等查看答案及解析
-
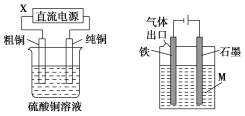
将图Ⅰ所示装置通电10 min后,撤掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左侧铁电极表面析出了白色胶状物质,U形管右侧液面上升。下列说法正确的是( )

A. 同温同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多
B. 装置Ⅱ中铁电极的电极反应式为Fe-2e-+2OH-===Fe(OH)2↓
C. 装置Ⅱ中石墨电极的电极反应式为2H++2e-===H2↑
D. 装置Ⅰ通电10 min后,铁电极附近溶液的pH降低
难度: 中等查看答案及解析
-
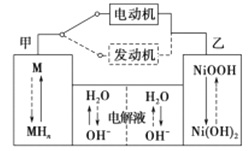
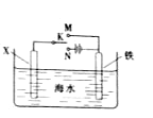
下列有关电化学装置的说法正确的是( )
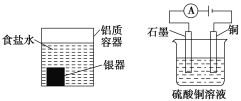
图a 图b 图c 图d
A. 利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-===2Ag+S2-
B. 图b装置电解一段时间后,铜电极溶解,石墨电极上有亮红色物质析出
C. 图c装置中的X若为直流电源的负极,则该装置可实现粗铜的精炼
D. 若图d装置中的M为海水,则该装置可通过“牺牲阳极的阴极保护法”使铁不被腐蚀
难度: 中等查看答案及解析
-
下列叙述正确的是( )

A. 如图1所示将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO
)为0.5 mol/L
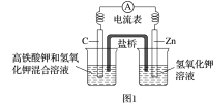
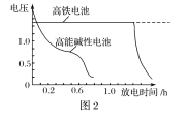
B. 如图2所示的装置中发生Cu+2Fe3+===Cu2++2Fe2+的反应,X极是负极,Y极的材料可以是铜
C. Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应
D. 如图3所示当有0.1 mol电子转移时,有0.1 mol Cu2O生成
难度: 中等查看答案及解析
-
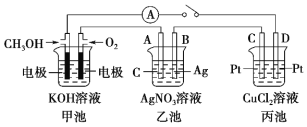
用电解乙二醛制备乙二酸(HOOC-COOH)的装置如图所示,通电后,Pt2电极上产生的氯气将乙二醛氧化为乙二酸,下列说法正确的是
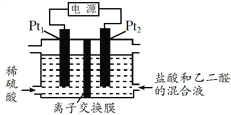
A. Pt2接电源的负极,发生还原反应
B. 盐酸的作用是提供Cl-和增强导电性
C. 电路上每转移1mol电子产生45g乙二酸
D. Pt1极上的电极反应为:2H2O-4e-=== O2↑ + 4H+
难度: 中等查看答案及解析
-
下列化学用语正确的是( )
A. 乙酸根离子的结构式:
B. CO2的球棍模型:
C. 3甲基1丁烯的结构简式:(CH3)2CHCH===CH2 D. 醛基的电子式:
难度: 中等查看答案及解析
-
对下列各组物质关系的描述中不正确的是
A. O2和O3互为同素异形体 B. CH2=CH2和环丁烷互为同系物
C.
、
和
互为同位素 D.
和
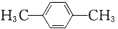 互为同分异构体
互为同分异构体难度: 中等查看答案及解析
-
下列物质中,互为同分异构体的是
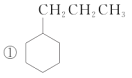
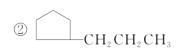
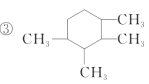
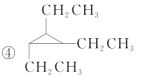
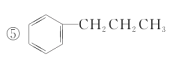
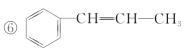
A. ①② B. ①④ C. ①⑤ D. ①③④
难度: 简单查看答案及解析
-
某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个—CH3、两个—CH2—、一个
和一个—Cl,它的可能的结构有几种
A. 4 B. 5 C. 6 D. 7
难度: 中等查看答案及解析
-
有机物的种类繁多,但其命名是有规则的。下列有机物命名正确的是( )
A. CH2=CH-CH=CH2 1,3—二丁烯 B.
3-丁醇
C.
甲基苯酚 D.
2—甲基丁烷
难度: 中等查看答案及解析
-
关于有机物
的下列叙述中,正确的是 ( )
A. 它的系统名称是2,4二甲基4戊烯
B. 它的分子中最多有5个碳原子在同一平面上
C. 它与甲基环己烷互为同分异构体
D. 该有机物的一氯取代产物共有4种
难度: 中等查看答案及解析
-
萜品油烯(D)可用作香料的原料,它可由A合成得到如下所示,下列说法正确的是 ( )
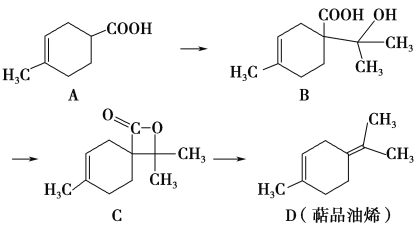
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 1 mol有机物A中含有1.204×1024个双键
D. 有机物C的同分异构体中不可能有芳香化合物
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是( )
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32−+CaSO4
CaCO3+SO42−
B. 酸化NaIO3和NaI的混合溶液:I− +IO3−+6H+=I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3=2FeO42−+3Cl−+4H++H2O
D. 电解饱和食盐水:2Cl−+2H+
Cl2↑+ H2↑
难度: 中等查看答案及解析
-
下列装置能达到相应实验目的的是( )
A.
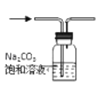 除去CO2中的HCl
除去CO2中的HClB.
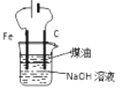 制备Fe(OH)2并能较长时间观察其颜色
制备Fe(OH)2并能较长时间观察其颜色C.
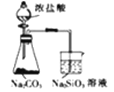 验证碳酸的酸性强于硅酸
验证碳酸的酸性强于硅酸D.
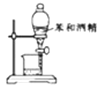 分离苯和酒精
分离苯和酒精难度: 困难查看答案及解析


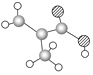
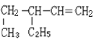 的名称(系统命名)________
的名称(系统命名)________