-
下列叙述正确的是( )

A. 如图1所示将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO )为0.5 mol/L
)为0.5 mol/L
B. 如图2所示的装置中发生Cu+2Fe3+===Cu2++2Fe2+的反应,X极是负极,Y极的材料可以是铜
C. Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应
D. 如图3所示当有0.1 mol电子转移时,有0.1 mol Cu2O生成
-
(14分)金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解。
(1)写出铜溶于上述混合溶液的离子方程式 。
(2)若在如图Ⅰ所示的装置中发生(1)中的反应,
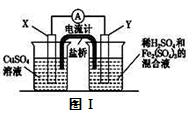
则X极是 (“正极”或“负极”),电极反应式是
(3)铜完全溶解时,所得溶液中Fe3+、Cu2+、H+三种阳离子的浓度均为0.2 mol/L(假设溶液体积不变),若用电解方法回收铜,装置如图Ⅱ所示。
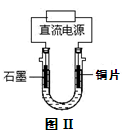
①电解开始阶段,阳极的电极反应式为 ,阴极的电极反应式为 。
②判断溶液中的Cu2+已完全析出的现象是 。当Cu2+恰好完全析出时,转移电子的物质的量 。
-
金属铜不溶于稀硫酸,但可溶于铁盐溶液。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)。
(1)写出铜溶解于上述混合溶液的离子方程式_______________________________________。
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是_________g,溶液中的c(SO42—)=__________mol/L。
(3)若欲在如图所示的装置中发生(1)中的反应,则:X极是________(正、负极),电极反应式________。Y极的材料是,电极反应式________。
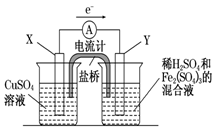
-
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)
(1)写出铜溶解于上述混合液的离子方程式____________________________.
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是______g,溶液中的c(SO)=______mol/L.
(3)若欲在如图所示的装置中发生(1)中的反应,请判断图中的正、负极,并选出适当的物质作电极,写出电极反应式,填在相应的表格中.
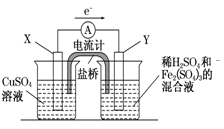
-
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )
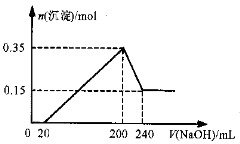
A.Mg和Al的总质量为8g
B.硫酸的物质的量浓度为5 mol/L
C.生成的H2在标准状况下的体积为11.2L
D.NaOH溶液的物质的量浓度为5mol/L
-
将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是( )
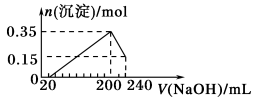
A.Mg和Al的总质量为8 g
B.原稀硫酸溶液的物质的量浓度为5 mol·L-1
C.生成的H2在标准状况下的体积为11.2 L
D.NaOH溶液的物质的量浓度为5 mol·L-1
-
室温下将一定量铜粉加入到l00mL#硫酸和硫酸铁混合溶液中,铜粉完全溶解,不考虑盐的水解和溶液体积变化,所得溶液中Fe3+、Cu2+、H+的物质的量浓度相同。此时溶液的pH=l,则溶液中c(SO42-)为
A. 0.2 mol•L-1 B. 0.3 mol•L-1 C. 0.4 mol•L-1 D. 0.5 mol•L-1
-
将5.6g铁粉投入100mL2mol/L的稀硫酸中,2min时铁刚好完全溶解(忽略溶液体积变化)。下列有关这个反应的反应速率表示正确的是( )
A.铁的反应速率为0.5mol/(L·min) B.硫酸 的反应速率为0.5mol/(L·min)
C.硫酸亚铁的反应速率为0.5mol/(L·min)D. 氢气的反应速率为0.5mol/(L·min)
-
下列有关实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.铜—锌—稀硫酸形成的原电池中,铜为正极
C.把铜片插入氯化铁溶液中,加入几滴氯化铜溶液,气泡放出的速率加大
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出的速率加大
-
取一定量的镁、铝混合粉末,加入1mol/L的硫酸300mL,使之完全溶解 (酸过量);再加入过量的未知浓度的KOH溶液200mL,得到 5.8g沉淀;过滤后向滤液中加入2mol/L盐酸100mL,恰好沉淀完全;将沉淀滤出,洗涤、干燥,称量为7.8g.求:
(1)原来混合物中镁和铝的质量分数;
(2)所用KOH的物质的量浓度.

)为0.5 mol/L





