-
下列有关化学药品的使用正确的是( )
A. 固体药品应盛放在细口瓶中
B. 将鼻孔凑到集气瓶口闻气体的气味
C. 给试管内液体加热,液体量不超过试管容积的三分之二
D. 一般用药匙或镊子取用固体药品
难度: 简单查看答案及解析
-
实验室配制1 mol•L-1盐酸250mL,下列不需用的仪器是( )
A. 250mL容量瓶 B. 托盘天平 C. 胶头滴管 D. 烧杯
难度: 简单查看答案及解析
-
某混合物的水溶液,只可能含有以下离子中的若干:NH4+、Cl﹣、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol;
③第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥,沉淀质量2.33g。
根据上述实验,以下推测正确的是( )
A. K+一定不存在 B. 该溶液中含CO32-的浓度为0.1 mol·L-1
C. Cl﹣可能存在 D. Ba2+一定不存在,Mg2+可能存在
难度: 中等查看答案及解析
-
下列有关胶体的说法不正确的是( )
A. 分散系中分散质粒子的大小:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
B. FeCl3溶液和Fe(OH)3胶体都能透过滤纸
C. 当一束强可见光通过Fe(OH)3胶体时会出现光亮的“通路”
D. 将饱和FeCl3溶液滴入NaOH溶液中可制得Fe(OH)3胶体
难度: 简单查看答案及解析
-
实验室制取氧气的试管壁上黏附有少量MnO2,除去黏附的MnO2可选用的试剂是
A. 蒸馏水 B. KOH溶液 C. 稀盐酸 D. 浓盐酸
难度: 简单查看答案及解析
-
下列现象不能用于检验NH3的是
A、气体遇浓盐酸产生白烟
B、气体使湿润的蓝色石蕊试纸变红
C、气体通人酚酞溶液中,溶液变红
D、气体使湿润的红色石蕊试纸变蓝
难度: 中等查看答案及解析
-
1mol氢氧化亚铁在空气中变质,理论上需要标准状况下的空气(假设氧气占空气体积的1/5)( )
A. 5.6L B. 22.4L C. 28L D. 2.8L
难度: 简单查看答案及解析
-
碳化硅又称金刚砂(SiC),它的分解温度很高(约2200℃),硬度极大,溶解性很差,性质很稳定。由此推断,下列物质中可能与它有相似结构的是( )
A. 晶体硅 B. 硅酸 C. 干冰 D. 水玻璃
难度: 简单查看答案及解析
-
对于溶液的溶质质量分数的概念叙述正确的是( )
A. 一定质量溶液里所含溶质的质量 B. 溶液中溶质质量与溶液质量之比
C. 1L溶液里所含溶质的质量 D. 100g溶剂里所含溶质的质量
难度: 简单查看答案及解析
-
下列关于钠单质性质的叙述中不正确的是( )
A. 在空气中极易被氧化,常保存在煤油中
B. 是一种银白色金属,具有金属光泽
C. 能与氯化铜溶液反应生成氯化钠和铜
D. 在空气中燃烧火焰为黄色
难度: 简单查看答案及解析
-
由钠、镁、铝、锌四种金属单质中的两种组成的合金共12g,跟足量的盐酸反应产生5.6L氢气(标准状况),那么此合金中一定含有的金属是( )
A. Na B. Mg C. Al D. Zn
难度: 中等查看答案及解析
-
在使用分液漏斗进行分液时,正确的操作是( )
A. 上层液体经漏斗下口放出
B. 分离液体时,将漏斗拿在手上进行分离
C. 分离液体时,使分液漏斗口上的小孔与大气相通,打开活塞
D. 分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出
难度: 简单查看答案及解析
-
联合国世界卫生组织经过严密的科学分析,认为我国的铁锅是最理想的炊具,并向全世界大力推广,其主要原因是( )
A. 铁锅价格便宜 B. 铸铁锅的铁熔点高
C. 使用铁锅烹饪的食物中留有铁元素 D. 铁锅含有有机物必含的碳元素
难度: 简单查看答案及解析
-
下列有关电解质的说法正确的是( )
A. 氢氧化钠溶液能导电,所以它是电解质
B. 电解质在熔融状态下都能导电
C. 水溶液能导电的化合物不一定是电解质
D. 难溶物质肯定不是电解质
难度: 中等查看答案及解析
-
下列说法中不正确的是( )
A. 普通干电池工作时将化学能转化为电能
B. 锌锰干电池中,锌电极是负极
C. 锌锰干电池属于一次电池
D. 锌锰干电池中,锌电极发生还原反应
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 34S原子核内的中子数为16 B. 1H和2H的化学性质相同
C. H
O与H
O互为同素异形体 D. Na和Na+属于同种元素,且性质相同
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 碱金属与氧气化合生成的产物都属于碱性氧化物
B. 碱金属都能与水发生置换反应生成强碱和氢气
C. 碱金属锂、钠、钾都可以保存在煤油中
D. 碱金属铷的密度比钾大,熔点比钾高
难度: 中等查看答案及解析
-
下列各组物质中,键的类型不同的是( )
A. HCl和HNO3 B. H2O和NH3 C. Na2S和NaCl D. CCl4和Na2O
难度: 中等查看答案及解析
-
如图所示能够组成原电池,并且产生明显的电流的是( )
A.
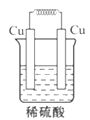 B.
B. 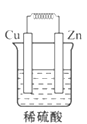 C.
C. 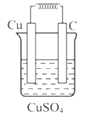 D.
D. 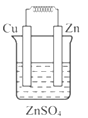
难度: 中等查看答案及解析
-
化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
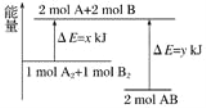
A. 该反应是吸收能量的反应
B. 1molA—A键和1 molB—B键断裂能放出xkJ的能量
C. 2molA—B键断裂需要吸收ykJ的能量
D. 2molAB的总能量高于1molA2和1molB2的总能量
难度: 中等查看答案及解析
-
近年来,科学家新研制的一种酸性乙醇电池(用磺酸类质子作溶剂),比甲醇电池效率高出32倍,电池反应式为C2H5OH+3O2=== 2CO2+3H2O,电池构造如下图所示:
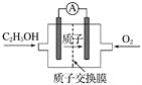
下列关于该电池的说法不正确的是( )
A. 通入乙醇的一极为负极
B. 正极反应式为4H++O2+4e-===2H2O
C. 负极反应式为C2H5OH-12e-+3H2O===2CO2+12H+
D. 随着反应的进行,溶液的酸性保持不变
难度: 中等查看答案及解析
-
下列各组物质的性质及粒子的性质变化正确的是( )
A. 稳定性H2S>HCl>HBr>HI B. 还原性Na+>S2->Br->Cl-
C. 微粒半径Cl->K+>S2->S D. 酸性HClO4>H2SO4>H2CO3>HClO
难度: 中等查看答案及解析
-
下列化学方程式或离子方程式书写有误的是( )
A. Cl2+2I-===I2+2CI- B. I2+2Br-===Br2+2I-
C. Cl2+2Br-===Br2+2Cl- D. Br2+H2O===HBr+HBrO
难度: 中等查看答案及解析