-
下列反应的离子方程式书写正确的是
A. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
B. FeCl2溶液与Cl2反应:Fe2++Cl2=Fe3++2Cl-
C. Cu(OH)2与稀HNO3反应:Cu(OH)2 + 2H+= Cu2+ +2H2O
D. CaCO3与CH3COOH反应:CaCO3+2H+ = Ca2+ +CO2↑+H2O
难度: 简单查看答案及解析
-
利用辉铜矿冶炼铜时发生的主要反应为Cu2S+O2
2Cu+SO2,下列有关该反应的说法正确的是
A. 硫元素被氧化 B. O2发生了氧化反应
C. Cu2S仅作还原剂 D. 反应中Cu元素无电子转移
难度: 中等查看答案及解析
-
下列有机反应不属于取代反应的是
A. CH4 +Cl2
CH3Cl + HCl
B. HC≡CH + HCl
H2C=CHCl
C.
D.
难度: 中等查看答案及解析
-
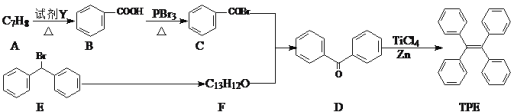
《科学美国人》评近三年十大创新技术之一是碳呼吸电池,电池装置如下图所示,下列说法正确的是
A. 金属铝作正极 B. 负极发生了还原反应
C. 利用该技术可捕捉大气中的CO2 D. 该电池工作时电能转变为化学能
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 常温常压下,1 mol CH4的体积是22.4 L
B. 0.1 mol Fe与Cl2完全反应失去电子数为0.2NA
C. 用激光笔照射可鉴别Fe(OH)3胶体和FeCl3溶液
D. SO2能使品红溶液褪色,说明SO2有氧化性
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W的原子序数依次增大,X是原子半径最小的元素,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍。下列叙述不正确的是( )
A. 原子半径的大小顺序:r(Z)>r(W)>r(Y)>r(X)
B. Y的气态氢化物的热稳定性比W的弱
C. X、Y两种元素可形成化合物X2Y、X2Y2
D. Z、W两种元素最高价氧化物对应的水化物之间能发生反应
难度: 中等查看答案及解析
-
为探究某铜的硫化物组成,取一定量硫化物在氧气中充分灼烧,将生成的气体全部通入盛有足量的H2O2和BaCl2的混合液中,得到白色沉淀 4.66 g;将灼烧后的固体(仅含铜与氧2种元素)完全溶于100 ml 1 mol/L H2SO4中,过滤,得到0.64 g 红色固体,将滤液稀释至 200 mL,测得c(Cu2+)=0.1 mol/L。已知:Cu2O+ H2SO4 =CuSO4+Cu+H2O。
下列说法正确的是
A. 得到白色沉淀亚硫酸钡
B. 原铜的硫化物中n(Cu)∶n(S)=2∶3
C. 最后所得的溶液最多可以溶解铁1.12 g
D. 灼烧后的固体中n(Cu2O)∶n(CuO)=1∶1
难度: 困难查看答案及解析
-
“低碳生活”可以理解为:减少二氧化碳的排放,低能量、低消耗、低开支的生活方式。下列行为不利于低碳生活的是

A. LED灯使用 B. 纸张双面打印
C. 多乘公共交通工具出行 D. 大量使用一次性餐具用品
难度: 简单查看答案及解析
-
无水氯化钙是一种价廉、优质的干燥剂,氯化钙属于
A. 酸 B. 碱 C. 盐 D. 混合物
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A. 氯化钠的分子式:NaCl B. 铝离子的结构示意图:
C. 葡萄糖的最简式:CH2O D. Ba(OH)2的电离方程式:Ba(OH)2=Ba2+ + OH-2
难度: 简单查看答案及解析
-
氢有三种同位素:1H、2H和3H,它们之间存在差异的是
A. 中子数 B. 电子数 C. 原子序数 D. 质子数
难度: 简单查看答案及解析
-
下列气体不能用向上排空气法收集的是
A. NO B. NO2 C. CO2 D. Cl2
难度: 简单查看答案及解析
-
下列互为同分异构体的是
A. 红磷和白磷 B. 16O和18O C. 甲烷和丁烷 D. CH3OCH3和CH3CH2OH
难度: 中等查看答案及解析
-
下列物质的主要成分不属于天然高分子的是
A. 淀粉 B. 蚕丝 C. 油脂 D. 纤维素
难度: 中等查看答案及解析
-
下列变化属于化学变化的是
A. 拨云见日 B. 花香四溢 C. 冰冻三尺 D. 酿谷成酒
难度: 简单查看答案及解析
-
下列有关物质应用的叙述中,正确的是
A. 明矾可用于水的杀菌消毒 B. 水玻璃可用作木材防火剂
C. Na2CO3可用于治疗胃酸过多 D. 焰色反应可用于鉴别NaCl和NaOH
难度: 中等查看答案及解析
-
下列物质中只含有共价键的是
A. N2 B. MgCl2 C. NH4Cl D. KF
难度: 简单查看答案及解析
-
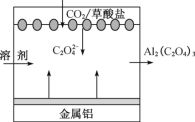
下列反应中热量变化与图一致的是
A. 天然气的燃烧 B. 油脂在人体内氧化
C. NaOH溶液和 HNO3溶液反应 D. 氢氧化钡晶体和氯化铵晶体反应
难度: 简单查看答案及解析
-
在含有大量SO42-、OH-、Na+的溶液中,还可能大量共存的离子是
A. Ba2+ B. Cl- C. Mg2+ D. HCO3-
难度: 中等查看答案及解析
-
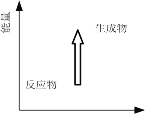
下列有关实验操作或现象描述正确的是( )
A. 实验室用图1装置制备Cl2
B. 加热后图2中溶液颜色恢复红色
C. 用图3装置除去Cl2中含有的少量HCl
D. 实验室用图4装置制取少量蒸馏水
难度: 简单查看答案及解析
-
实验室用铁片和稀硫酸制备H2。下列说法不正确的是
A. 升高温度能加快反应速率 B. 用铁粉代替铁片能加快反应速率
C. 滴入数滴CuSO4溶液能加快反应速率 D. 增加H2SO4用量能加快反应速率
难度: 中等查看答案及解析
-
高温时铁与水蒸气能发生反应:3Fe+4H2O(g)
Fe3O4+4H2,该反应属于
A. 置换反应 B. 分解反应 C. 化合反应 D. 复分解反应
难度: 简单查看答案及解析
-
苯是一种重要的有机化工原料,下列有关苯的叙述不正确的是
A. 分子式为C6H6 B. 属于不饱和烃
C. 密度比水小 D. 无色无毒的液体
难度: 简单查看答案及解析