-
中华传统文化蕴含着很多科学知识,下列说法错误的是
A. “丹砂(HgS烧之成水银,积变又还成丹砂”描述的是可逆反应
B. “水声冰下咽,沙路雪中平”未涉及化学变化
C. “霾尘积聚难见路人”形容的霾尘中有气溶胶,具有丁达尔效应
D. “含浆似注甘露钵,好与文园止消渴”说明柑橘糖浆有甜味,可以止渴
难度: 简单查看答案及解析
-
羟甲香豆素(
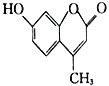 )是一种治疗胆结石的药物,下列说法正确的是
)是一种治疗胆结石的药物,下列说法正确的是A. 分子中的两个苯环都可以发生加成反应 B. 所有原子均处于同一平面
C. 二氯代物超过两种 D. 1mol羟甲香豆素与氢气加成,最多需要5molH2
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的数值。下列说法正确的是
A. 常温常压下,11.2L甲烷中含有的共价键数为2NA
B. 1 mol OH-中含有9NA个电子
C. 1L1mol·L-1AlCl3溶液中含有NA个Al3+
D. 3.2g由O2和O3组成的混合气体中含有的氧原子数为0.2NA
难度: 中等查看答案及解析
-
用下列装置完成相应的实验,能达到实验目的的是
A.
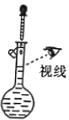 配制一定浓度的氯化钠溶液
配制一定浓度的氯化钠溶液B.
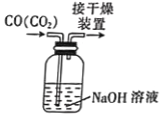 除去CO中的CO2
除去CO中的CO2C.
 中和滴定
中和滴定D.
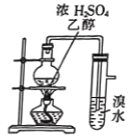 制取并检验乙烯
制取并检验乙烯难度: 中等查看答案及解析
-
短周期主族元素W、X,Y、Z的原子序数依次增大,四种原子的最外层电子数之和为18,W与Y同主族,X原子的最外层电子数等于周期数,Z的单质在常温下为气体,下列说法正确的是( )
A. 最简单氢化物的稳定性:Z>W>Y
B. 原子半径:Y>X>W
C. X与Z形成的化合物的水溶液能使红色石蕊试纸变蓝
D. Y的氧化物既能与碱反应,也能与酸反应,属于两性氧化物
难度: 中等查看答案及解析
-
一种正投入生产的大型蓄电系统如图所示。放电前,被交换膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述不正确的是

A. 放电时,负极的电极反应式为2S22――2e-===S42-
B. 充电时,阳极的电极反应式为3Br--2e-===Br3-
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 充电时,M接电源负极,N接电源正极
难度: 中等查看答案及解析
-
常温下,向25.00mL 0.1mol·L-1 HSCN溶液中滴入0.1 mol·L-1 NaOH溶液,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加NaOH溶液体积的关系如图所示,下列说法正确的是
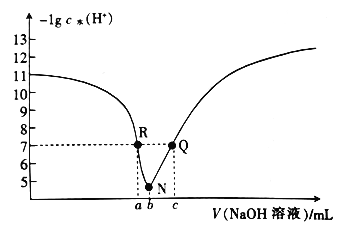
A. 常温下,Ka(HSCN)约为1×10-3
B. b=25.00
C. R、Q两点溶液对应的pH=7
D. N点溶液中:c(Na+)<c(SCN-)
难度: 困难查看答案及解析

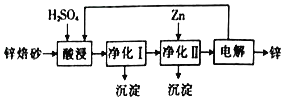
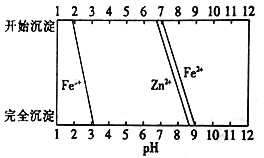
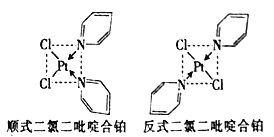

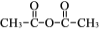 。
。 为原料制备
为原料制备 的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br
的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br