-
下列自然现象属于丁达尔效应的是
A. 雷雨天气
 B. 冬季雾凇
B. 冬季雾凇
C. 光照榕树
 D. 泥石流
D. 泥石流
难度: 简单查看答案及解析
-
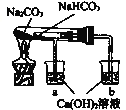
下列物质能与水发生氧化还原反应的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A. 金属钠 B. 硫酸钠 C. 食盐水 D. 碱石灰
难度: 简单查看答案及解析
-
配制一定物质的量浓度的溶液,不需要使用的仪器是
A. 烧杯 B. 玻璃棒 C. 容量瓶 D. 圆底烧瓶
难度: 简单查看答案及解析
-
下列物质不属于合金的是
A. 青铜器 B. 不锈钢 C. 合金钢 D. 金刚石
难度: 简单查看答案及解析
-
下列变化过程发生还原反应的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列有关金属钠与水反应的现象描述不正确的是
A. 钠熔成小球 B. 钠沉入水底
C. 钠四处游动 D. 发出嘶嘶声
难度: 简单查看答案及解析
-
下列实验装置可用于分离互不相溶的两种液体的是
A.
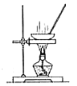 B.
B. 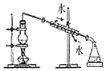 C.
C. 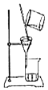 D.
D. 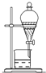
难度: 简单查看答案及解析
-
下列气体能使湿润红色布条褪色的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
常温时可以用铁制器皿存放的酸是
A. 稀硫酸 B. 稀醋酸 C. 浓盐酸 D. 浓硝酸
难度: 简单查看答案及解析
-
下列关于二氧化硫的说法正确的是
A.
能使溴水褪色,说明
具有还原性
B.
能使品红溶液褪色,说明
具有氧化性
C.
能与
反应生成
,说明
具有酸性
D.
能使酸性
溶液褪色,说明
具有漂白性
难度: 简单查看答案及解析
-
下列关于物质的用途说法不正确的是
A. 液氨作制冷剂 B. 过氧化钠作供氧剂
C. 氯气制漂白粉 D. 浓硝酸作干燥剂
难度: 简单查看答案及解析
-
如图是喷泉实验装置图,下列说法不正确的是
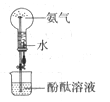
A. 烧瓶中的溶液呈红色
B. 该实验说明氨气属于碱
C. 该实验说明氨气极易溶于水
D. 形成喷泉的原因是烧瓶内压强小于外界大气压
难度: 简单查看答案及解析
-
下列溶液含有的氯离子物质的量浓度最大的是
A.
溶液 B.
溶液
C.
溶液 D.
溶液
难度: 简单查看答案及解析
-
下图是氮元素的循环示意图,下列说法不正确的是
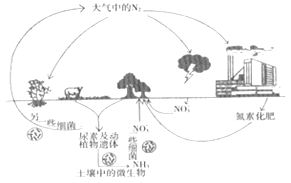
A.
均由氮气经氧化反应得到
B. 氮素化肥的生产属于人工固氮
C. 循环中氮元素发生氧化、还原反应
D. 尿素及动植物的遗体一定含氮元素
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 铁与稀硫酸反应:
B. 稀盐酸除碳酸钙水垢:
C. 浓硝酸与铜反应:
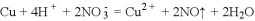
D. 氢氧化钡溶液与稀硫酸反应:
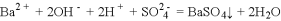
难度: 简单查看答案及解析
-
下列有关酸雨说法不正确的是
A. 酸雨形成过程中一定有氧化还原反应发生
B. 煤和石油的燃烧是酸雨污染物的唯一来源
C. 二氧化硫以及氮氧化物是形成酸雨的主要因素
D. 酸雨的危害有使土壤、湖泊酸化以及加速建筑物、桥梁的腐蚀等
难度: 简单查看答案及解析
-
下列说法正确的是
A.
的摩尔质量是
B. 常温常压下,
的体积是
C.
中含有的氯原子数约为
D.
与足量
反应转移
电子
难度: 简单查看答案及解析
-
下列有关铜与浓硫酸反应的实验说法不正确的是

A. 喷有碱液的棉花是为了防止SO2污染环境
B. 将水注入反应后冷却的试管a中,溶液变为蓝色
C. 铜片表面先发黑,反应完全后试管a底部有白色固体
D. 反应的化学方程式是Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
难度: 中等查看答案及解析
-
下列“实验结论”与“实验操作及现象”相符的一组是
选项
实验操作及现象
实验结论
A
向某溶液中加入
溶液,有白色沉淀生成
该溶液中一定含有
B
向某溶液中加入稀盐酸,有无色气体产生
该溶液中一定含有
C
向某溶液中加入
溶液,有白色沉淀生成
该溶液中一定含有
D
向某溶液中加入酚酞溶液,溶液变为红色
该溶液中一定含有
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
以空气中的氮气为原料制备硝酸,合成线路如下(反应条件及部分反应物、生成物已略去)。
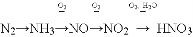
已知空气中含氮气的体积分数为78%,若用
(已折算成标准状况下)空气制备硝酸,则理论上可制得硝酸的量的计算式正确的是
A.
B.
C.
D.
难度: 简单查看答案及解析

 _____________
_____________