-
下列变化中,一定发生了化学变化的是
A.澄清的石灰水变浑浊 B.爆炸 C.海水晒盐 D.剩饭久放有馊味
难度: 简单查看答案及解析
-
下列物质按混合物、单质顺序进行分类的是
A.冰水共存物 氢气 B.四氧化三铁 金刚石
C.盐 酸 臭氧 D.空气 钢
难度: 简单查看答案及解析
-
下列实验的基本操作正确的是
A.
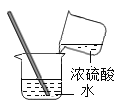 浓硫酸的稀释
浓硫酸的稀释B.
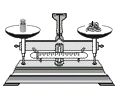 称量一定质量的食盐
称量一定质量的食盐C.
 闻气味
闻气味D.
 CO2验满
CO2验满难度: 简单查看答案及解析
-
下列实验现象的描述与事实不符的是( )
A.红磷在氧气中燃烧产生大量白烟
B.氢气在空气中燃烧产生淡蓝色火焰
C.二氧化碳通入紫色石蕊溶液中变蓝色
D.打开盛有浓盐酸的试剂瓶后,瓶口出现白雾
难度: 中等查看答案及解析
-
生活离不开化学,下列认识正确的是
A.煤炉生火时,用木材引燃是为了提高煤的着火点
B.用硬水洗涤衣物,既浪费肥皂,也洗不净衣物
C.用洗涤剂除油污是因为洗涤剂能将油污溶解,形成溶液
D.用食盐水除去菜刀表面的锈斑
难度: 中等查看答案及解析
-
有关物质的应用叙述不正确的是
A.油能隔绝空气和水,涂油可防止钢铁生锈
B.一氧化碳易与血红蛋白结合能使人中毒
C.石墨能导电,可用作电极
D.焦炭具有氧化性,可用于冶金工业
难度: 简单查看答案及解析
-
大蒜素的化学式为C6H10S3,下列说法正确的是
A.大蒜素分子中氢元素的质量分数最低
B.大蒜素属于氧化物
C.大蒜素由6个碳原子、10个氢原子和3个硫原子构成
D.大蒜素中碳元素、氢元素和硫元素的质量比为36:5:48
难度: 中等查看答案及解析
-
建立宏观与微观的联系是化学学科特有的思维方式。对下列事实的解释错误的是
A.花香四溢——分子不断运动
B.烧碱溶液、石灰水均显碱性——溶液中都含有金属离子
C.CO和CO2的化学性质不同——分子构成不同
D.石墨变为金刚石——碳原子的排列方式发生改变
难度: 简单查看答案及解析
-
在一定条件下,下列转化不能一步实现的是
A.CO2→CaCO3 B.HCl→NaCl C.Al2O3→AlCl3 D.Fe→Fe2(SO4)3
难度: 中等查看答案及解析
-
下列推理正确的是
A.离子是带电的粒子,带电的粒子一定是离子
B.物质与氧气发生的反应是氧化反应,氧化反应一定是物质与氧气的反应
C.活泼金属可与酸发生置换反应,置换反应一定是金属和酸的反应
D.最外层电子数为8的粒子不一定都是稀有气体元素的原子
难度: 中等查看答案及解析
-
把X、Y两种金属分别放入另外两种金属Z、M的盐溶液中,实验结果如下表,其中“/”表示金属与盐不反应, “√”表示金属与盐能反应。
金属 溶液
Z的盐溶液
M的盐溶液
X
∕
√
Y
∕
∕
上述四种金属活动性由强到弱的顺序是( )
A.Z、M、X、Y B.M、X、Z、Y C.Z、X、M、Y D.Z、Y、X、M
难度: 简单查看答案及解析
-
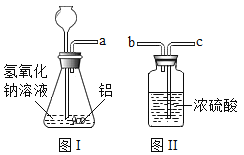
下列实验进行中的现象或实验原理正确的是
A.
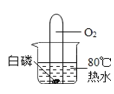 白磷始终不燃烧
白磷始终不燃烧B.
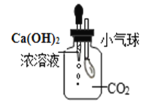 小气球变瘪
小气球变瘪C.
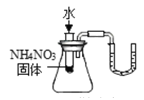 U型管内液面左高右低
U型管内液面左高右低D.
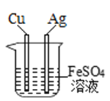 验证Fe、Cu、Ag的金属活动性强弱
验证Fe、Cu、Ag的金属活动性强弱难度: 中等查看答案及解析
-
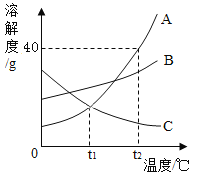
下列图象能正确反映其对应关系的是
A.
某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度
B.
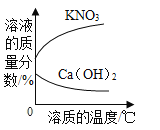 加热的饱和溶液的KNO3和饱和溶液的Ca(OH)2(不考虑溶剂的蒸发)
加热的饱和溶液的KNO3和饱和溶液的Ca(OH)2(不考虑溶剂的蒸发)C.
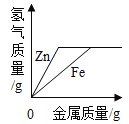 向等质量、等浓度的稀硫酸中分别加入过量的Zn和Fe
向等质量、等浓度的稀硫酸中分别加入过量的Zn和FeD.
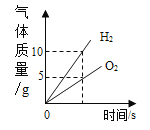 将水通电一段时间
将水通电一段时间难度: 困难查看答案及解析
-
硫铁矿烧渣(主要成分Fe2O3、FeO、SiO2).现取含Fe2O3、FeO、SiO2混合物100吨,测得其中含硅量为28%,则通过炼制得到铁的质量不可能是(假设铁无损耗)
A.29吨 B.32吨 C.31吨 D.30吨
难度: 中等查看答案及解析