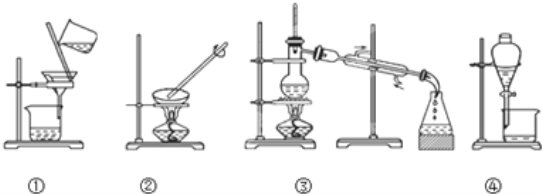
-
实验室制取Cl2及性质的验证实验组合装置如下,请回答下列问题:
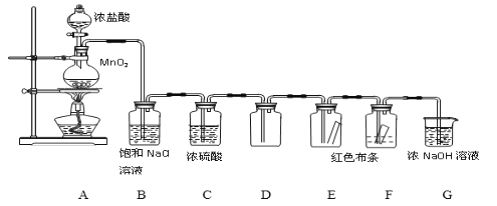
(1)图中装浓盐酸的玻璃仪器名称是________________,
(2)A中发生的离子方程式为____________________________________,若产生的氯气标准状况下为5.6L,参加反应的二氧化锰为_______克。
(3)装置D采用向上排空气收集氯气的原因是_______________________。
(4)能证明干燥的氯气没有漂白性的现象是________________________。
(5)B的作用是____________,G中的化学方程式为________________________。
-
某化学兴趣小组为检验木炭和浓硫酸反应生成的产物,设计如图装置(已知SO2能使溴水褪色),请回答:
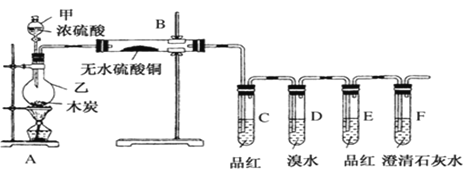
(1)试管D中发生反应的化学方程式为______________________;
(2)试管B中现象是_________________________;
(3)F试管中澄清石灰水的作用是__________________________;
(二)同时该小组设计如下图所示的实验装置(固定装置略),进行SO2性质的研究:
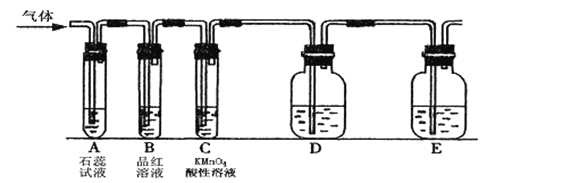
(4)当通入SO2时,A中紫色石蕊溶液变红,用化学方程式解释其原因是___________。
(5)可用来验证SO2具有漂白性的现象是:_______________________。
(6)从元素化合价的角度分析,SO2的性质:
①当通入SO2一段时间后,可观察C中溶液褪色,说明SO2具有_____________性。
②如要验证SO2还具有另一方面的性质,D装置中的药品应为_____________。
A.FeCl3溶液B.氯水C.氢硫酸D.浓硝酸
-
(一)某课外小组为了检验Na2O2与水反应的产物,设计如图装置(夹持装置已省略):(14分2分一空)
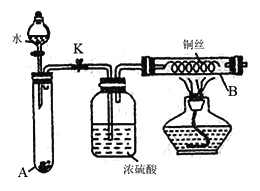
(1)装置B中的现象为____________________________ 。
(2)反应完全后向装置A中滴入几滴酚酞试液,现象为__________________。
(3)写出Na2O2与水反应的离子方程式: ______________________________。
(二)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。 请回答该实验中的问题。
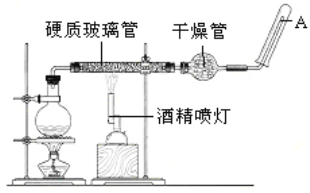
(4)圆底烧瓶中盛装水,烧瓶里应事先放置碎瓷片,其作用是______________。
(5)若该反应的化学方程式为3Fe+4H2O(g) Fe3O4+4H2,求16.8克铁粉完全反应转移的电子为___________mol。
Fe3O4+4H2,求16.8克铁粉完全反应转移的电子为___________mol。
(6)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是_________,若溶液未变红色则说明硬质试管中固体物质的成分____________。