-
(一)某课外小组为了检验Na2O2与水反应的产物,设计如图装置(夹持装置已省略):(14分2分一空)
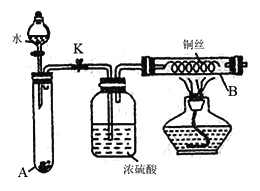
(1)装置B中的现象为____________________________ 。
(2)反应完全后向装置A中滴入几滴酚酞试液,现象为__________________。
(3)写出Na2O2与水反应的离子方程式: ______________________________。
(二)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。 请回答该实验中的问题。
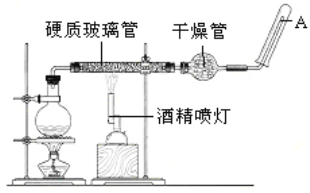
(4)圆底烧瓶中盛装水,烧瓶里应事先放置碎瓷片,其作用是______________。
(5)若该反应的化学方程式为3Fe+4H2O(g) Fe3O4+4H2,求16.8克铁粉完全反应转移的电子为___________mol。
Fe3O4+4H2,求16.8克铁粉完全反应转移的电子为___________mol。
(6)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是_________,若溶液未变红色则说明硬质试管中固体物质的成分____________。
-
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象____________。
(2)U形管中溶液的颜色____________,说明有______生成。
(3)铜丝的变化现象______,说明有_____生成。
-
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象________。
(2)U形管中溶液的颜色_____,说明有__________生成。
(3)铜丝的变化现象____________,说明有________生成;若去掉后面的装置,简述检验气体的方法____
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______。
-
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。
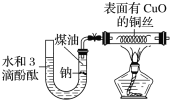
根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象________。
(2)U形管中溶液的颜色_____,说明有__________生成。
(3)铜丝的变化现象____________,说明有________生成;若去掉后面的装置,简述检验气体的方法____
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______。
-
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿加热铜丝。
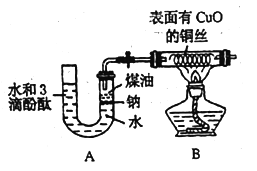
根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象____________。
(2)U形管中溶液的颜色____________,说明有______生成。
(3)铜丝的变化现象______,说明有_____生成。
-
I.某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和儿粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿点燃酒精灯加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)反应过程中金属钠除了逐渐变小外,还有什么现象? 。请写出该反应的化学方
程式为________________。
(2)铜丝的变化现象 ,反应的化学方程式是 ,
II.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
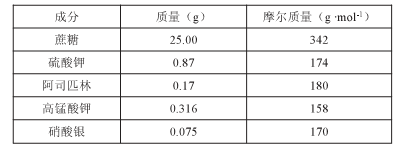
(1)配制1L上述“鲜花保鲜剂”所需 的仪器有:量筒、玻璃棒、药匙、烧杯、托盘天平、 、 。(在横线上填写所缺仪器的名称)。
的仪器有:量筒、玻璃棒、药匙、烧杯、托盘天平、 、 。(在横线上填写所缺仪器的名称)。
(2)在溶液配制过程中, 下列操作对配制结果没有影响的是 。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(3)一鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 mol/L。
-
(16分)某课外学习小组在学习了Na2O2与CO2的反应后,认为Na2O2与SO2应该也可以反应。他们设计了下图装置(夹持装置已略去,装置的气密性良好)进行实验,探究SO2与Na2O2反应的产物,请按要求回答下列问题。
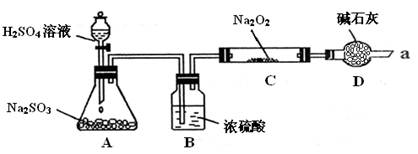
Ⅰ﹒写出装置A中发生反应的化学方程式:___________________________
Ⅱ﹒装置D的作用:除了可以防止空气中的CO2、水蒸气等进入C中与Na2O2反应,还可以_____________
Ⅲ﹒在通入足量的SO2与Na2O2充分反应后,他们对C中固体产物提出如下假设:
假设1:只有Na2SO3;
假设2:_________;
假设3:既有Na2SO3,又有Na2SO4。
(1)若假设1成立,写出SO2与Na2O2反应的化学方程式:________________
(2)为进一步确定C中反应后固体产物的成分(Na2O2已反应完全),甲同学设计了如下实验:

甲同学由此得出结论:产物是Na2SO4,该方案是否合理______(填“是”或“否”),理由是_____________
(3)乙同学设计了如下实验验证假设3成立,请帮助他完成下表。
| 实验步骤 | 现象 |
| ①取少量C中固体产物于试管中,加入适量的蒸馏水溶解。 | 固体全部溶解 |
| ②向上试管中加入过量的_____________,将产生的气体通入少量酸性KMnO4溶液中。 | KMnO4溶液__________ |
| ③向步骤②反应后的试管中,加入适量的BaCl2溶液。 | 产生白色沉淀 |
步骤②中将产生的气体通入少量酸性KMnO4溶液中,发生反应的离子方程式为:__________
-
某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如下装置进行实验(夹持仪器已省略)。
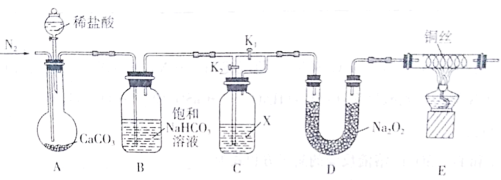
回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是________。
(2)饱和NaHCO3溶液的作用是_________;试剂X是___________。
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是_______。
(4)若_____(填操作),E中灼热的铜丝变为黑色,可证明潮湿的CO2能与Na2O2反应。
(5)写出D中CO2与Na2O2反应的化学方程式___________。
-
(10分)某校化学课外活动小组学生利用如图所示装置进行铁与水反应”的实验,并利用产物进一步与氧化铁反应(图中夹持及其他后续装置均已省略).碱石灰是一种固体干燥剂,其中含有氢氧化钠和生石灰等物质.
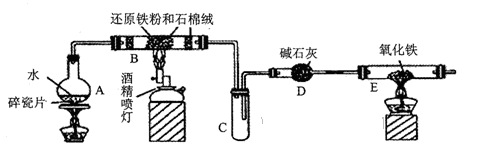
(1)圆底烧瓶中盛装的是水,该装置受热后的主要作用是___________;装置B中发生反应的化学方程式____________.
(2)碱石灰的作用是___________.
(3)实验过程中最后点燃的是___________(填编号)
①A处酒精灯 ②B处酒精喷灯 ③E处酒精灯
(4)装置E中的现象是 .
-
某课外小组同学设计如图实验装置(部分夹持仪器未画出)探究氨气的还原性并检验部分产物。
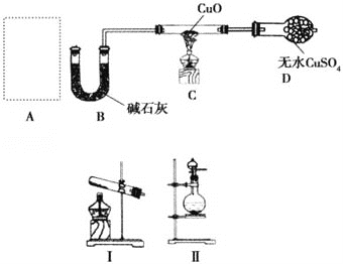
(1)若A中使用装置Ⅰ制取氨气,则化学方程式为__,发生装置试管口略向下倾斜的原因_____;若A中使用装置Ⅱ制取氨气,则分液漏斗中的试剂为__,圆底烧瓶中的固体可以为__。
(2)B中碱石灰的作用是__。
(3)氨气还原炽热氧化铜的化学方程式为__,装置C中的实验现象为__,装置D中的实验现象为__。
(4)①该装置存在明显的缺陷是__。
②请画出改进后需要增加连接的实验装置图________。


Fe3O4+4H2,求16.8克铁粉完全反应转移的电子为___________mol。










