-
化学与生产和生活密切相关,下列过程中没有发生化学变化的是
A. 铁生锈 B. 电解饱和食盐水制氯气
C. 用酒精擦洗布料上的油污 D. 用食醋除去水壶内的水垢
难度: 简单查看答案及解析
-
对16O叙述正确的是
A. 16O原子的核外电子数为8 B. 16O与 18O 互为同素异形体
C. 16O的中子数为16 D. 氧元素的近似相对原子质量是16
难度: 简单查看答案及解析
-
下列电子层上运动的电子能量最低的是
A. L B. K C. N D. M
难度: 简单查看答案及解析
-
既含离子键又含共价键的物质是
A. H2 B. NaOH C. H2O D. MgC12
难度: 简单查看答案及解析
-
下列化学用语能确定为水的是
A. H3O+ B. H-O-H C.
D.
难度: 简单查看答案及解析
-
不能用单质直接反应得到的是
A. NaCl B. FeCl2 C. AlCl3 D. MgCl2
难度: 简单查看答案及解析
-
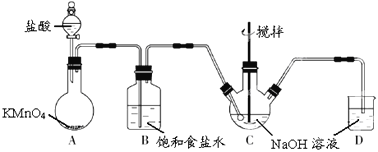
工业上仅以食盐和水为原料,不能得到的产品是
A. 烧碱 B. NaClO溶液 C. 盐酸 D. 氮肥NH4Cl
难度: 简单查看答案及解析
-
下列物质属于分子晶体的是
A. CaO B. CO2 C. SiO2 D. NaCl
难度: 简单查看答案及解析
-
下列微粒只有还原性的是
A. H + B. Fe2+ C. Br - D. Cl2
难度: 简单查看答案及解析
-
下列变化属于氧化-还原反应的是
A. CaCO3
CaO+CO2↑ B. 2KI+Br2→2KBr+I2
C. NaCl+H2SO4
NaHSO4+HCl↑ D. NH4Cl
NH3↑+HCl↑
难度: 简单查看答案及解析
-
下列物质是纯净物的是
A. 氯水 B. 液态氯化氢 C. 食醋 D. 漂粉精
难度: 简单查看答案及解析
-
检验氯气方法不合理的是
A. 碘水 B. 湿润的淀粉KI试纸
C. 含淀粉的NaI溶液 D. 湿润的蓝色石蕊试纸
难度: 简单查看答案及解析
-
最容易与氢气反应的物质是
A. F2 B. Br2 C. Cl2 D. I2
难度: 简单查看答案及解析
-
下列试剂保存不正确的是
A. 碘必须保存在苯中 B. 新制的氯水用棕色试剂瓶装并密封保存
C. 白磷保存在水中 D. 液溴用一薄层水封盖再密闭保存于低温处
难度: 简单查看答案及解析
-
能证明NaCl是离子化合物的事实是
A. 常温下是固体 B. 熔融态能导电 C. 水溶液能导电 D. 易溶于水
难度: 简单查看答案及解析
-
漂粉精暴露在潮湿的空气中易失效,其原因与下列叙述无关的是
A. HClO的酸性比H2CO3弱 B. Ca(ClO)2是盐
C. HClO见光易分解 D. Ca(ClO)2能与碳酸反应
难度: 简单查看答案及解析
-
下列各组气体与对应的液体或溶液不易产生喷泉现象的是
选项
A
B
C
D
气体
HCl
HCl
CO2
HCl
液体
H2O
CCl4
NaOH
AgNO3
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
能在溶液中大量共存的离子组合是
A. Ba2+ 、H+ 、Cl-、CO32- B. H+ 、Ag+ 、Cl-、ClO-
C. Mg2+、Na+、Cl-、SO42- D. Cu2+ 、Mg2+ 、OH-、Br-
难度: 中等查看答案及解析
-
下列反应能用离子方程式CO32-+2H+==CO2↑+H2O表示的是
A. 石灰石与足量盐酸反应 B. 碳酸钠与足量盐酸反应
C. 碳酸钠与足量醋酸反应 D. 碳酸钡与足量硝酸反应
难度: 中等查看答案及解析
-
下列有关化学基本概念的判断依据正确的是
A. 弱电解质:溶液的导电能力弱 B. 共价化合物:含有共价键
C. 离子化合物:含有离子键 D. 分子晶体:常温下不导电
难度: 简单查看答案及解析
-
关于阿佛加德罗常数(NA)的说法正确的是
A. 1 mol NaCl的质量是58.5 g
B. 标况下,NA个水分子所占的体积是22.4 L
C. 常温下,1 mol任何气体的体积都不可能是22.4 L
D. 标况下,44 g CO2分子中含有NA个氧分子
难度: 中等查看答案及解析
-
标准状况下将充满HCl气体的烧瓶倒置于水中,水充满整个烧瓶后,溶液的物质的量浓度是(假设HCl没有扩散到瓶外)
A. 1mol/L B. 22.4mol/L C.
mol/L D. 无法确定
难度: 中等查看答案及解析
-
下列化工生产不符合实际的是
A. 海水提溴时用到热空气将Br2吹出
B. 工业制HCl时氯气在氢气中燃烧
C. 将氯气通入石灰乳中制取漂粉精
D. 钠在氯气中燃烧生产氯化钠
难度: 简单查看答案及解析
-
用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是
A. 实验使用的主要仪器是分液漏斗
B. 分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
C. 碘的四氯化碳溶液呈紫红色
D. 碘在四氯化碳中的溶解度比在水中的溶解度大
难度: 简单查看答案及解析
-
关于溴和碘的说法中不合理的是
A. 碘单质是从海水中大量提取的 B. 溴水可使湿润的淀粉KI试纸变蓝
C. 单质碘易升华 D. 单质溴是一种深红棕色液体
难度: 简单查看答案及解析
-
下列关于卤族元素结构和性质的说法错误的是
A. F、Cl、Br、I原子半径依次增大
B. F、Cl、Br、I的电子层数逐渐增多
C. F-、Cl-、Br -、I-离子的还原性依次减弱
D. F2、Cl2、Br2、I2的氧化性逐渐减弱
难度: 简单查看答案及解析
-
可采用NaCl(s)+NaHSO4(s)→Na2SO4+HCl↑制备HCl,下列气体的制备与上述反应装置相同的是
A. 氧气:2H2O2
2H2O+O2↑
B. 氢气:2Al+6HCl→2AlCl3+3H2↑
C. 氯气:KClO3(s)+6HCl(浓)
KCl+3Cl2↑+3H2O
D. 氧气:2KMnO4
K2MnO4+MnO2+O2↑
难度: 简单查看答案及解析
-
下列装置不能达到除杂目的(括号内为杂质)的是
A. Cl2(HCl)
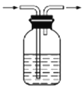 B. 苯(水)
B. 苯(水)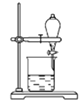
C. NaCl固体(碘固体)
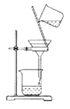 D. I2(CCl4)
D. I2(CCl4)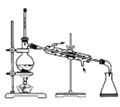
难度: 中等查看答案及解析
-
标准状况下实验室用浓盐酸与二氧化锰反应制取氯气,MnO2+ 4HCl(浓)
MnCl2 + Cl2 + 2H2O,下列有关说法中正确的是
A. MnO2被氧化
B. 浓盐酸仅体现还原性
C. 若有0.4 mol HCl参与反应,则可制得氯气2.24 L
D. 若有0.4 mol HCl被还原,则可制得氯气2.24 L
难度: 中等查看答案及解析
-
某固体混合物中可能含有:K+、Na+、Clˉ、CO32—、SO42—等离子,将该固体溶解所得到的溶液进行如下实验:
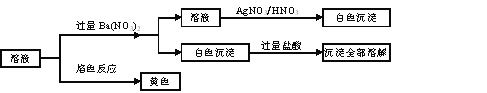
下列说法正确的是
A. 该混合物一定是Na2CO3和NaCl B. 该混合物可能是Na2CO3和KCl
C. 该混合物一定是K2CO3和NaCl D. 该混合物可能是Na2SO4和Na2CO3
难度: 中等查看答案及解析